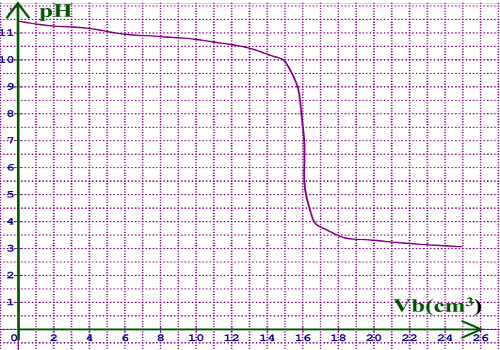
titrage d'un acide faible par une base forte
|
Cours-titrage-acide-base-2ème-annnée-pdf
du titrage d'une base faible par un acide fort le pH au point d'équivalence est toujours inférieur à 7 (point d'équivalence en zone acide) Page 8 8 Courbe |
|
Chimie Analytique I: Chapitre 8 Les titrages acido-basiques
Ceci contraste avec le titrage d'un acide fort par une base forte où le pH au point d'équivalence est neutre Plus l'acide est faible plus sa base conjuguée |
|
Dosages acidobasiques
il y a 5 jours · Le dosage d'un acide faible est différent de celui d'un acide fort car la réaction de dissociation avec l'eau pour libérer un ion hydronium H3O+ |
|
Dosage acide faible – base forte
dosage d'un acide faible (pKa=5 ca=0 01 mol L -1 ) par une base forte (cb=0 1 mol L-1) x = n base versé / n acide initial 0 0 0 2 0 4 0 6 0 8 1 0 1 2 |
Comment déterminer un acide faible ?
Le pKa va permettre de déterminer la force d'un acide.
En effet, plus l'acide est fort, plus sa réaction avec l'eau est importante voire totale pour former des ions oxonium H3O+ donc plus le Ka est élevé et, par conséquent, plus le pKa est faible.1.
3) L'échelle de pH Le pH d'une solution est compris entre 0 et 14. - Si pH < 7, la solution est acide. - Si pH = 7, la solution est neutre. - Si pH > 7, la solution est basique.
Pourquoi le pH est inférieur à 7 à l'équivalence ?
Notez en particulier que le pH au point d'équivalence dans le titrage d'une base faible est inférieur à 7,00 parce que le titrage produit un acide.
|
Dosage acide faible – base forte
Dosage acide faible – base forte Acide faible HA : constante d'acidité Ka titré Ceci implique que l'acide ne soit pas trop fort ou trop dilué pour que sa |
|
COURS DE CHIMIE GENERALE Semestre 1 SVI - Université Cadi
Calcul du pH de ST 4 Titrages acide-base 1 1 Titrage d'un acide fort par une base forte 1 2 Titrage d'un acide faible par |
|
C2 - DOSAGE ACIDE FAIBLE - BASE FORTE - Texas Instruments
Une solution de base forte de concentration connue (NaOH à 0,2 mol L– 1 par exemple) • Une solution d'acide faible de concentration inconnue (ac acétique |
|
§ 7 (suite) Titrages acide-base - EPFL
Considérons le titrage d'une solution d'un acide faible, tel que l'acide acétique par exemple, par une base forte, comme NaOH La fonction pH = ƒ() dans ce cas |
|
Informatique Titrage acide/base - Cours dinformatique
17 avr 2013 · Dans le cas du titrage d'un acide fort par une base forte, Figure 7 Diagramme de bilan Acide faible / Base forte 2 4 2 Le pH à la moitié de l' |
|
Chapitre 1 Acides et bases
La base conjuguée d'un acide fort est dite “indifférente dans l'eau”, i e cette 1) L'ammoniaque est une base faible dans l'eau (cf plus haut), le pKa du couple où cA et cB sont les concentrations respectives de l'acide à titrer et de la base |
|
Dosage pH-métrique dun acide fort par une base forte
Figure 12 : équation de la réaction de titrage d'un acide faible par une base forte 42 Figure 13 : tableau d'avancement de la réaction entre l'acide |
|
VIEtude sommaire des mélanges
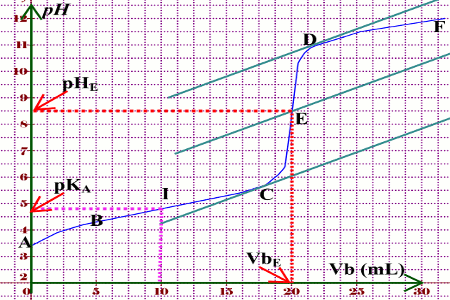
2) Titrage d'un acide faible par une base forte: 20 ml CH3COOH (pKa = 4,75) ±0, 10 mol/l (en principe de concentration inconnue au début du titrage) titrés par |