enthalpie libre standard de formation
|
CHM-1903 Chimie des eaux
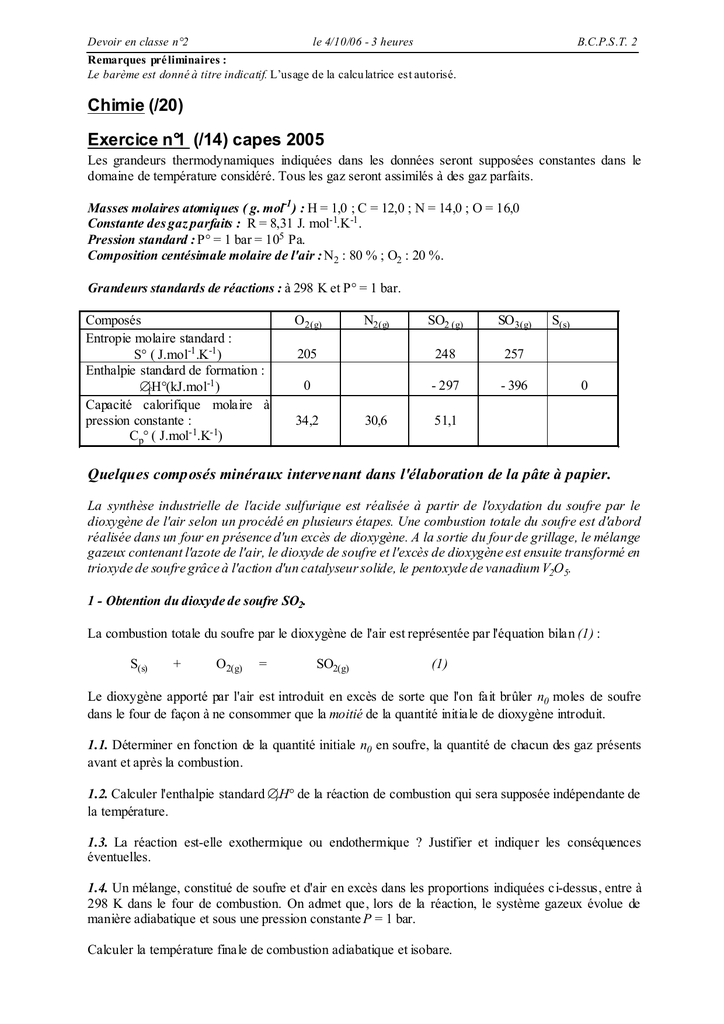
25 août 2015 · Données thermodynamiques pour les composés inorganiques à 25°C et P°=1 bar Enthalpie de formation standard Enthalpie libre de formation |
|
Enthalpie libre standard de réaction
Enthalpie libre standard de réaction et prédiction de réaction La réaction est favorisée car les produits formés sont stables et leur formation libère de |
|
Fascicule TDThermo L1SV 2014-2015pdf
a) Calculer l'enthalpie libre standard de formation de l'ammoniac à 298 K 1/2 N2 b) Déterminer l'enthalpie libre standard de formation de l'ammoniac à 500 K |
|
Lenthalpie libre standard ΔG°r 298 de la réaction
Par convention quelle que soit la température l'enthalpie de formation d'un corps pur dans état standard est prise égale à 0J ΔH°r298 =2 x (216)-0 -0 |
|
La Thermodynamique
L'enthalpie libre standard de formation ΔfG° (kJ/mol) 26 75 502 31 77 L'entropie standard de formation ΔfS° (J/K mol) -42 -134 -209 Exercice N°3 Soit |
|
Les processus spontanés
L'enthalpie libre standard de formation • l'enthalpie libre standard de formation ∆G f o d'un composé est la variation d'enthalpie libre qui se produit |
|
Quelques enthalpies standard de formation (∆Hf°) à 25°C: Substance
Enthalpie standard de formation (∆Hf°) Enthalpie standard de formation (∆Hf°) H2O(l) - 285 9 kJ C2H5OH(l) -280 4 kJ H2O(g) - 241 9 kJ C6H6 -50 2 kJ CO2 |
|
Thermochimie/equilibres chimiques
✓ Par convention l'enthalpie standard de formation des corps simples (dans leur état normal à 25°C (298K) et sous P = 1 atm) est égal à zéro ΔH°f(N2) = 0 0 |
Comment calculer l'enthalpie libre standard de formation ?
Δ r C p = ∑ ν i .
C p i , où représente le coefficient stœchiométrique associé au composé dans la réaction , ( étant positif pour les produits formés et négatif pour les réactifs) et C p i la capacité calorifique molaire à pression constante du composé .C'est quoi l'enthalpie libre standard ?
L'enthalpie libre standard de formation d'un composé est la valeur de ΔG0r de la réaction de formation d'une mole du composé à partir des corps simples dans leur forme la plus stable et dans les conditions standard.
La forme la plus stable d'un corps simple est l'état dans lequel son enthalpie libre est la plus faible.Comment calculer ∆ G ?
ΔG = ΔG� + R.T.ln K
ΔG = variation de l'enthalpie (énergie) libre du système réactionnel, ΔG° = variation de l'enthalpie libre standard définie comme ci-dessus.Calculer l'enthalpie standard ΔH°r,298K de la réaction suivante :
1CO (g)+ 3H2(g) → CH4(g) + H2O (l) a) En déduire la valeur de l'énergie interne ΔU°r,298K de la même réaction.
2) CO (g) + 1/2O2 (g) → CO2 (g) ΔH°r,298K (1) = -283 kJ.
3) H2 (g) + 1/2O2 (g) → H2O (l) 4CH4 (g) + 2O2 (g) → CO2 (g) + 2H2O (g)
|
4. Thermochimie
On définit l'enthalpie standard de formation ?H0f d'une substance comme l'enthalpie standard L'enthalpie libre standard de formation d'un composé est la. |
|
Enthalpie libre évolution et équilibre
Enthalpie libre standard de réaction : ? G enthalpie libre de formation données dans les tables thermodynamiques. (remarque : même convention que pour ... |
|
Enthalpie libre Equilibres chimiques
II-1-Enthalpie libre standard de formation ?fG°T. II-2-Enthalpie libre standard de réaction ?rG°T. III-L'enthalpie libre molaire- Equilibre chimique. |
|
Les dosages acido-basiques
enthalpie libre de formation standard ?fG° (en kJ.mol-1) |
|
La chimie
L'enthalpie libre standard de formation. • l'enthalpie libre standard de formation ?G f o |
|
Thermodynamique de loxydoréduction
Ecrire la réaction de la pile qui a lieu lorsque la pile débite. 3. Calculer l'enthalpie libre standard de formation du chlorure mercureux solide à 25°C. |
|
Thermodynamique des réactions doxydoréduction; formule de
II.2 Enthalpie libre standard d'une demi-équation rédox et potentiel standard d'un couple rédox. Soit la réaction d'équation schématique Ox + n/2 H2(g) |
|
Reaction chimique - Thermodynamique - Cinétique
Notée ?fHo ; elle correspond à l'enthalpie standard de formation d'un corps Mesure directe d'une enthalpie libre de réaction : construction d'une pile ... |
|
CHAPITRE VII : Energie et enthalpie libres – Critères dévolution d
L'enthalpie libre standard de formation d'un composé est définie comme étant la variation d'enthalpie libre accompagnant la réaction de formation de ce |
|
Thermodynamique de la transformation chimique
L'enthalpie standard de formation d'un composé chimique est l'enthalpie Calcul de l'enthalpie libre standard de réaction et de la constante d'équi-. |
|
Tables des enthalpie de formation standard fH° (en kJmol
Tables des enthalpie de formation standard ? fH° (en kJ mol-1) enthalpie libre de formation standard ? fG° (en kJ mol-1) entropie standard So (en J K-1 mol-1) des corps purs à 29815 K Nom Formule Etat physique 0 ? fH 0 f G S o A acétone CH3COCH3(g) -2167 -1527 3042 acétone CH3COCH3(l) -2482 -1557 |
|
Enthalpie libre ; évolution et équilibre - Le Mans University
Enthalpie libre ; évolution et équilibre I Enthalpie libre 1 Définition G = H – TS G fonction d’état extensive s’exprime en joule Rq : elle se calcule à l’aide des potentiels chimiques ? (sera vu en 3ème année) 2 Variation élémentaire d’enthalpie libre dG = dH – TdS – SdT dG = dU + PdV + VdP – TdS + SdT |
|
La thermodynamique II - University of Ottawa
L'enthalpie libre standard de formation • l'enthalpie libre standard de formation DG f o d'un composé est la variation d'enthalpie libre qui se produit quand une mole d'un composé est synthétisée à partir de ses éléments à leur état standard • par définition DG f o d'un élément dans son état standard est zéro • ex ; la |
|
5 Equilibres chimiques - EPFL
L’enthalpie libre molaire de l’un des constituants d’un mélange ne peut évidemment pas être donnée dans des conditions standard puisqu’il n’apparait pas à l’état pur ?G = n R T ln P f P i Nous venons de voir que pour un gaz parfait : Pour une opération virtuelle qui consisterait à faire passer une mole de gaz pur |
|
EPFL
EPFL |
|
Searches related to enthalpie libre standard de formation PDF
1-Calculer la variation d’entropie standard à 25°C accompagnant les réactions de dissociation des composés NO 2 (g) et CaCO 3 (s) selon les schémas réactionnels suivants : 1 NO 2 (g) O 2 (g) +1/2 N 2 (g) 2 CaCO 3 (s) CO 2 (g) + CaO (s) 2-Calculer l’enthalpie libre standard (?G°) à 25°C de la réaction suivante : N 2 |
Comment calculer l’enthalpie libre de formation données dans les tables thermodynamiques ?
?G0enthalpie libre de formation données dans les tables thermodynamiques (remarque : même convention que pour ?fH° c’est-à-dire ?fG° = 0 pour les corps purs simples) • soit à partir de la relation : rr r ?G (298)00 0=??H (298) T.?S (298)
Comment calculer l'enthalpie libre ?
Variation élémentaire d’enthalpie libre dG = dH – TdS – SdT dG = dU + PdV + VdP – TdS + SdT dG = ?Q – PdV + PdV + VdP – TdS +SdT or ?Q = TdS dG = VdP - SdT 3. Influence de la température Toutes autres variables étant maintenues constantes :
Qu'est-ce que l'enthalpie standard de formation?
On dé?nit l’enthalpie standard de formation?H0f d’une substance comme l’enthalpie standard de la réaction formant une mole de la substance à partir de ses éléments constitutifs dans leur forme simple la plus stable.
Quel est le signe de la variation d’enthalpie libre de la réaction ?
La comparaison de Q ret K° permet de trouver le signe de la variation d’enthalpie libre de la réaction et de connaître l’évolution. Exemple d’application: Soit un système à 298K contenant du diazote, du dihydrogène et de l’ammoniac avec les pressions partielles respectives : 2 bar, 1 bar et 3 bar.
| Enthalpie libre ; évolution et équilibre - Le Mans University |
| Exemples d’enthalpies standard - Sélection de votre |
| Chapitre VI Energie libre – Enthalpie libre |
| Exemples d’enthalpies standard - Le Mans University |
| Fiche de présentation 25 - ac-versaillesfr |
Qu'est-ce que l'enthalpie standard de formation?
- Enthalpie standard de formation.
. Notée ?fH. o ; elle correspond à l’enthalpie standard de formation d’un corps composé par la réaction de formation de ce corps à partir des éléments pris dans leur état standard.
. Par convention, ?fH. o corps pur simple dans l’état standard = 0 J.mol-1 quelque soit T.