tp solubilité et produit de solubilité
|
Equilibre : Précipitation-Solubilité /Dr Maghchiche
Le produit de solubilité est une constante qui permet de : - Définir la quantité limitée de substance dissoute (solubilité) - Prévoir les conditions de |
|
POLYCOPIÉ DE TRAVAUX PRATIQUES CHIMIE 3
30 jan 2018 · 1/ Produit de solubilité : Considérons une solution saturée d'un électrolyte CmAn peu soluble en présence d'un excès de ce corps à l'état |
|
TP :SOLUBILITE DU CHLORURE DE SODIUM DANS LEAU
I Principe Le but de la manipulation est de trouver la solubilité et le produit de solubilité du chlorure de sodium dans l'eau à |
|
TP CHIMIE ANALYTIQUE
La solubilité d'un électrolyte est donc la quantité maximale exprimée en mole ou en gramme d'un soluté que l'on peut dissoudre dans un litre de solvant à une |
|
TRAVAUX PRATIQUES DE CHIMIE DES SOLUTIONS
TP N°5: SOLUBILITÉ Relation entre solubilité et produit de solubilité : Soit l'équilibre |
Quelle est la relation entre S et KS ?
mol−1.
La relation entre Ks et s est à redémontrer à chaque fois.
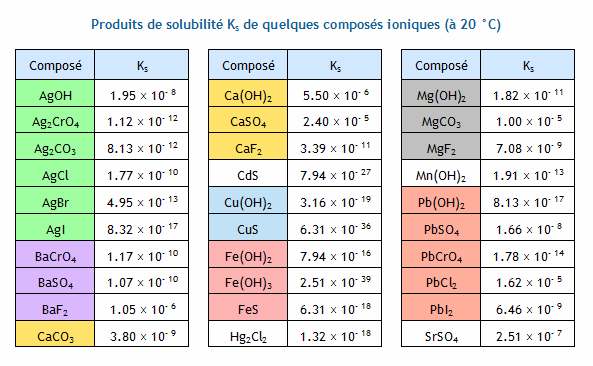
Ks(AgCl) > Ks(Ag2CrO4) mais s(AgCl) < s(Ag2CrO4) donc Ag2CrO4 est plus soluble que AgCl Conclusion : le plus soluble n'est pas toujours celui qui a le plus grand Ks car cela dépend de la stoechiométrie du solideComment calculer le produit de la solubilité ?
La formule est donc : �� s p + – = [ M ] [ A ] .
Ce type particulier de constante d'équilibre est différent des autres, où une certaine valeur des produits est habituellement divisée par une certaine valeur des réactifs.Quelle est la différence entre la dissolution et la solubilité ?
La solubilité est la capacité d'une substance, appelée soluté, à se dissoudre dans une autre substance, appelée solvant, pour former un mélange homogène appelé solution.
La dissolution est ce processus.- Kps est une mesure de la quantité de soluté dissous ou de la solubilité molaire d'un composé.
Plus une substance est soluble, plus sa valeur de Kps est élevée.
Donc, s'il y a une concentration relativement élevée de particules dissoutes dans la solution, Kps sera plus élevée.
|
POLYCOPIÉ DE TRAVAUX PRATIQUES CHIMIE 3
30 janv. 2018 Tp n° 04 : Dosage des ions hypochlorite dans une eau de Javel. 15. Tp n° 05 : solubilité et produit de solubilité. 17. Page 3. Hygiène et ... |
|
TP 03 : Solubilité - produit de solubilité
I-. GENERALITES. 1. La solubilisation : est la dissolution d'un solide ionique dans l'eau. En effet lorsqu'un solide ionique de type AnBm est dissout dans |
|
TRAVAUX PRATIQUES DE CHIMIE DES SOLUTIONS
TP N°5: SOLUBILITÉ Relation entre solubilité et produit de solubilité : Soit l'équilibre ... |
|
TP CHIMIE ANALYTIQUE - Dakar
A. ANALYSE QUANTITATIVE. (14 points). (durée : 02 heures). DETERMINATION D'UN PRODUIT DE SOLUBILITE. 1. Partie Théorique. 1.1. Introduction. |
|
Travaux pratiques
25 nov. 2020 . Déterminer la concentration en ions calcium dans la solution saturée en sulfate de calcium. En déduire le produit de solubilité Ks du sulfate ... |
|
Fiche 5 : Solubilité dune espèce chimique
À cette valeur mmax correspond une concentration maximale de soluté dans la solution c'est la solubilité notée s. Si la masse de soluté est supérieure à |
|
Introduction :
On calcule le produit de solubilité dans chaque cas. H2O+ Ca(OH)2 A partir de cette manipulation (TP) on peut déterminer le produit de solubilité d'un solide. |
|
CORRECTION TP :SOLUBILITE DU CHLORURE DE SODIUM
CORRECTION TP :SOLUBILITE DU CHLORURE DE SODIUM DANS L'EAU. III Dosage des ions chlorures par les ions argent. 1. mol.L-1. NaCl = Na+. + Cl-. E.I.. Excès. |
|
Ks du iodate de calcium et solubilité dans KI
4) Calculez le produit de solubilité du iodate de calcium. 5) Calculez la Préparation du TP. Préparation de Ca(I03)2. Dissoudre 56 g de KIO3 dans 300 ml d ... |
|
Ks BaIO3
DETERMINATION DU PRODUIT DE SOLUBILITE. DE L'IODATE DE BARYUM. Le but des dosages réalisés dans ce TP est de déterminer le produit de solubilité de l'iodate |
|
POLYCOPIÉ DE TRAVAUX PRATIQUES CHIMIE 3
Tp n° 02 : Étalonnage d'une solution acide (HCl) par une solution de carbonate de sodium Tp n° 05 : solubilité et produit de solubilité. |
|
TP n 6 Détermination du produit de solubilité du sulfate de calcium
Le but du TP est de déterminer la valeur de la constante de cet équilibre aussi appelée produit de solubilité de l'iodate de baryum et notée Ks. |
|
TP CHIMIE ANALYTIQUE
TP CHIMIE ANALYTIQUE DETERMINATION D'UN PRODUIT DE SOLUBILITE ... Ks produit de solubilité de Ca(OH)2 dépend de la température et du solvant. |
|
Chimie et développement durable Partie 1 / Synthèses chimiques
B : Le produit de solubilité. 1. Définition La solubilité du chlorure de calcium CaCl2(s) dans l'eau est s = 745 g/L. On verse 221 g de chlorure de ... |
|
CORRECTION TP :SOLUBILITE DU CHLORURE DE SODIUM
CORRECTION TP :SOLUBILITE DU CHLORURE DE SODIUM DANS L'EAU. III Dosage des ions chlorures par les ions argent. 1. mol.L-1. NaCl = Na+. + Cl-. E.I.. Excès. |
|
Précipitation et produit de solubilité
Précipitation et produit de solubilité. I - Produit de solubilité. Dans une solution saturée de chlorure d'argent AgCl solide coexiste avec AgCl dissous |
|
TRAVAUX PRATIQUES DE CHIMIE DES SOLUTIONS
TP N°6 : EFFET DE LA COMPLEXATION ET DE LA SOLUBILITE. A saturation la concentration des ions en solution est appelée solubilité |
|
TP n°9 Solubilité de lhydroxyde de calcium
L'objectif de ce TP est d'étudier une solution d'eau de chaux pour En déduire une relation entre le produit de solubilité KS de l'hydroxyde de calcium ... |
|
Introduction :
La solubilité d'un composé ionique ou moléculaire appelé soluté |
|
1) Principe 2) Détermination dun produit de solubilité (cf. annexe)
V est voltmètre électronique de très grande résistance interne. • (P) est un pont salin constitué d'une solution de nitrate de potassium contenue dans un. |
|
Chapitre Chapitre II: II: La La solubilité solubilité
Chapitre II: La solubilité 1 Aspect qualitatif de la solubilité: 1 1Notion de solubilité-saturation: Pour tout soluté mis en solution dans un volume défini de solvant il existe à une température donnée une limite de concentration au-delà de quelle le corps ne peut plus être dissous c’est la solubilité maximale |
|
Chapitre 1 Solubilité - ac-montpellierfr
Tle STL – SPCL Chimie et développement durable Fiche de synthèse – Chapitre 1 : Solubilité 1 Chapitre 1 Solubilité 1 Equilibres hétérogène 1 1 Produit de solubilité Certaines espèces neutres peuvent se révéler peu solubles en solution aqueuse un solide (précipité) peut alors apparaitre |
|
Searches related to tp solubilité et produit de solubilité PDF
TP pour tester les connaissances de l’étudiant(e) sur la préparation de la manipulation Les notes correspondantes seront comptabilisées avec celles des comptes rendus et du contrôle final L'attitude de l'étudiant lors des séances de TP sera prise en compte lors de la notation (ponctualité préparation préalable des TP ) |
Qu'est-ce que le produit de solubilité ?
Le produit de solubilité peut être défini comme le produit des concentrations des ions dans une solution saturée, chacune d’elles élevée à la puissance de leurs coefficients stœchiométriques respectifs. Lorsque le produit de solubilité est égal au produit de la concentration des ions, la solution est saturée.
Comment calculer la solubilité ?
Calculer la solubilité dans l'eau S0 :exprimer d'abord [Ca2+] et [OH-] littéralement, effectuer ensuite le calcul numérique de S0. Expliquer le calcul de la solubilité S1 dans la solution sodée F1 : calculer[OH-] apporté par la soude , [OH- ] présent dans le filtrat dosé, on en déduit la solubilité . Calculer Ks .
Comment calculer la solubilité du bromure d’argent ?
La valeur finale nous indique que 0,000137 g de bromure d’argent est dissous dans 1 dm3 ( 1???000 mL) d’eau à 298 K. Nous avons vu dans l’exemple ci-dessus que le produit de solubilité pour le bromure d’argent est 5, 3 5 × 1 0 ? ? ? mol2?dm?6.
Quels sont les facteurs qui influencent la solubilité du chlorure d’argent ?
La solubilité du chlorure d’argent AgCl(s) dans l’eau à 25°C et Patmosphérique est de 1,33x10-5 mol/L. 2.3. Facteurs influençant la solubilité Différents paramètres physiques ou chimiques vont influer directement la solubilité d’un soluté dans un solvant donné :
| Chapitre 1 Solubilité - ac-montpellierfr |
| Équilibres de solubilité - AlloSchool |
| SOLUBILITE / PRECIPITATION |
| LES REACTIONS DE PRECIPITATION 1 La solubilité |
| Équilibres de solubilité |
| Searches related to tp solubilité et produit de solubilité filetype:pdf |
|
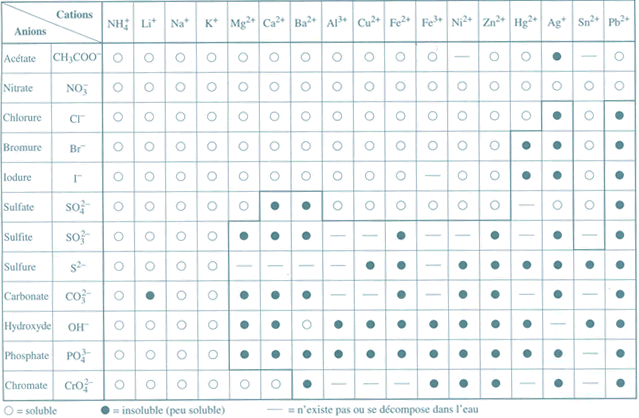
II- Solubilité et produit de solubilité 1- Définition
Le produit de solubilité (ou la constante de solubilité) noté « Ks » d'un solide ionique correspond à la constante d'équilibre de la réaction de dissolution de ce |
|
Précipitation - Produit de solubilité A – Introduction - Nicole Cortial
La solubilité s du chlorure d'argent est la quantité maximale de ce solide qui passe en solution Un litre de solution d'acide chlorhydrique de concentration 1 L |
|
Ks - univ-biskra
Calculer le produit de solubilité du chromate d'argent Ag=108; Cr=52; O=16 gmol -1 Ag2CrO4 solide en équilibre avec 2Ag+ + CrO4 2- masse molaire Ag2CrO4 : |
|
SOLUBILITE / PRECIPITATION
Tableau 1 : Produit de solubilité de quelques composés peu solubles Sel Expression de k SP Valeur de K Sp pK Sp AgCl K SP = [Ag+] [Cl-] 1,8 10-10 |
|
SOLUBILITE , PRODUIT DE SOLUBILITÉ ET SOLUBILITÉ DES
SOLUBILITE , PRODUIT DE SOLUBILITÉ ET SOLUBILITÉ DES SELS EN MILIEU COMPLEXANT Prérequis Kps est liée à la solubilité • Q < Kps : pas de |
|
Précipitation et produit de solubilité
Précipitation et solubilité 1/5 Précipitation et produit de solubilité I - Produit de solubilité Dans une solution saturée de chlorure d'argent, AgCl solide coexiste |
|
Semestre 2 – Chapitre 4 : Équilibres de solubilité La notion intuitive
1- Lorsqu'on dissout dans l'eau de l'hydroxyde de magnésium (II) Mg(OH)2 (s) jusqu'à saturation, la solution possède un pH égal à 10,5 Montrer que le produit de |
|
Transformations chimiques en solution aqueuse - Chimie en PCSI
On appelle produit de solubilité, noté Ks, la constante d'équilibre associée à l' équilibre entre le solide –le précipité-‐ et ses ions en solution aqueuse : Equilibre |
|
Produit de solubilité de la calcite et constantes de - Érudit
Produit de solubilité de la calcite et constantes de dissociation de CaHCO3+ et CaCO30 entre 5 et 75 °C Calcite solubility product and dissociation constants of |