Devoir physique Masse et Taille D'un Atome 2nd 2nde Physique
|
Correction du TD 1 Analyse dimensionelle et ordres de grandeurs
Considérez le système formé par un électron de charge qe et de masse me tournant autour d'un proton de charge qp et de masse mp On considère ce système |
|
Les grandeurs physiques et leurs unités (à connaître par cœur) Il ne
Taille Largeur Epaisseur Distance etc Une règle Le mètre (symbole : m) La masse volumique d'un liquide ou d'un solide ou d'un gaz (symbole : ρ) La |
Quelle est la formule de la masse d'un corps ?
Son intensité P se mesure avec un dynamomètre.
Le poids et la masse d'un objet sont deux grandeurs proportionnelles.
Cela s'écrit P = m × g où :▪ P est l'intensité du poids (en N) ;▪ m est la masse (en kg) ;▪ g est l'intensité de pesanteur (en N/kg).Quelle est la règle de la masse ?
On rappelle la formule liant la quantité de matière n à la masse m : m = n \\times M.
C'est quoi la masse d'un corps ?
La masse représente la quantité de matière d'une substance ou d'un objet.
Elle se mesure généralement en grammes (g). ( g ) .
Pour mesurer la masse d'une substance ou d'un objet, on utilise une balance.- Le poids est une force qui se mesure à l'aide d'un dynamomètre et est graduée en newton, alors que la masse représente une quantité de matière et se mesure avec une balance graduée en gramme ou dans une de ses sous-unités.
|
Seconde générale - Exercices - Devoirs - Physique et Maths
Le noyau d'un atome porte une charge électrique Q=96.10-19C et la masse de cet atome est m(X)=2 |
|
Problèmes de physique de concours corrigés – 1ère année de
et par seconde on déduit que le nombre de particules ? diffusées (par un seul atome diffuseur) par seconde d'un angle supérieur ou égal à ?1 est s/n)b(. |
|
CONTROLE n°1 : CHIMIE
2- Quel est le nombre de charges positives portés par le noyau de l'atome de fer ? 3- En déduire le numéro atomique de l'atome de fer. La masse d'un atome de |
|
CORRIGE
11 déc. 2015 DEVOIR COMMUN N° 2 PHYSIQUE-?CHIMIE ... nombre de masse alors la masse molaire de cet atome est : M = A.(12/12.N).N = A g.mol-?1. |
|
Corrigé
2) Combien un atome de titane possède-t-il d'électrons de valence ? Lesquels ? 8) Préparer le calcul qui permet de calculer la masse atomique du titane ... |
|
Programme de physique-chimie de seconde générale et
Programme de physique-chimie de seconde générale et technologique grandeur de taille et de masse de l'atome et du noyau et par le modèle du cortège. |
|
Fiche de révision de 3eme en physique chimie - DNB
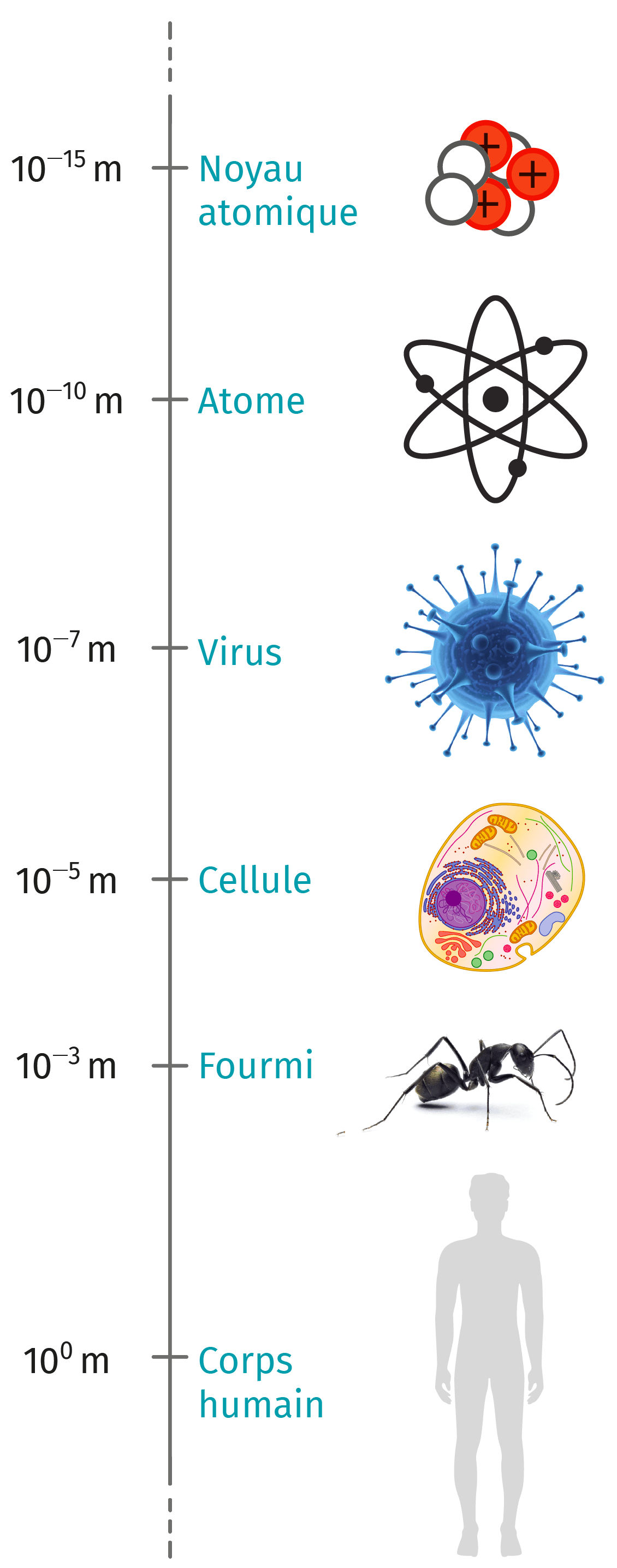
Description d'un atome : • Quasiment toute la masse est contenue dans le noyau. • La taille du noyau ? 10-15 m la taille de l'atome ? 10-10 m. |
|
Physique Statistique Exercices de Travaux Dirigés
= 2?2. mL2. (41). 13. Page 14. A.N. : Calculer ?0 (en J puis en eV) pour des atomes d'Hélium dans une bo?te de taille L = 1m. 2/ Atomes indiscernables.– Les |
|
Fiche de révision de 3eme en physique chimie - DNB
Description d'un atome : • Quasiment toute la masse est contenue dans le noyau. • La taille du noyau ? 10-15 m la taille de l'atome ? 10-10 m un noyau |
|
LES RÉACTIONS NUCLÉAIRES DANS LES ÉTOILES
2de Physique-Chimie • Constitution et transformation de la matière. DOSSIER 2 LES RÉACTIONS depuis stable de par sa taille et l'énergie qu'il délivre. |
| Exercice du chapitre 4 le noyau de latome - Plus de bonnes notes |
| EXERCICES - Physicus |
| Corrigé |
| CORRIGE |
| CONTROLE n°1 : CHIMIE |
| Exercices résolus de Chimie Physique - 3ème édition - ChercheInfo |
| Problèmes de physique de concours corrigés – 1ère année de |
| Physique des solides (MP 022) - LPTMC |
| Chapitre 1 - Léchelle des longueurs - Lycée dAdultes |
| PHQ434 : Mécanique quantique II - Département de physique |
| Troisième - Constitution des atomes - Exercices - Devoirs |
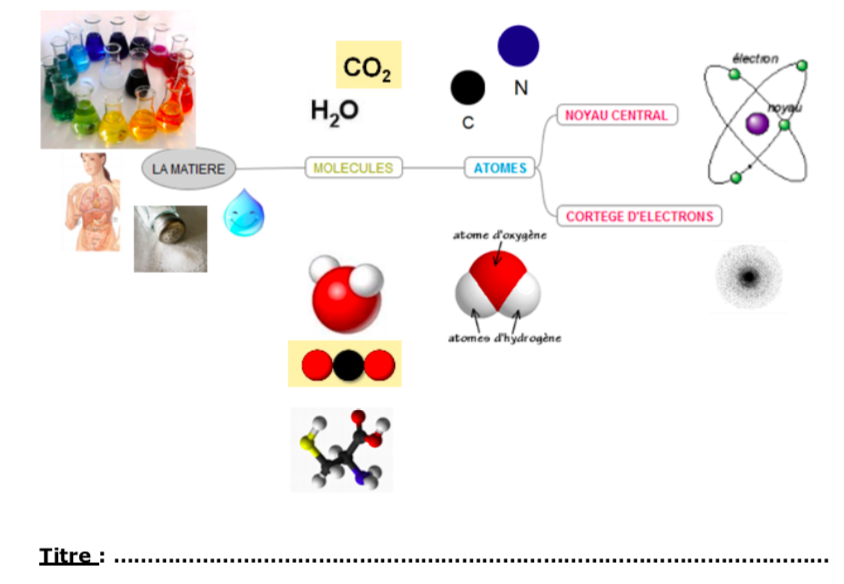
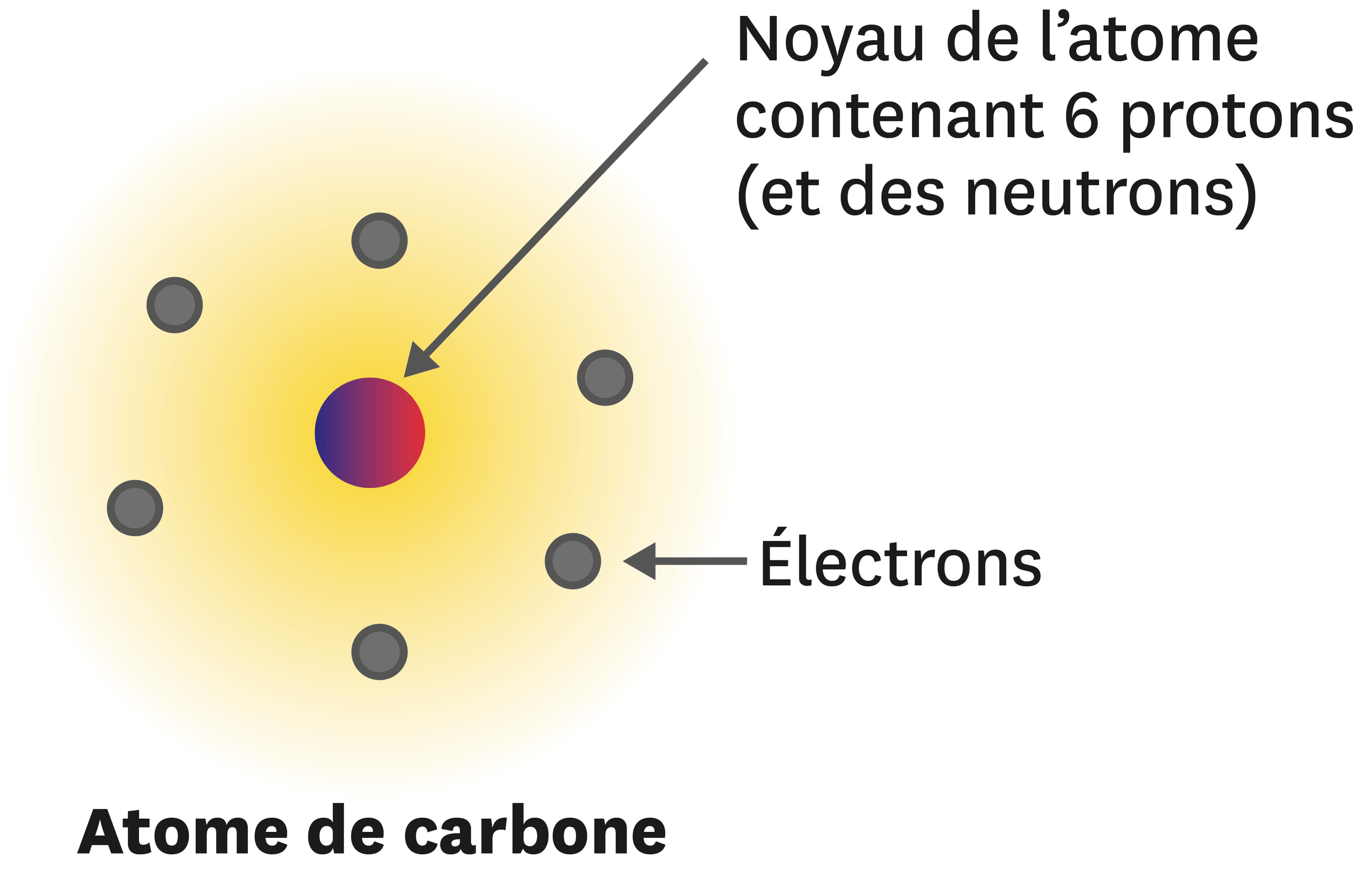
Forme et Limites d’un Atome
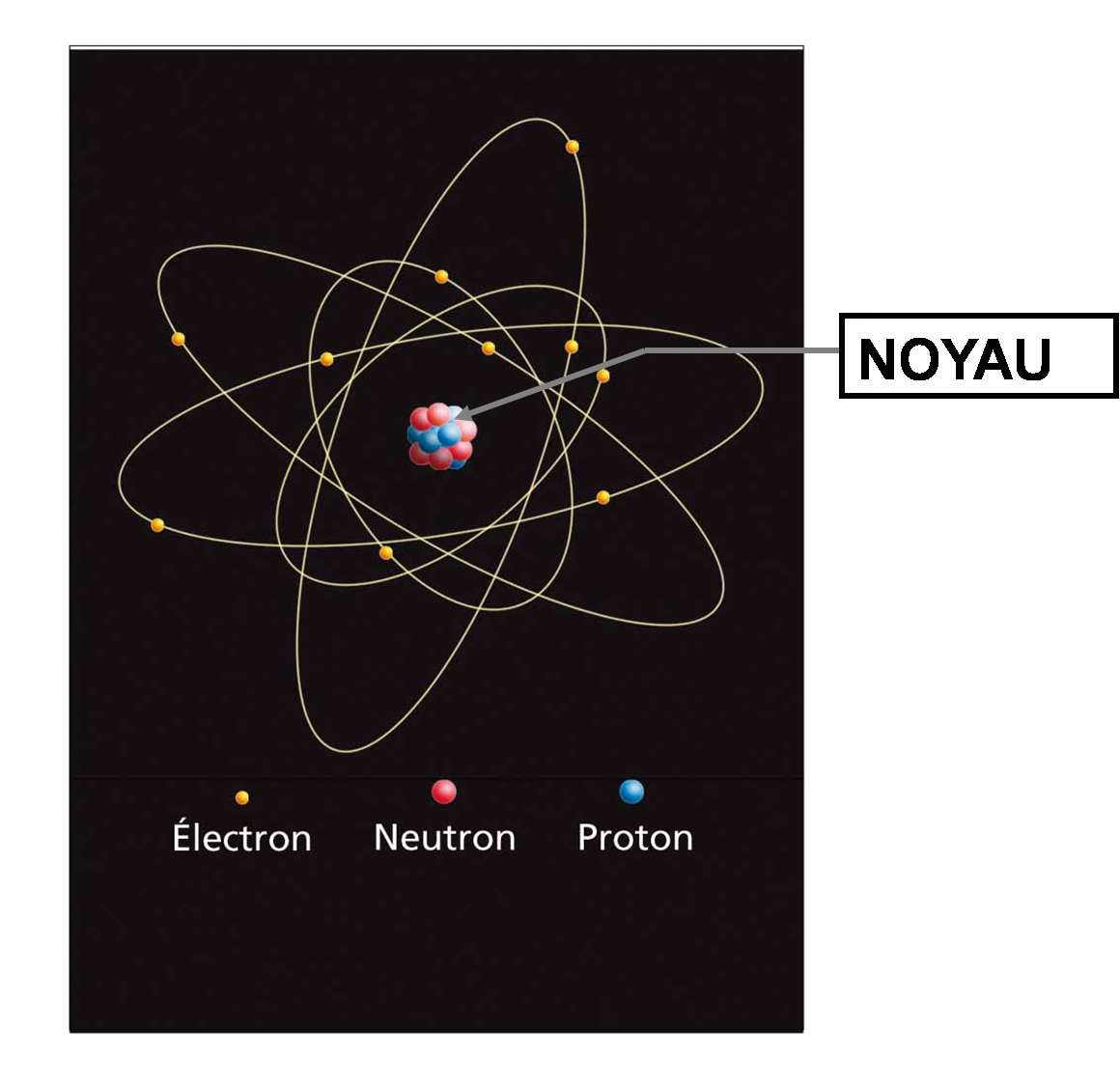
Un atome est constitué d’un noyau entouré d’un cortège d’électrons: 1. Le noyau est un agrégat de nucléons (protons et neutrons) que l’on peut considérer comme sphérique . 2. L’atome dans son ensemble peut lui aussi être modélisé par une sphère. La limite d’un atome correspond à la zone où évoluent les électrons les plus éloignés de son noyau: il s...
Ordre de Grandeur Du Noyau
Le plus petit noyau atomique est celui de l’hydrogène constitué d’un seul et unique proton dont le noyau a un diamètre de 1,68.10-15 m. L’uranium est un des plus lourd élément chimique stable, les noyaux de ses isotopes stable ont un diamètre de l’ordre de 2.10-14 m*1.
10-15 M
*1 Source: Livret thématique du CEA “L’atome” http://www.cea.fr/multimedia/Documents/publications/livrets-thematiques/livret-atome.pdf
Ordre de Grandeur de L’Atome
L’un des plus petit atomes est l’hydrogène, il a un diamètre de 0,5.10-10 m L’un des plus gros atome est l’actinide, son rayon de 2,9.10-10m
L’Atome Est donc Environ 100 000 Fois Plus Grand Que Son Noyau !
Sachant que la dimension des électrons est très faible (un électron est si petit qu’il est difficile de déterminer sa taille) on en déduit que la matière est très minoritaire et qu’un atome est essentiellement constitué de vide. Pour traduire cette caractéristique on dit que l’atome a une structure “lacunaire“.
Rayons Atomiques
Les tables de données fournissent en général le rayon des atomes et non leur diamètre. Ce dernier peut être déterminé de manière théorique (en se basant sur des modèles plus ou moins complexes) ou expérimentalement en considérant que le rayon atomique correspond à la moitié de la distance séparant les noyaux de deux atomes identiques liés par une l...
Petite Histoire de l'atome
Qu'est-ce qu'un atome ?
La Structure de l'atome
L'atome a une structure particulière, les scientifiques sont passés par différents stades avant d'arriver à décrire celle-ci. Le noyau d'un atome est constitué de protons et de neutrons, il est donc électriquement positif. Ce noyau est entouré d'électrons qui gravitent autour de celui-ci, la partie la plus extérieure de l'atome est donc électriquem...
Etude de La Masse d'un Atome à l'aide d'un Spectromètre de Masse
Le spectromètre de masse est un procédé d’analyse physico-chimique par mesure de la masse des éléments. Le spectromètre de masse a été mis au point par Joseph John Thomson. Il est composé d’une source d’ionisation qui permet de vaporiser les molécules et à les ioniser. Les ions sont ensuite séparés en fonction de leur rapport masse/charge (m/z) dan...
Comment calculer la taille et la masse d'un atome ?
. On obtient la masse de l'atome (m) en multipliant le nombre de nucléons (A) par la masse (m) d'un nucléon.
Comment comparer la taille et la masse d'un atome ?
. Si le noyau de l'atome d'hydrogène de symbole H avait un diamètre égal à 1 mm, l'atome aurait un diamètre égal à 1 × 100 000 = 100 000 mm = 100 m.
Comment calculer l'ordre de grandeur de la taille d'un atome ?
. Donc le rayon du noyau est 100 000 fois ou 105 fois plus petit que celui de l'atome.
. Exemple : Si le noyau était une orange de 3 cm de rayon, l'atome aurait un rayon de 3 kilomètres.
Comment calculer la taille et la masse d’un atome ?
- Comparer la taille et la masse d’un atome et de son noyau. L’atome possède une structure lacunaire, c’est-à-dire qu’il est essentiellement composé de vide. Les masses des neutrons et protons sont très supérieures à celle des électrons donc la masse de l’atome est concentrée dans son noyau : matome ≈ (A) × mp ≈ (A) × mn .
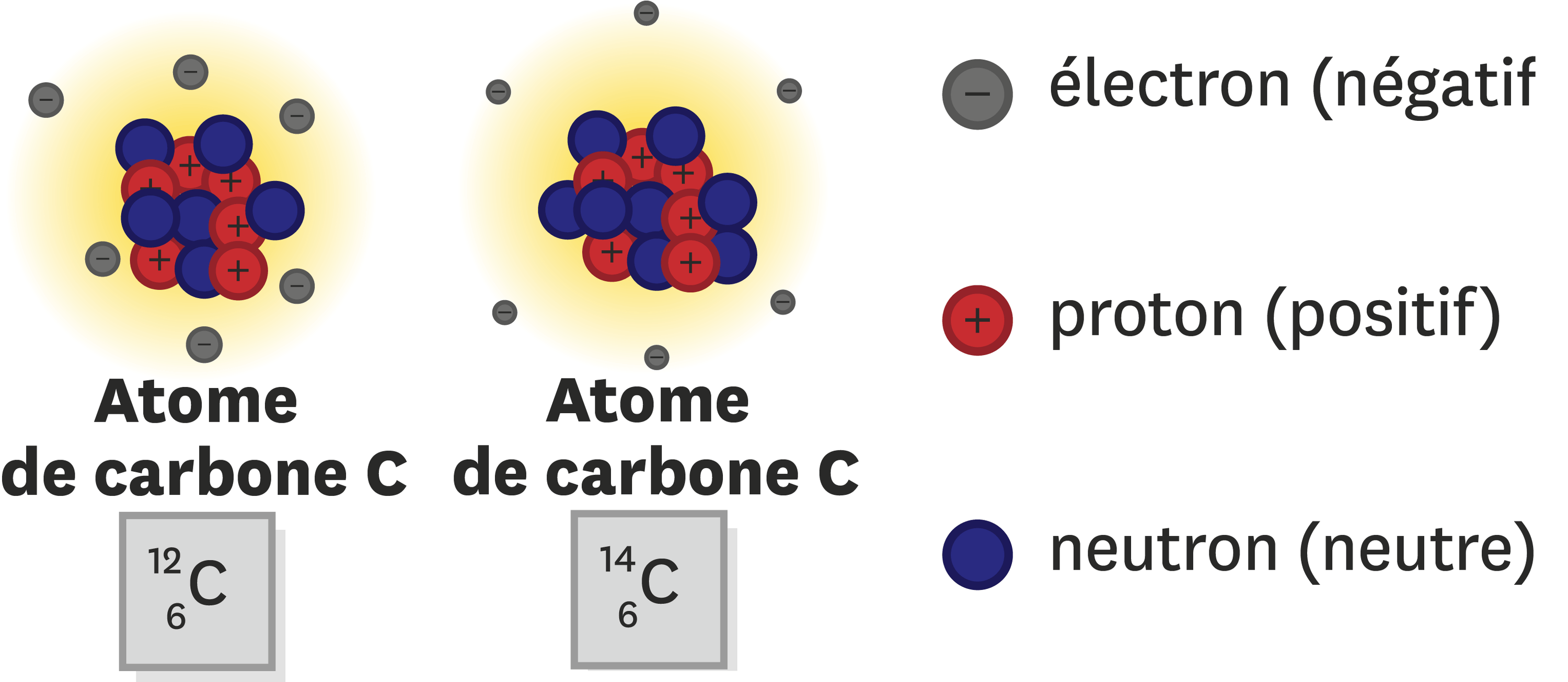
Comment calculer la masse d’un noyau d’atome ?
- La masse d’un noyau d’atome peut être calculée en additionnant la masse de tout ses composants: les neutrons et les protons. Le nombre de protons d’un noyau correspond au numéro atomique Z tandis que le nombre de neutrons correspond à la différence du nombre de masse et du numéro atomique (A-Z).
Qu'est-ce que la masse atomique relative?
- La masse atomique relative d'un élément est définie comme le rapport entre la masse moyenne d'un atome pour la composition isotopique naturelle sur le douzième de la masse d'un atome de carbone.
Comment calculer la masse d'un atome de fluor ?
- " Le fluor, de symbole chimique F, a pour numéro atomique Z=9. La masse d'un atome de fluor est m=3,17 * 10^-26 kg. 1. Rappeler la relation qui permet de calculer la masse d'un atome. 2. En déduire alors une expression permettant de calculer le nombre de masse A à partir de la masse de l'atome. 3.
|
CONTROLE n°1 : CHIMIE
2- L'électron d'un atome d'aluminium est différent de l'électron d'un atome de zinc 3- Un isolant La masse de tous les électrons de l'atome de fer est 2,366 x 10 -29 kg Pour faire le calcul tu dois donc convertir les 2,5 g en kg |
|
Atome et cortège électronique - Physique et Maths
Le noyau d'un atome de fer est représenté par : 26 masse de cet atome est m( X)=2,04 10-26kg a Calculer le rapport entre la taille de l'atome et du noyau |
|
DEVOIR SURVEILLE - SCIENCES PHYSIQUES - Free
2 Calculer la masse d'un atome de magnésium La masse d'un atome est tout simplement la somme des masses sciences physiques et chimiques - Seconde |
|
Seconde 10 – Sciences physiques - Lycée Louis Pasteur – Lille - ENT
Lister les connaissances, savoir-faire théoriques et capacités expérimentales 2 Calculer la masse de ce noyau 3 Calculer la masse d'un atome de carbone Quelle doit être la taille de l'objet représentant le noyau s'il choisit un ballon de |
|
EXERCICES - Physicus
2e Physique chimie CHAPITRE 2 2 L'atome Exercice 1 Exercice 2 Exercice 3 Exercice 4 Exercice 5 charges négatives faut-il ajouter pour avoir masse de 3 00×10−26 kg, la masse totale Quelle serait la taille du noyau de l'atome |
|
Seconde CONTROLE N°2 ( 1h)
1) Déterminer la structure électronique des atomes de 2) En déduire combien d'atomes de chlore sont liés à l' 2) Quel est son nombre de masse A ? autant de liaison que d'électrons manquant sur la couche externe pour avoir une |
|
Correction du DS 3 de seconde - Physique Chimie - Free
2nde CORRECTION Physique - Chimie Devoir 3 EXERCICE I 1 C'est la 2 Le noyau de l'atome d'étain contient 50 protons chargés positivement et 70 neutrons électriquement neutres La masse d'un atome est concentrée dans son noyau, un électron étant 2000 fois moins Ce résultat est cohérent avec la taille |
|
Classe de seconde Nom et prénom : Devoir
Devoir de Sciences Physiques n°1 2 Calculer la masse volumique de l'espèce chimique solide étudiée dans cet exercice (0,5) 3 A : Taille d'un atome |