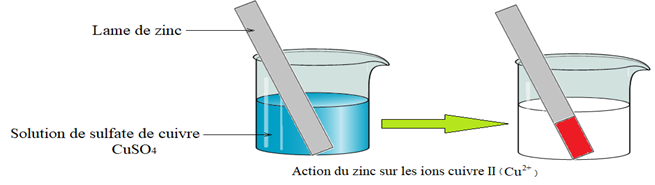
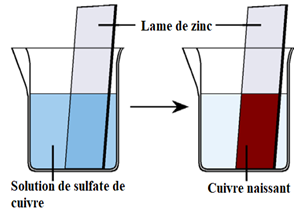
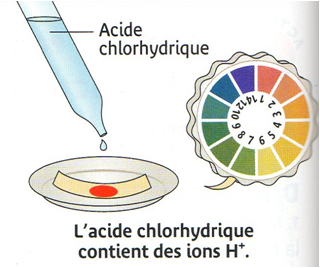
Devoir sur la réaction nitrate d'argent + cuivre 1ère Physique
|
BACCALAURÉAT GÉNÉRAL PHYSIQUE-CHIMIE
Chez les enfants les ions nitrite en excès provoquent une moindre capacité des globules rouges à fixer et transporter l'oxygène C'est pourquoi la |
|
Devoir Surveillé n° 1
13 oct 2016 · nitrate de plomb ( Pb2+ + 2 NO3 - ) de concentration CA = 20 10-2 mol 7) Calculer le temps de demi-réaction de la réaction Noté t1/2 c |
|
DEVOIR SURVEILLE N°3
9 déc 2016 · Les ions nitrate (NO ) sont spectateurs lors de cette réaction car ils n'interviennent pas lors de la réaction 3) Calculer les quantités de |
|
Exercices sur la réaction chimique NII
Exercice N°1 : Au cours de la réaction suivante : CO2 à C + O2 précisez s'il y a : - Conservation des éléments - Conservation du nombre de molécules - |
|
Matière Physique-Chimie Devoir: N° 3 Semestre
➢ Solution de nitrate d'argent : ➢ Solution de sulfate de fer Écrivez l'équation de cette réaction de précipitation |
|
Seconde générale
La réaction chimique est-elle exothermique ou endothermique ? Exercice 3 corrigé disponible Equilibrer les équations bilans ci-dessous : Exercice 4 corrigé |
Quels sont les différents types de réactions ?
Une réaction peut dégager de l'énergie (en général sous forme de chaleur, mais aussi de la lumière), elle est alors une réaction exothermique.
Elle peut nécessiter un apport d'énergie, sous forme de chaleur (donc « produire du froid ») ou de lumière, elle est alors une réaction endothermique.Quelles sont les caractéristiques d'une réaction ?
L'équation de la réaction chimique s'écrit, en toutes lettres, de la manière suivante : carbone + dioxygène → dioxyde de carbone.
On peut aussi écrire cette équation de la réaction chimique avec les formules chimiques des réactifs et des produits.
Dans le cas du carbone, la formule chimique est C.Quel est l équation de la réaction ?
Un produit de réaction est une substance résultant d'une réaction chimique.
Les produits de réaction de la combustion du méthane sont le dioxyde de carbone et l'eau.
Par exemple, lors de la combustion d'un composé comme le glucose (un sucre de formule C6H12O6), selon la réaction : C6H12O6 + 6 O2.
|
Physique-chimie RÉALISER LE BILAN DE MATIÈRE DUNE
transformation chimique par une réaction chimique ». différentes transformations entre le cuivre et une solution aqueuse de nitrate d'argent ont été. |
|
Corrigé DS no 2 : Avancement dune réaction chimique
5 oct. 2019 1ère spécialité Physique-Chimie - Lycée d'adultes - Poisson Florian ... on verse un volume V = 50 mL de solution de nitrate d'argent (Ag. |
|
Quand le nitrate dargent rencontre le cuivre_macro.pdf
Une solution de nitrate d'argent 01 M. EXPLOITATION PÉDAGOGIQUE. Dans cette expérience |
|
Physique-chimie MODÉLISER AU NIVEAU MACROSCOPIQUE
Physique-chimie. 2de 1re. Modélisation d'une transformation mettant en jeu du cuivre solide et une solution aqueuse de nitrate d'argent. |
|
Première Spécialité Activité Expérimentale : Les réactions d
1. Les ions cuivre Cu2+ les ions fer II Fe2+ et les ions argent Ag+ sont des oxydants et les métaux cuivre. Cu |
|
TP 7
Chimie Spé 1ère. TP 3.1 Les couples Ox/Red et les réactions d'oxydoréduction. I/ Réaction entre le cuivre et une solution de nitrate d'argent :. |
|
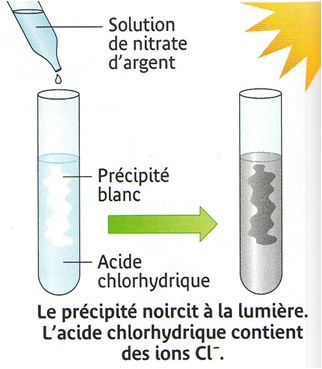
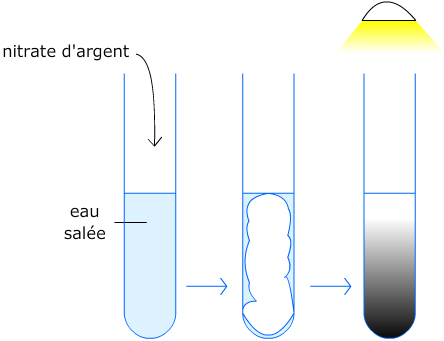
Chapitre CHIMIE – Comment identifier les IONS présents dans une
II – Test d'identification des ions par réaction de précipitation je vais verser quelques gouttes de nitrate d'argent pour identifier l'ion négatif et ... |
|
Nom : Durée : 2h00 Prénom : Classe : DEVOIR SURVEILLE n°8 de
DEVOIR SURVEILLE n°8 de PHYSIQUE-CHIMIE Exercice n°4 Etude de la pile cuivre-argent ... cuivre est bleue celle de nitrate d'argent incolore. |
|
Exercices de physique-chimie Première Spécialité
Pour ce faire on place un fil de cuivre dans un bécher contenant une solution de nitrate d'argent. On réalise l?expérience |
|
DEVOIR DE VACANCES – SPÉCIALITÉ PHYSIQUE-CHIMIE
- déterminer le rendement d'une synthèse organique. Exercice 1 : On immerge un fil de cuivre Cu(s) dans une solution de nitrate d'argent (Ag+(aq) ; NO3. |
| Chap 4 Tests de reconnaissance de quelques ions |
| Comment identifier les IONS présents dans une solution |
| Série des exercices sur les réactions doxydo-réduction 1BIOF |
| Cours et exercices de chimie des solutions - Elearning-ESGEE |
| Devoir Maison n°7 - Chimie en PCSI |
| Corrigé des exercices |
| Exercices doxydoréduction ( ) ( ) - Jean-Marc Drocourt |
| Oxydoréduction - Étienne Thibierge |
| Chapitre 5 - EXERCICES |
| Chimie XPLOITATION P - UCLouvain |
| Série d’exercices : réactions d’oxydo-réduction pr |
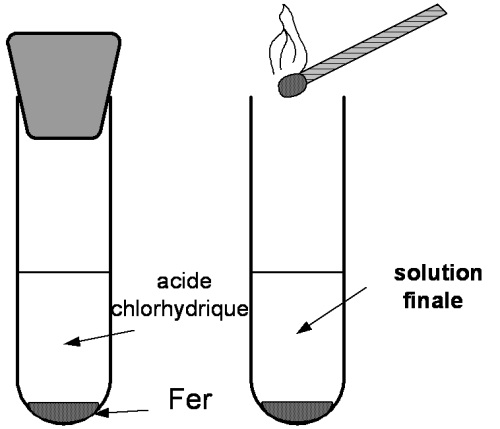
| I) ACTION DE L’ACIDE CHLORHYDRIQUE SUR LES METAUX - AlloSchool |
Comment calculer le nitrate de cuivre ?
- On ajoute V 2 = 20 mL de solution de nitrate de cuivre (Cu2+(aq) ; 2 NO3−(aq)) de concentration c2 = 5,0×10−2 mol⋅L -1 . On obtient une solution dans laquelle coexistent les ions argent Ag+(aq), cuivre Cu2+(aq) et nitrate NO3−(aq) .
Comment calculer le quotient de réaction entre le métal cuivre et l'ion argent ?
- 2. Écrire l'équation de réaction entre le métal cuivre Cu (s) et l'ion argent Ag+(aq) . 3. Exprimer le quotient de réaction Qr correspondant à la réaction précédente. 4. Calculer la valeur notée Qr,i du quotient de réaction à l'état initial du système.
Qu'est-ce que la réaction de l'argent ?
- L’argent se dépose autour du fil de cuivre et la solution devient bleue caractéristique de la présence d'ion Cu 2+. L’équation de la réaction qui se produit est : Cu
Comment calculer les ions argent et cuivre ?
- On obtient une solution dans laquelle coexistent les ions argent Ag+(aq), cuivre Cu2+(aq) et nitrate NO3−(aq) . 1. Calculer les concentrations initiales en ion cuivre Cu2+(aq) et en ion argent Ag+(aq) dans le mélange. On plonge ensuite dans le bécher un fil de cuivre Cu (s) et un fil d'argent Ag (s) bien décapés.
|
Chap2 Tests de reconnaissance de quelques ions
Ion cuivre II : Cu 2+ b ion fer II : Fe 2+ c ion fer III : Fe 3+ 17p62 : 1 Elle peut identifier les ions chlorure et les ions fer II ou fer III 2 Elle utilise le nitrate d' argent |
|
Réactions chimiques dangereuses - INRS
Un flacon de nitrate d'argent débouché ayant séjourné dans un laboratoire explosion due à l'acétylure de cuivre formé au contact de Dans l'action de l' acide nitrique sur les métaux, il se forme réaction initiée, elle se poursuit même après avoir coupé la Celle-ci semble jouer un rôle purement physique en favorisant |
|
Chap 4 Tests de reconnaissance de quelques ions
Ion cuivre Cu2+ Ion fer II Fe2+ Ion fer III Fe3+ Ion sodium Na+ Ion argent Ag+ Ion sulfate SO4 2- Ion hydroxyde OH- Ion chlorure Cl- Ion nitrate NO3 |
|
Physique-chimie - Ministère de lÉducation nationale
Action de l'eau, des acides et du dioxygène sur les métaux Une solution de nitrate d'argent à 0,1 mol/L Un fil de cuivre nettoyé et un fil de fer nettoyé selon les mots d'Arik Levy, se nourrit d'art et de design, dans un aller-retour incessant |
|
Oxydation du cuivre par lacide nitrique Corrigé - Transformations
Soit la réaction d'oxydation du métal cuivre par une solution aqueuse d'acide nitrique H3O+, NO3 dissous, une concentration en ions nitrate de [NO3 La constante K° a une valeur très grande : on peut dire que la transformation sera |
|
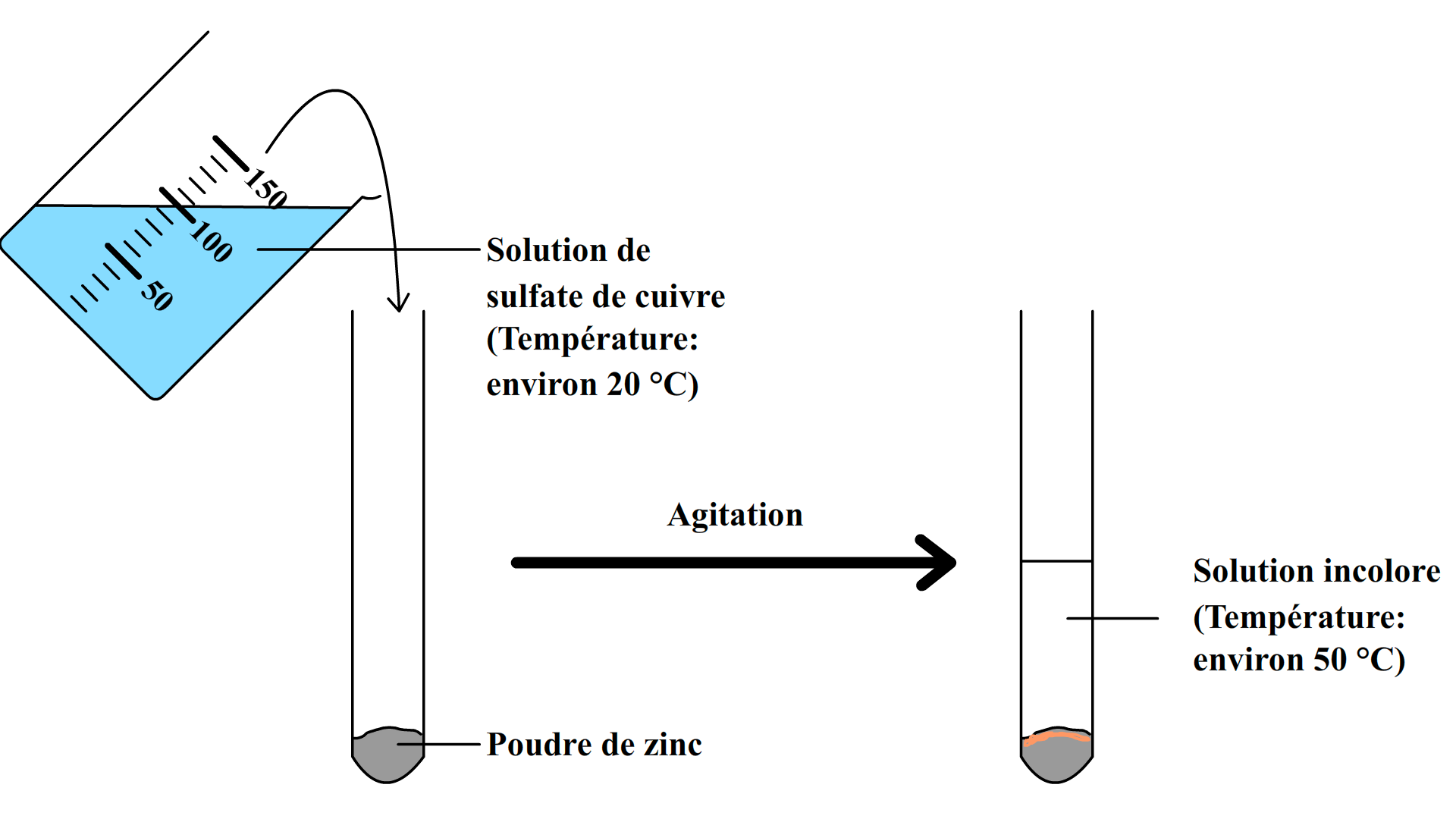
Chapitre 6 : Les réactions doxydoréduction - Physagreg
(on peut faire un témoin avec une solution de sulfate de zinc) 3) Autre exemple : réaction entre le métal cuivre et les ions argent : ➢ Expérience : Dans un erlenmeyer, on verse du nitrate d'argent et on ajoute de la tournure de cuivre |
|
CORRECTION DU TP N°6 - Physagreg
La solution se colore en bleu (Int : il se forme des ions cuivre (II) Cu2+) • Un gaz roux de cuivre) c La déshydratation est l'action d'enlever à un corps tout ou une partie de son eau d anion O2- pour avoir sa formule : il s'agit de CuO e |
|
Fiche de révision de 3eme en physique chimie - DNB
Pour identifier des ions, on peut utiliser des réactifs (soude, nitrate d'argent) qui vont donner Réaction entre de l'acide chlorhydrique et l'or / argent / cuivre : RIEN (inter)action gravitationnelle : exercée sur les objets qui ont une masse L'Univers est par définition, tout ce qui existe, c'est-à-dire la matière et l'énergie |
|
II Conseils pour la résolution dun exercice de Sciences physiques
Chapitre 3 : Les transformations chimiques du cuivre et de l'ion cuivre Chapitre 4 Si un solide est en équilibre sous l'action de deux forces 1 ⃗⃗⃗ et 2 a) Faire le schéma du montage électrique qui doit être réalisé (Annoter ce 2) L'électrolyte à utiliser est la solution de nitrate d'argent car elle contient des |