exercice pile électrochimique
|
Exercice 1 (6 points) La fabrication du verre
Exercice 2 (7 points) Piles électrochimiques Une pile électrochimique convertit l'énergie chimique en énergie électrique Différents types de métaux |
|
Exercices de la séquence n°4
De façon générale le fonctionnement électrochimique d'une cellule EXERCICE 5 : choix d'une pile pour alimenter une ampoule On dispose d'une petite ampoule |
|
Thème : Piles et électrolyses Fiche 4
6) Déterminer le sens du courant électrique et le sens de déplacement des porteurs de charge dans la pile et hors de la pile ▻ Exercice n°2 On réalise une |
|
TS2 Piles électrochimiques Exercice n°1 On réalise une pile
On considère une pile cuivre-argent réalisée à partir de deux lames de masse m = 1000 g Les solutions aqueuses de nitrate d'argent et de sulfate de cuivre |
Comment faire une pile électrochimique ?
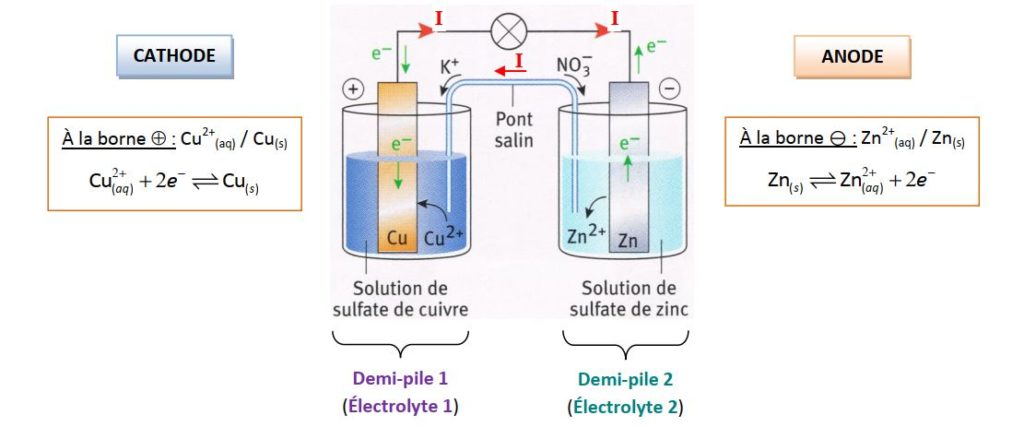
Pour fabriquer une pile électrochimique, il suffit d'immerger deux métaux différents dans des électrolytes contenant leurs propres ions Mn+ , et relier ces deux électrolytes par un pont salin.
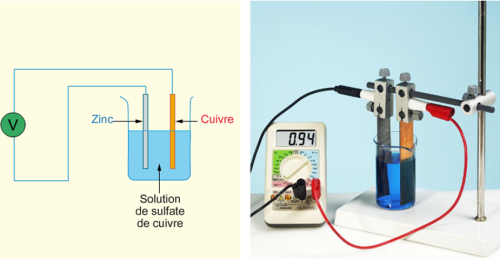
Quel est le schéma d'une pile ?
Le courant électrique circule en sens inverse des électrons, c'est-à-dire du pôle (+) (cathode) vers le pôle (–) (anode).
L'écriture symbolique d'une pile est : (–) Réd1/Ox1//Ox2/Réd2 (+).C'est quoi une pile électrochimique ?
Une pile électrochimique est le siège d'une réaction d'oxydoréduction spontanée (c'est à dire naturelle) entre deux couples redox.
Elle permet la conversion de l'énergie chimique en une autre forme d'énergie.- Déterminer la polarité de la pile
On détermine, à partir des sens dans lesquels se déroulent les demi-équations électroniques, la polarité de la pile sachant que : Le pôle négatif est celui qui libère les électrons.
Le pôle positif est celui qui capte les électrons.
|
Exercices de révision- Oxydo-réduction et Piles électrochimiques
Exercice I. On considère la pile symbolisée par: Cu / Cu2+ (01M) // Fe2+ (0 |
|
Thème : Piles et électrolyses Fiche 4 : Piles et électrolyses
Fiche 4 : Piles et électrolyses. ? Exercice n°1 5) Dans une pile l'anode s'enrichit en électrons |
|
Electrochimie Exercice n° 1 :
On réalise la pile Daniell en utilisant : - un bécher renfermant 100cm3 Exercice n° 2 : ... 1) Préciser les réactions électrochimiques mises en jeu. |
|
TS2 Piles électrochimiques Exercice n°1 On réalise une pile
Piles électrochimiques. Exercice n°1. On réalise une pile cadmium-argent contenant les couples oxydant/réducteur suivants : Ag+. (aq)/Ag(s). |
|
Exercice 1 (6 points) La fabrication du verre Exercice 2 (7 points
Exercice 2 (7 points). Piles électrochimiques. Une pile électrochimique convertit l'énergie chimique en énergie électrique. Différents types de métaux. |
|
Sentraîner : Piles et oxydoréduction Exercice : Laccumulateur au
Exercice : L'accumulateur au plomb et le démarrage automobile. La batterie d'une voiture est un accumulateur au plomb siège d'une transformation chimique |
|
Chimie et développement durable Partie 1
Les piles électrochimiques Exercice 1. Pour chacune des piles suivantes : Pile 1 : pile constituée d'une électrode de cuivre Cu plongée dans une ... |
|
Premier exercice
Premier exercice (6 points). Construction d'une pile électrochimique. Se référer aux demi- piles (I) (II) et (III) données ci-dessous pour répondre aux |
|
??????? ???? ??? ???? ??????? ???????? ??????? ??????
Deuxième exercice (7 points). Anode ou cathode ! Pour savoir si un métal est l'anode ou la cathode d'une pile électrochimique on compare sa tendance à. |
|
Exercices de la séquence n°4 - Piles
Exercices de la séquence n°4. Piles. EXERCICE 1 : vrai ou faux ? en nombre suffisant pour assurer la production électrochimique d'électricité. |
|
Série d’exercices Piles électrochimiques Exercice n°1/
Exercice n°4/ Pile à combustible (Session normale 2010 PC ) La pile à combustible est formée de deux parties séparées par un électrolyte qui joue le rôle du pont salin et deux électrodes A et B (figure) La pile au cours de son fonctionnement consomme le dioxygène et du méthanol liquide Données : |
|
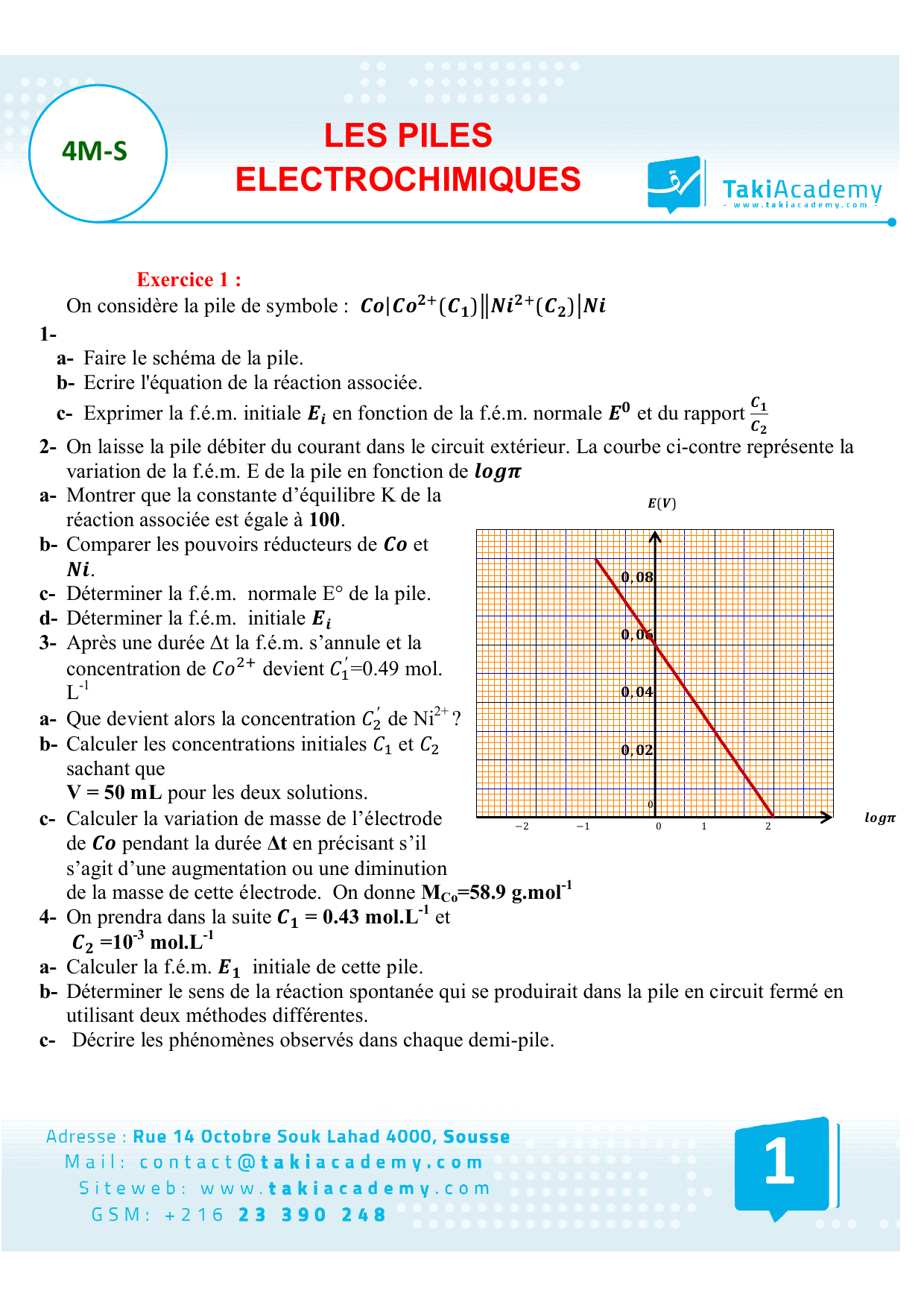
Série n°1 de chimie Thème : piles électrochimiques Exercice n
Exercice n°3 : On considère la pile électrochimique de symbole : Fe/ Fe2+ (C 1)?Cd2+ (C 2)/Cd 1) Faire le schéma de la pile et écrire l’équation associée à cette pile 2) Donner l’expression de la fem de la pile en fonction de sa fem normale E° C 1 et C 2 3) En maintenant C 2 = 01 mol L-1 on fait varier C 1 |
|
Professeur Piles électrochimiques
Exercice nol A la température 250C on réallse une pile électrochimique mettant en jeu les deux courbes Ni2+/ Ni et Zn2+/ Zn L' equation chimique associée à la pile est la suivante Zn + Ni2 Zn + Zn (Sd) Les solutions contenues dans les deux compartiments de la pile ont la même concentration molaire et le même volume |
Comment fonctionnent les piles électrochimiques ?
Série d'exercices :Transformations spontanées et production d'énergie dans les piles - étude des piles électrochimiques. Le fonctionnement des piles est basé sur la conversion d'une partie de l'énergie chimique en énergie électrique. Cet exercice se propose d'étudier le principe de fonctionnement de la pile aluminium-zinc.
Comment calculer la réaction chimique d’une pile ?
Ecrire l’équation chimique associée à cette pile. Faire un schéma de la pile sur lequel on précisera le sens du courant électrique et celui du mouvement des électrons dans le circuit extérieur. Calculer la constante d’équilibre K relative à l’équation de la réaction chimique associée à cette pile.
Comment calculer la polarité D’une pile ?
Préciser la polarité de la pile. Ecrire les équations aux électrodes ainsi que l’équation bilan lors du fonctionnement de la pile. Déterminer la concentration effective des ions Zn 2+ après une durée ?t=30min de fonctionnement. Exercice corrigé 2 : Etude de la pile Argent-Chrome.
Comment calculer la pile ?
On considère la pile symbolisée par : Cu ? Cu 2+ (1mol.L-1) ?? Fe2+(1mol.L-1) ? Fe Ecrire l’équation chimique associée à cette pile. Faire un schéma de la pile sur lequel on précisera le sens du courant électrique et celui du mouvement des électrons dans le circuit extérieur.
|
TS2 Piles électrochimiques Exercice n°1 On réalise une pile
Piles électrochimiques Exercice n°1 On réalise une pile cadmium-argent contenant les couples oxydant/réducteur suivants : Ag+ (aq)/Ag(s) et Cd2+ (aq)/ Cd(s) |
|
Piles et électrolyses - Studyrama
Dans la pile, les cations circulent de la demi pile à l'aluminium vers la demi pile au nickel et les anions en sens inverse ▻ Exercice n°2 1) Les électrons circulent |
|
TD électrochimie
Electrochimie Exercice n° 1 : On réalise la pile Daniell en utilisant : - un bécher renfermant 100cm3 d'une solution molaire de sulfate de cuivre dans laquelle |
|
EXERCICE DE REMÉDIATION - CHIMIE - 3 3C3D1I13CH14
Une pile électrochimique est un générateur qui transforme une partie de l' énergie chimique (provenant d'une réaction chimique) en énergie électrique Les piles |
|
Exercice exsm14_03
1 - Quel type d'électrodes (ou demi-piles) sont en présence ? Donner l' expression du potentiel dans chaque cas La demi-pile (A) est du type métal-ion, son |
|
Corrigé de lexamen du 20 juin 2007 2 heures
20 jui 2007 · Exercice I: oxydo-réduction et précipitation I Oxydo-réduction On se propose d' étudier une pile électrochimique dont la représentation est |
|
Piles et oxydoréduction Exercice - Lycée Ismael Dauphin
Exercice : L'accumulateur au plomb et le démarrage automobile La batterie d' une voiture est un accumulateur au plomb, siège d'une transformation chimique, |
|
EXERCICES SUR “LES PILES ÉLECTROCHIMIQUES”
EXERCICES SUR “LES PILES ÉLECTROCHIMIQUES” EXERCICE 1: Atomes de fer et ions cuivre(II) Début de l'expérience Après quelques heures |