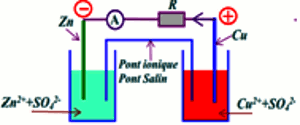
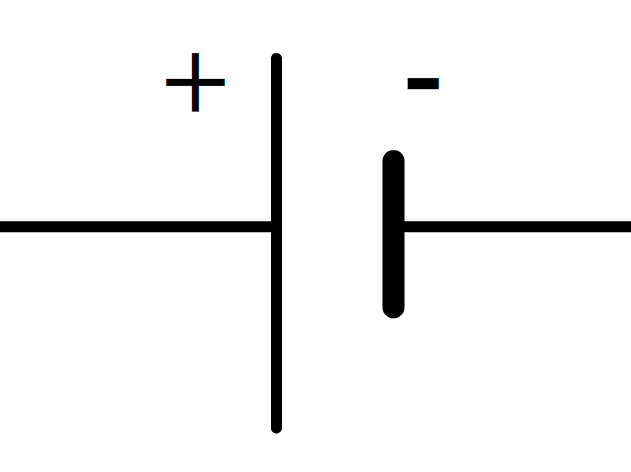représentation conventionnelle pile
|
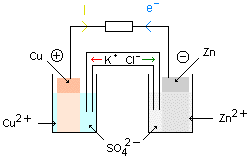
B) Fonctionnement de la pile Daniell : c) Réaction aux électrodes: d
le pont ionique vers la solution de sulfate de zinc et les ions K+ vers la solution de sulfate de cuivre). e) Représentation conventionnelle de la pile: |
|
Rés chim P3C2 (pile)
La cathode est donc l'électrode +de la pile. Page 2. Schéma conventionnel d'une pile : Soit la pile Daniell : couples |
|
étude dune pile à combustible au méthanol
C'est donc le pôle positif de la pile. 3). Représentation conventionnelle : solution aqueuse solution aqueuse. Pt. CO%(g). |
|
Les piles dispositifs mettant en jeu des transformations spontanées
s'agit de la borne ? de la pile. ? Des électrons sont captés par la solution ionique d'ions cuivre II selon la demi-équation électronique : Cu. |
| Thème : Piles et électrolyses Fiche 4 : Piles et électrolyses |
|
5_Sol aqueuses_pc_exercices
On constitue une pile en solution aqueuse dans laquelle le méthanol liquide est dissous dans Donner une représentation conventionnelle de cette pile. |
|
Www.AdrarPhysic.Fr
le pont ionique vers la solution de sulfate de zinc et les ions K+ vers la solution de sulfate de cuivre). e) Représentation conventionnelle de la pile:. |
|
Chap8 les piles
Détermination expérimentale des caractéristiques d'une pile (expérience 3). 2.3. Autres piles (expérience 4). 2.4. Représentation conventionnelle d'une pile |
|
PROF :Zakaryae Chriki Matière: chimie Résumé N:7 Niveaux: SM
Une pile électrochimique est un générateur qui transforme de l'énergie chimique en énergie électrique. Représentation conventionnelle de la pile. |
|
Page de garde Science pour rapport
LES PILES ET EVOLUTION D'UN SYSTEME. PC. C. H. I. M. I. E. Les piles et évolution d'un système 2-3/ Représentation conventionnelle de la pile :. |
|
C) Réaction aux électrodes: d) Rôle du pont salin - AlloSchool
On représente symboliquement la pile Daniell par la représentation conventionnelle suivante: 2) Généralisation : On peut réaliser des piles identiques à la pile |
|
Les piles dispositifs mettant en jeu des transformations spontanées
Une pile électrochimique est un générateur qui transforme de l'énergie chimique fournie par une réaction d'oxydoréduction spontanée en énergie électrique |
|
Thème : Piles et électrolyses Fiche 4 - Studyrama
Pile : ensemble de deux demi piles reliées par un pont électrolytique qui assure la neutralité électrique de chaque solution et la circulation de l'électricité |
|
Les piles - physique chimie terminale S
Ecrire le schéma conventionnel de cette pile 5 On branche un voltmètre aux bornes de la pile ; il affiche U = - 11V Dessiner le avec ses bornes sur le |
|
2019_20_CCF_17 Piles électrolyse_2
Donner la représentation formelle de la pile Daniell 3 Faire le schéma d'une pile Daniell où le pont salin Donner le schéma conventionnel de la pile |
|
Oxydo-réduction et Piles électrochimiques SMPC2 fsr 2015
On considère la pile symbolisée par: Cu / Cu2+ (01M) // Fe2+ (01 M) /Fe 1) Calculer le potentiel de chaque électrode 2) Indiquer l'anode la cathode et |
|
Cours-pc-2bac-sp-international-fr-27-1pdf - Moutamadrisma
On représente symboliquement la pile Daniell par la représentation conventionnelle suivante: 2) Généralisation : On peut réaliser des piles identiques à la pile |
|
Zakaryae Chriki Matière: chimie Résumé N:7 Niveaux: SM PC SVT
Représentation conventionnelle de la pile (-) Zn/Zn2+ Cu2+/Cu (+) Zn(s) ? Zn 2+(aq)2e? Cu2+(aq)+2e? ? Cu(s) Cu2+(aq)+Zn(s) ? Cu(s)+Zn2+(aq) |
|
Chapitre-7-ETUDE-DE-LA-PILE-DANIELLpdf - Matheleve
Dans cette représentation le trait vertical symbolise une séparation entre deux phases et le double trait symbolise la jonction (le pont salin ou la paroi |
|
Chap8 les piles - LycOrsayPhy
Représentation conventionnelle d'une pile 2 5 Evolution spontanée d'une pile 3 Quantité d'électricité fournie 3 1 Définitions |
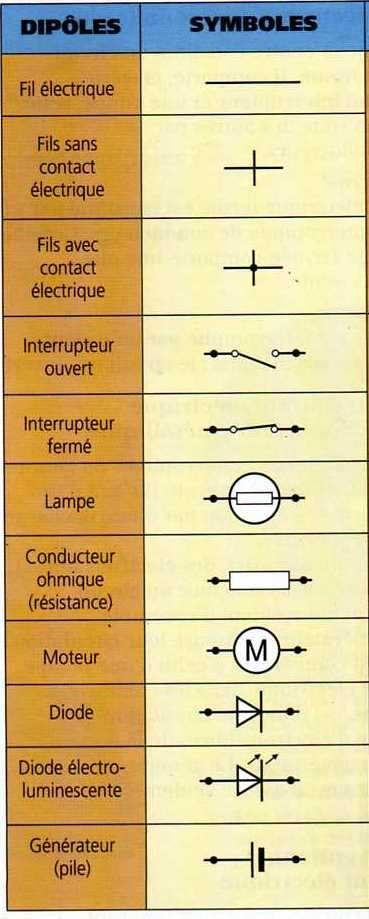
Quel est le symbole de la pile ?
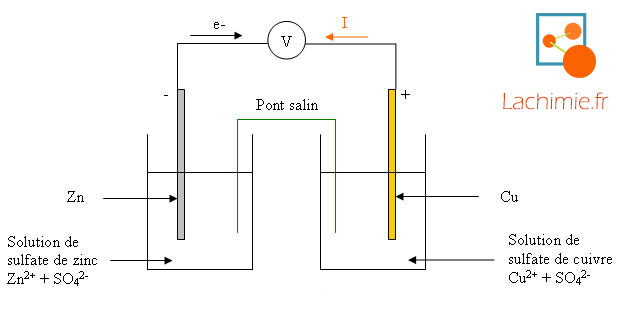
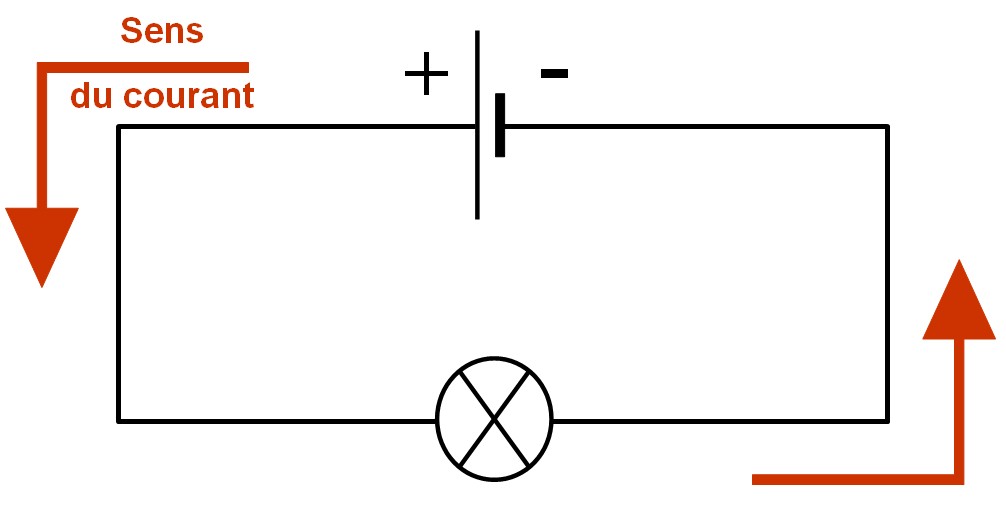
. Le courant électrique ne circule que dans un seul sens : de la borne positive vers la borne négative du générateur (ou de la pile) à l'extérieur de celui-ci.
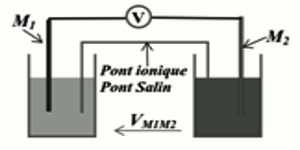
Comment identifier les pôles d'une pile ?
. Si celui-ci indique une valeur négative, alors on l'a branché à l'envers.
. Avec un branchement correct, la borne « com » (négative) du voltmètre est reliée à l'électrode de zinc.
. La borne positive est l'électrode de cuivre.
Comment indiquer la polarité d'une pile ?
. Le pôle positif est celui qui capte les électrons.
Quelle est la FEM de cette pile ?
. E est appelée force électromotrice (f.e.m) de la pile.
. Elle se mesure en volt.
. C'est la tension aux bornes de la pile lorsqu'elle ne débite pas.
|
1) La pile Daniell - AlloSchool
le pont ionique vers la solution de sulfate de zinc et les ions K+ vers la solution de sulfate de cuivre) e) Représentation conventionnelle de la pile: |
|
10-Les piles électrochimiques - Physagreg
Fiche élève Cas de la pile Daniell : Nous allons nous intéresser à la pile Daniell (pile Cu-Zn vue dans le TPχn°10) qui débite à partir du moment où les deux |
|
Rés chim P3C2 (pile) - physique chimie terminale S
borne – vers la borne + de la pile - Les ions en solution Le sens du courant I conventionnel est l'inverse de celui des électrons Les ions du pont salin assurent |
|
Chap8 les piles - LycOrsayPhy
Donner la représentation conventionnelle de cette pile Exercice 2 : Soit la pile cuivre-argent de l'exercice 1 Pendant la durée ∆t = 1,5 min, |
|
Electrochimie - théorie -version élèves - 2018
Calculer le potentiel d'une demi-pile et d'une pile avec l'équation de Nernst Notre pile Zn-cuivre peut être représentée par la représentation conventionnelle ( |
|
Pile Daniell et pile - BACCARI - Jimdo
La représentation conventionnelle (schématique, symbolique et équationnelle) de la pile dépend de l'emplacement (gauche ou droite) des couples redox II |
|
Chimie Résumé N:7 Niveaux - Moutamadrisma
Une pile est constituée par deux demi-piles reliées par un pont salin • Une demi- pile est Représentation conventionnelle de la pile (-) Zn/Zn2+ Cu2+/Cu (+) |
|
TD1 – Léquilibre rédox - Chamilo
Lorsque la pile est à l'équilibre (usée), la réaction redox a atteint l'équilibre thermodynamique Schéma conventionnel : Sn ZnSO4 Fe SO4 Fe 5) Représenter sur le dessin de la question 1, le sens de déplacement des électrons et du |