acide faible base forte
|
Fiche de révisions sur les acides et les bases
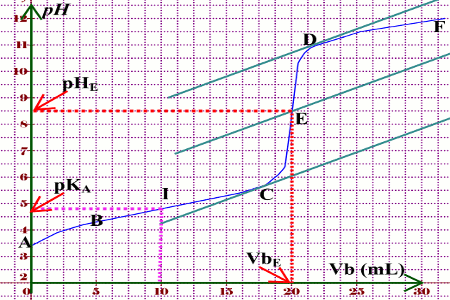
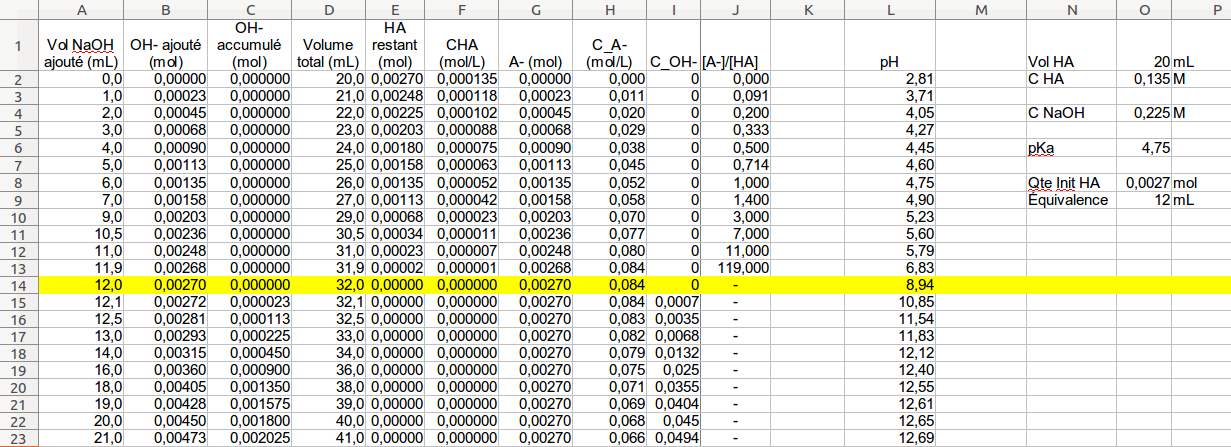
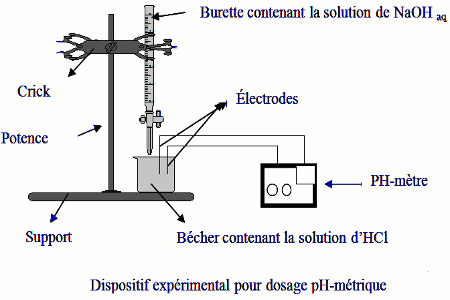
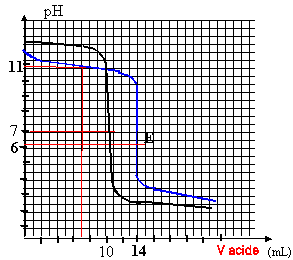
2°) Réaction entre une solution d'acide faible et une solution de base forte : On prend l'exemple d'une réaction entre une solution d'acide éthanoïque et une |
|
Cours-titrage-acide-base-2ème-annnée-pdf
REMARQUE : par analogie dans le cas du titrage d'une base faible par un acide fort le pH au point d'équivalence est toujours inférieur à 7 (point d' |
|
Dosage acide faible – base forte
Les relations établies classiquement le sont pour : ▫ un acide suffisamment faible et pas trop dilué ▫ ou un acide pas trop faible |
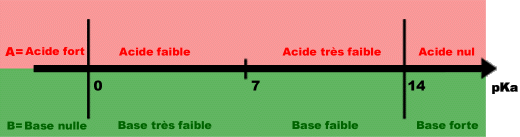
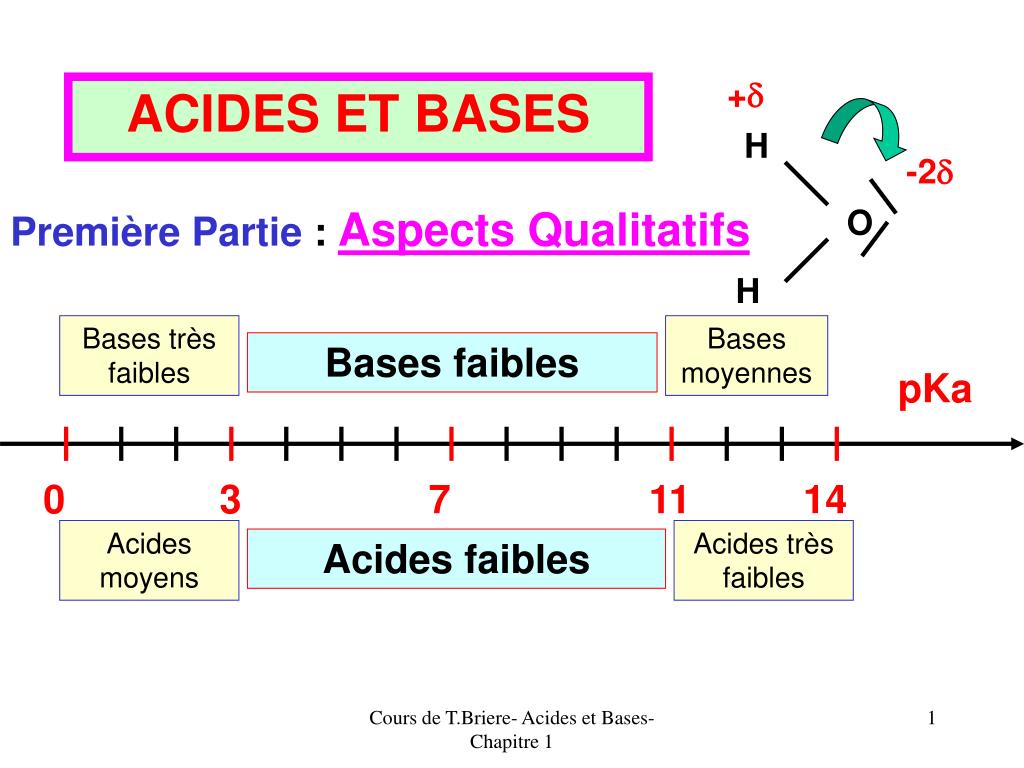
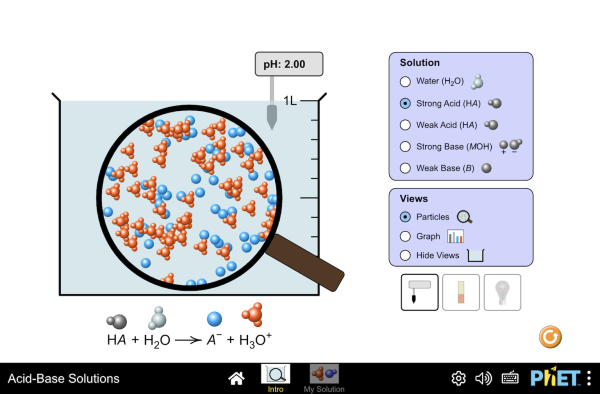
Comment savoir si un acide ou une base est forte ou faible ?
Il est déterminé par la concentration en ions H+ (protons) dans la solution.
Les acides libèrent des protons dans l'eau, abaissant ainsi le pH, tandis que les bases acceptent des protons, augmentant le pH.
Un pH inférieur à 7 indique une solution acide, un pH égal à 7 est neutre, et un pH supérieur à 7 est basique.Est-ce que NaOH est une base forte ou faible ?
L'hydroxyde de sodium (NaOH), également appelé soude caustique, est une base forte qui se présente, à température ambiante, sous forme solide.
Il est constitué de cations sodium (Na+) et d'anions hydroxyde (OH-).Hyponymes
Hyponymes
acide acétique.acide chloroacétique.acide fluorhydrique.acide formique.acide phosphorique.
Comment calculer le pH d'un acide faible et d'une base forte ?
Formule de calcul de pH
1Pour un acide fort : pH = - log C.2) Pour une base forte: pH = 14 + log C.
Ces formules sont valables pour les concentrations supérieures à 10-7 mol/L.
3) Pour un acide faible : pH = 1/2 pKa - 1/2log C.
4) Pour une base faible : pH = 7 + 1/2 pKa + 1/2log C. 5pH = 1/2( pKa1 + pKa2)
|
Dosage acide faible – base forte
Acide faible - base forte. 1. Dosage acide faible – base forte. Les relations établies classiquement le sont pour : ▫ un acide suffisamment faible et pas trop |
|
§ 7 (suite) Titrages acide-base
Le titrage d'une base faible par un acide fort est également le symétrique du cas du titrage d'un acide faible par une base forte: La solution initiale est |
|
Fiche de révisions sur les acides et les bases
donc la base la plus forte dans l'eau. Les couples acide faible / base faible ont tous des constantes d'acidité comprises entre 1 et. 14. 10. |
|
LES TITRAGES ACIDES-BASES
Sa zone de virage couvrant une zone de pH théorique. pH = pKi ± 1. III) Titrage d'un acide fort HA par une base forte B. Considérons le titrage de 100 |
|
VI..Etude sommaire des mélanges
Acides et bases. Chapitre VI. 96 c) courbe de titration pH = f(x). 2) Titrage d'un acide faible par une base forte: 20 ml CH3COOH (pKa = 475) 0 |
|
Dosages acidobasiques
9 fév. 2018 la concentration de l'acide. • le pKa dans le cas d'un acide faible. III.1 Acide fort. Vb = 0 Avant toute introduction de base |
|
Equilibre acidobasique
d'un acide ou d'une base. En général : acide faible / son sel de base forte base forte / son sel d'acide fort. Acide (tampon H) <====> base (tampon. -. ) + H. +. |
|
Chapitre 1 Acides et bases
Un acide est dit : — fort dans l'eau ssi il est totalement dissocié dans l'eau ssi Ka > 1 ssi pKa < 0;. — faible ssi la dissociation est une réaction équilibrée |
|
TRAVAUX PRATIQUES DE CHIMIE DES SOLUTIONS
A la fin d'année les étudiants doivent restituer ces polycopiés. Page 3. Sommaire. TP N°1 : DOSAGE ACIDE FORT - BASE FORTE PAR |
|
7. Transferts de protons Equilibres acide-base
NH3. +. H2O. NH4+. OH–. +. Base (1). Acide (2). Acide (1). Base (2). HCl est un acide fort. Son hydrolyse (réaction avec l'eau) est complète. Dans ce cas H2O |
|
Dosage acide faible – base forte
Dosage acide faible – base forte. Les relations établies classiquement le sont pour : ? un acide suffisamment faible et pas trop dilué. |
|
§ 7 (suite) Titrages acide-base
Le titrage d'une base faible par un acide fort est également le symétrique du cas du titrage d'un acide faible par une base forte: La solution initiale est |
|
Fiche de révisions sur les acides et les bases
donc la base la plus forte dans l'eau. Les couples acide faible / base faible ont tous des constantes d'acidité comprises entre 1 et. 14. 10. |
|
VI..Etude sommaire des mélanges
Acides et bases. Chapitre VI. 80 b) Mélanges d'acides. 1) Acide fort 1 et acide fort 2. Le pH se calcule en sachant que les deux acides sont entièrement |
|
COURS DE CHIMIE GENERALE Semestre 1 SVI
Cas d'une base forte. 2.4. Cas des bases faibles. 2.5. Cas d'un mélange d'un acide fort et d'un acide faible. |
|
Dosage acide faible-base forte
Dosage acide faible – base forte. Les relations établies classiquement le sont pour : ? un acide suffisamment faible et pas trop dilué. |
|
Cours de Chimie - Informatique Titrage acide/base
17 avr. 2013 tion du graphique de l'évolution du pH en fonction du volume de réactif introduit. 1 Titrage d'un acide fort par une base forte. 1.1 Données. |
|
Solutions tampons
de la concentration (voir dosage acide fort - base forte) et ces solutions ne sont donc pas des tampons satisfaisants vis à vis de la dilution. |
|
Les couples acide-base conjuguées
Les acides forts et les bases fortes. • dans un couple acide/base conjuguée si un acide est fort |
|
Chapitre 1 Acides et bases
La base conjuguée d'un acide fort est dite “indifférente dans l'eau” i.e. cette espèce ne L'acide conjugué d'une base faible est un acide faible. |
|
Dosage acide faible – base forte
Dosage acide faible – base forte un acide suffisamment faible et pas trop dilué, ▫ ou un acide pas trop faible Acide faible HA : constante d'acidité Ka titré |
|
Révisions sur les acides et les bases - Nicole Cortial
donc la base la plus forte, dans l'eau Les couples acide faible / base faible ont tous des constantes d'acidité comprises entre 1 et 14 10 |
|
COURS DE CHIMIE GENERALE Semestre 1 SVI - Université Cadi
Cas d'une base forte 2 4 Cas des bases faibles 2 5 Cas d'un mélange d'un acide fort et d'un acide faible |
|
C2 - DOSAGE ACIDE FAIBLE - BASE FORTE - Texas Instruments
Une solution de base forte de concentration connue (NaOH à 0,2 mol L– 1 par exemple) • Une solution d'acide faible de concentration inconnue (ac acétique |
|
VIEtude sommaire des mélanges
d'hydrolyse des acides et bases faibles augmente avec la dilution) Exemple: La réaction entre un acide fort et une base faible est complète si la constante |
|
PH et pKa - Eli Zysman-Colman
pH d'une solution de base forte pH = 14 + log [B] 8 Calcul de pH Formule générale pour le pH de solutions d'acide/base faible: [H3O+] = Ka (([AH] - [H3O+] + |
|
Chapitre 1 Acides et bases
Un acide est dit : — fort dans l'eau ssi il est totalement dissocié dans l'eau ssi Ka > 1 ssi pKa < 0; — faible ssi la dissociation est une réaction équilibrée ssi pKa > |
|
Le pH 6 Le dosage des solutions dacides et des bases faibles
Le dosage des solutions d'acides et de bases faibles 2 n(B) Moles de base forte (utilisée pour doser l'acide faible) CA0 Concentration initiale d'acide fort |
|
§ 7 (suite) Titrages acide-base - EPFL
Considérons le titrage d'une solution d'un acide faible, tel que l'acide acétique par exemple, par une base forte, comme NaOH La fonction pH = ƒ() dans ce cas |
|
Transformations chimiques en solution aqueuse - Chimie en PCSI
7 II – LA REACTION ACIDE/BASE 8 1 LES ACIDES FORTS ET LES BASES FORTES 8 2 LES ACIDES FAIBLES ET LES BASES FAIBLES : CONSTANTE |