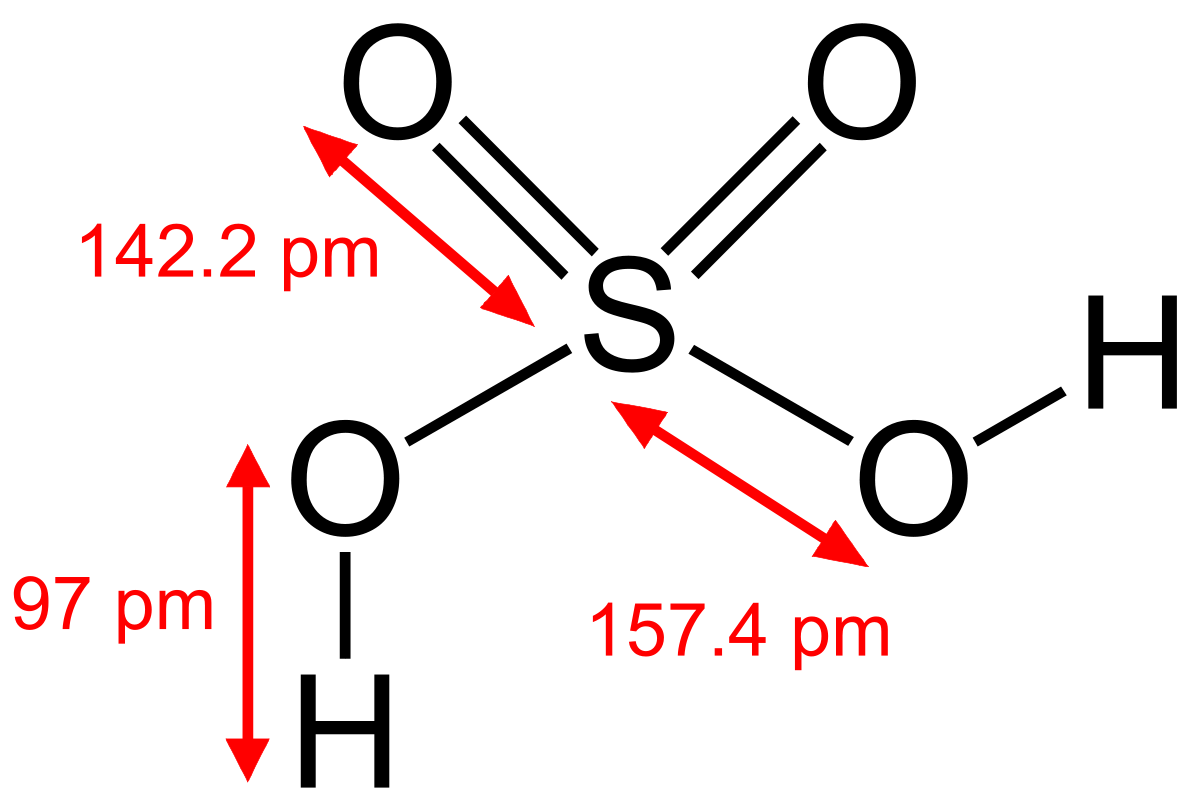
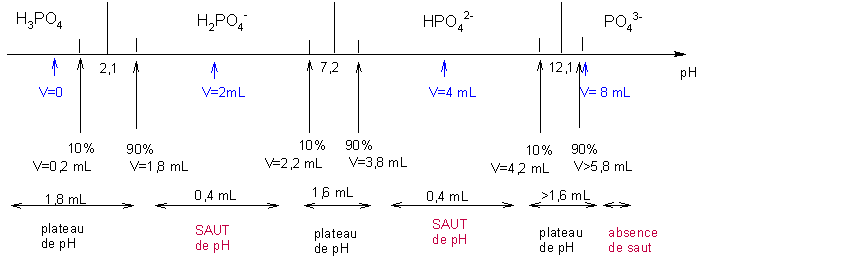
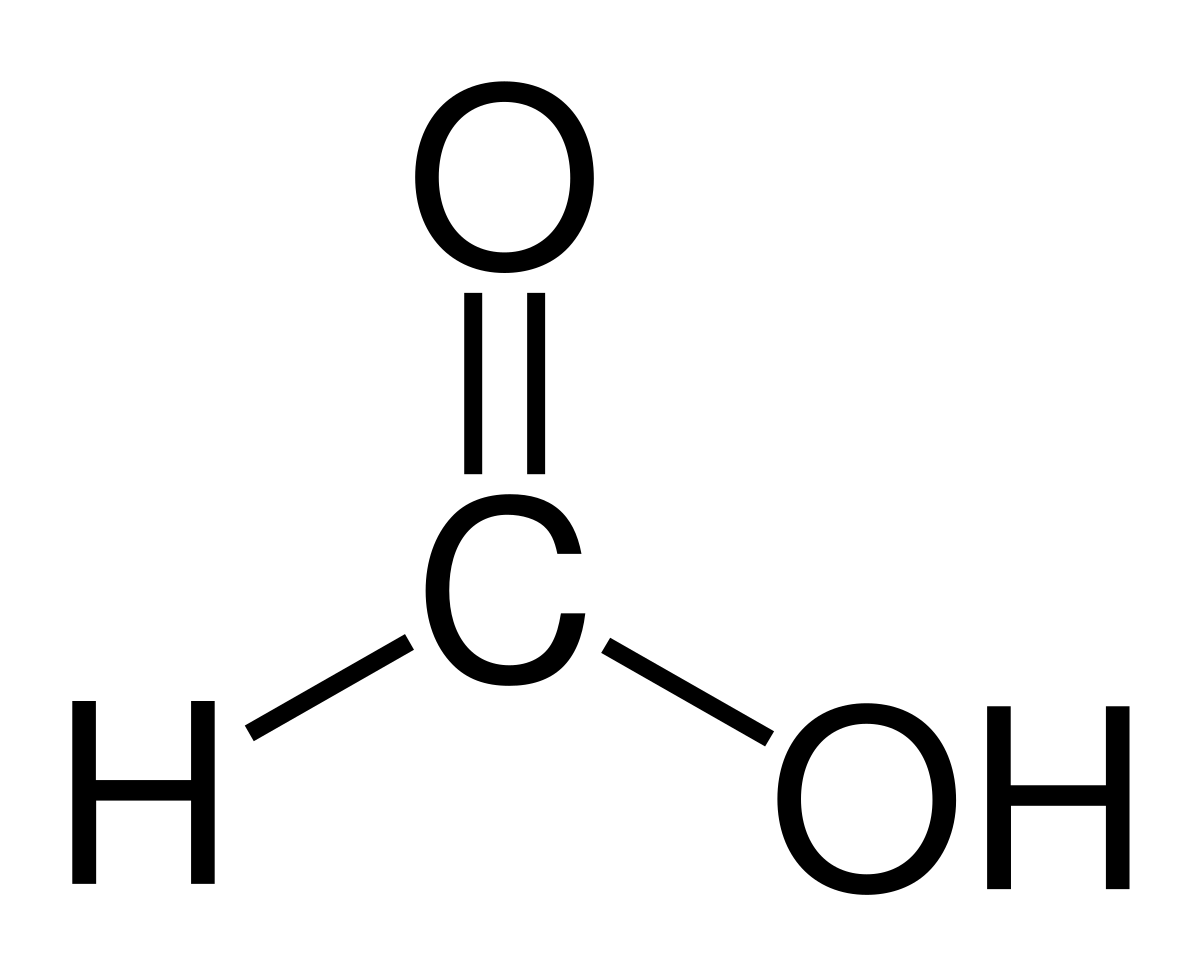
acide faible formule
Quelles sont les acides faibles ?
Il a défini le pH comme le logarithme négatif de base 10 de l'activité des ions hydrogène dans une solution, exprimée en mol par litre.
Ainsi, la formule du pH est pH = -log[H⁺], où [H⁺] représente la concentration des ions hydrogène dans la solution.Comment calculer un acide faible ?
Les acides faibles forment un équilibre, dans lequel la majorité des molécules présentes sont des molécules d'acide et seule une infime partie donne ses protons et se dissocie en ions.
Plus un acide est fort, plus l'équilibre se déplace vers la droite et plus la concentration d'ions hydrogène en solution est élevée.
|
PH et pKa - Eli Zysman-Colman
Formule générale pour le pH de solutions d'acide/base faible: [H3O+] = Ka (([AH] - [H3O+] + [OH-]) / ([A-] + [H3O+] - [OH-])) • pH d'une solution d'acide faible |
|
COURS DE CHIMIE GENERALE Semestre 1 SVI - Université Cadi
2 5 Cas d'un mélange d'un acide fort et d'un acide faible Soit par des formules physiques appelées équations d'état comme, par exemple, l'équation |
|
Révisions sur les acides et les bases - Nicole Cortial
donc la base la plus forte, dans l'eau Les couples acide faible / base faible ont tous des constantes d'acidité comprises entre 1 et 14 10 |
|
Formules de Phpdf - Proximus
d'ionisation de l'eau 3 Monoacides faibles Un acide faible est un acide qui n'est pas totalement dissocié et donc dont le pKa |
|
Dosage acide faible – base forte
Les relations établies classiquement le sont pour : ▫ un acide suffisamment faible et pas trop dilué, ▫ ou un acide pas trop faible Acide faible HA : constante |
|
Chapitre 1 Acides et bases
L'acide conjugué d'une base faible est un acide faible Exemples : Voici par exemple l'alanine, de formule générale CH3 – CH(NH2)–COOH : CH3 – CH( NH3 |
|
VIEtude sommaire des mélanges
Les formules de dilution restent valables pour les concentrations d'espèces l' acide faible possède une constante d'acidité et une concentration assez faibles), |
|
Réactions acido-basiques en solution aqueuse
Soit un acide faible AH qui réagit avec l'eau selon la réaction d'équation : en soluté apporté C0 se calcule simplement à l'aide de la formule : En effet [AH]f = 0 |
|
Transformations chimiques en solution aqueuse - Chimie en PCSI
LES ACIDES FAIBLES ET LES BASES FAIBLES : CONSTANTE D'ACIDITE ASSOCIEE 9 3 formule et nature – faible ou forte – des acides sulfurique, |