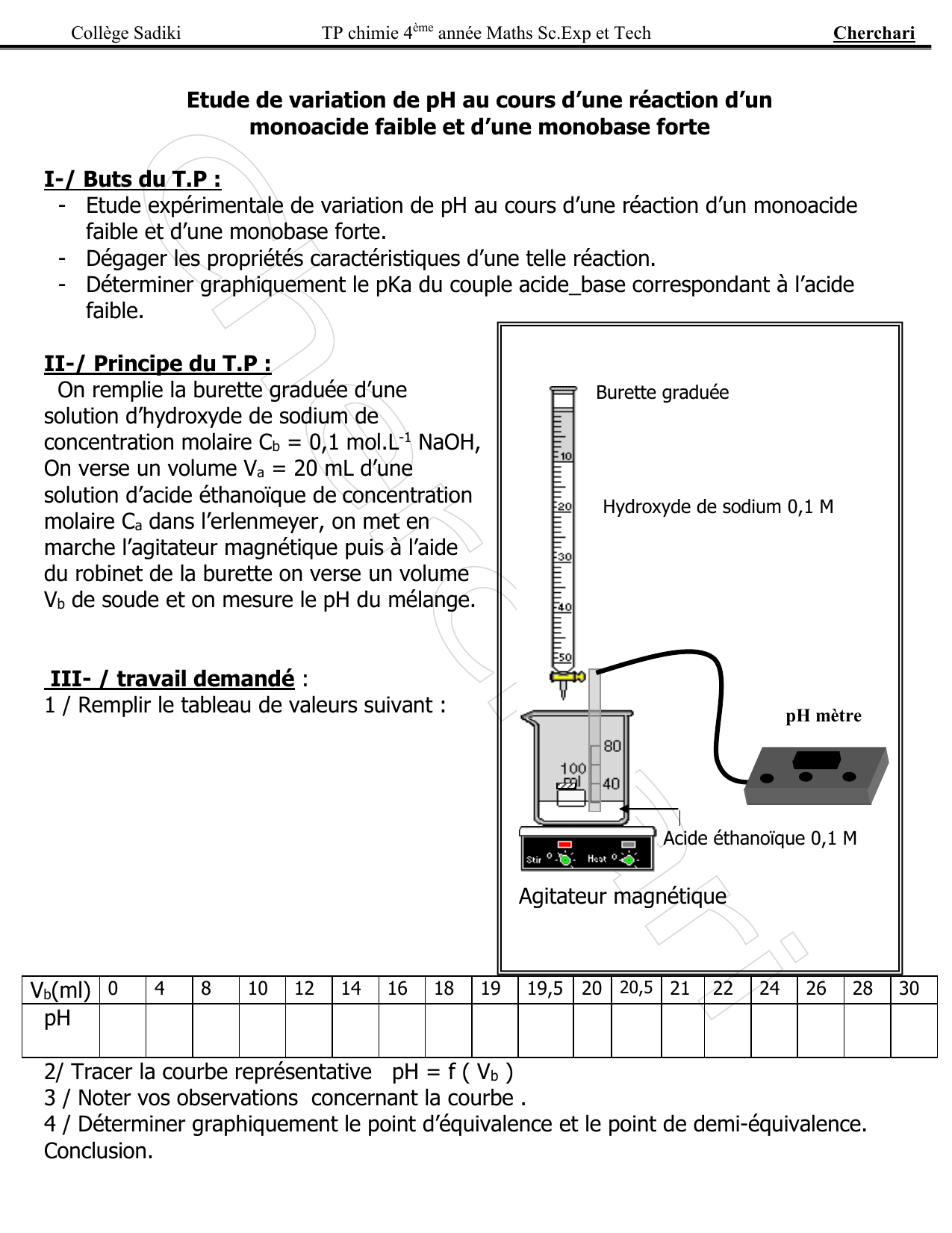
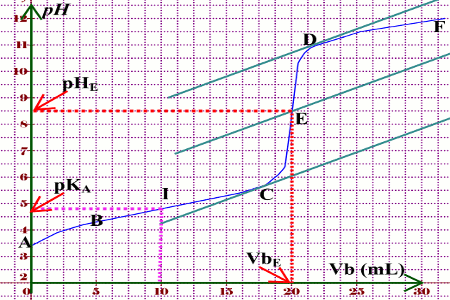
acide faible ph pka
|
PH et pKa
Un acide est une espèce qui a tendance à perdre un proton [H2O] est très grand et ~constant Constante d'acidité pKa = -log Ka |
|
§ 7 (suite) Calcul du pH de solutions
Si la concentration d'un acide faible HA ou d'une base faible B en solution est suffisamment grande et leur pKa ou pKb également suffisamment grand la fraction |
|
Réactions acido-basiques en solution aqueuse
Exemple : Pour un acide faible de pKa = 5 et C0 = 10-3 mol L-1 on a α = 0095 = 95 Cela signifie que pour 100 moles d'acide moins de 10 d'entre elles |
Comment trouver le Ka à partir du pH ?
Comment calculer le pKa à partir du pH ? - Quora.
Dans une réaction acide+H20 la constante d'acidité (Ka) = concentration des produits/concentration des réactifs.pKA, = 15,75 (couple H,O/OH-). = - 1,'75.
Les points représentant, sur l'échelle d'acide-basicité de l'eau, les deux couples H30+/Hz0 et HzO/OH- sont donc déplacés symé- triquement de 1,75 unité de pK par rapport aux valeurs 0- 14, les autres couples acide-base conservant les mêmes positions.
Quelle est le pKa d'un acide faible ?
On classe les acides faibles en fonction de leur constante d'acidité, c'est-à-dire en fonction de leur capacité à plus ou moins se dissocier en présence d'eau.
On considère qu'un acide est faible lorsque son pKa est supérieur à −1,74 à 25 °C (pKa du cation hydronium H3O+).
Quelle est la relation entre le pKa et le pH ?
La formule qui relie le pH et le pKA d'un couple acide-base AH / A– est : pH = pKA + .
|
Fiche de synthèse n°2 : réactions acido-basiques en solution aqueuse
Lien entre le pH et le pKa d'un couple. Le pH d'une solution contenant un acide faible AH et sa base conjuguée A? est lié au pKa du couple AH/A?par la |
|
PH et pKa
de même concentration d'un acide faible. ([HCl] 0.1 M pH < 1; [CH3COOH] 0.1 M |
|
§ 7 (suite) Titrages acide-base
1 et pH = pKa. – pour ! = 1 la neutralisation est terminée. On a une solution contenant ca· "a du sel de la base conjuguée de notre acide faible (de |
|
Dosage acide faible – base forte
pH a bb aa bb a. ?. +. = ?. +. = dosage d'un acide faible (pKa=3 ca=0.01 mol.L-1) par une base forte (cb=0.01 mol.L-1) x = n base versé / n acide initial. |
|
Chapitre 1 Acides et bases
acide si son pH est inférieur à 7 i.e. [H3O+]> 10?7 mol.L?1 (à 25?C) ; faible ssi la dissociation est une réaction équilibrée ssi pKa > 0. |
|
§ 7 (suite) Calcul du pH de solutions
Si la concentration d'un acide faible HA ou d'une base faible B en solution est suffisamment grande et leur pKa ou pKb également suffisamment grand |
|
Solutions tampons
négligeables si le pKa de l'acide faible est peu élevé. Dans ces conditions pour les faibles valeurs de x |
|
LES REACTIONS ACIDE-BASE 1. Le pH 1.1 Définition Le pH
Le pH est lié à la concentration en ions oxonium [H3O+] par la relation : couple acide-base faible dont le pKa est voisin du « pH tanponné ». |
|
PH dune solution de chlorure dammonium pH = 5.6
+ est un acide faible ; il va rester de façon prédominante sous cette forme (pH ? pKa). La solution est une solution acide : on peut donc prévoir que le pH |
|
PH et pKa - Eli Zysman-Colman
de même concentration d'un acide faible ([HCl] 0 1 M, pH < 1; [CH3COOH] 0 1 M , pH = 3 7) 6 Exercices 1) Le Ka d'un acide est 8 10-3 Quel est son pKa? |
|
Chapitre 1 Acides et bases
acide si son pH est inférieur à 7, i e [H3O+]> 10−7 mol L−1 (à 25◦C) ; faible ssi la dissociation est une réaction équilibrée ssi pKa > 0 Dans le cas d'un |
|
§ 7 (suite) Calcul du pH de solutions - EPFL
Si la concentration d'un acide faible HA ou d'une base faible B en solution est suffisamment grande et leur pKa ou pKb également suffisamment grand, |
|
PH - UNF3S
Calculer le pH de solutions d'un acide faible HA (pKa = 3,75) aux concentrations suivantes : C = 0,1 mol L-1 ; 10-3 mol L-1 ; 1,5 10-6 mol L-1 A: 2,4 ; 4 8 ; 5,0 |
|
Dosage acide faible – base forte
log pK pH a bb aa bb a − + = − + = dosage d'un acide faible (pKa=3, ca= 0 01 mol L-1) par une base forte (cb=0 01 mol L-1) x = n base versé / n acide initial |
|
Transformations chimiques en solution aqueuse - Chimie en PCSI
LES ACIDES FAIBLES ET LES BASES FAIBLES : CONSTANTE D'ACIDITE en quantités notables les 2 espèces conjuguées AH et A- : pH entre pKA – 1 et |
|
Propriétés des acides et des bases
Equation d'Henderson Hasselbach et Calcul de pH Courbes de Si pH < 7la solution est dite « acide » Si pH > 7la •pKa élevé « Ka faible : acide faible |
|
Cours 5 - Equilibres Acido-basiques
Selon cette théorie un acide est un donneur de proton □ Selon Acides forts Acides faibles Acides négligeables Echelle de pKa : pH 0 14 Bases fortes |