acide fort et faible ph
|
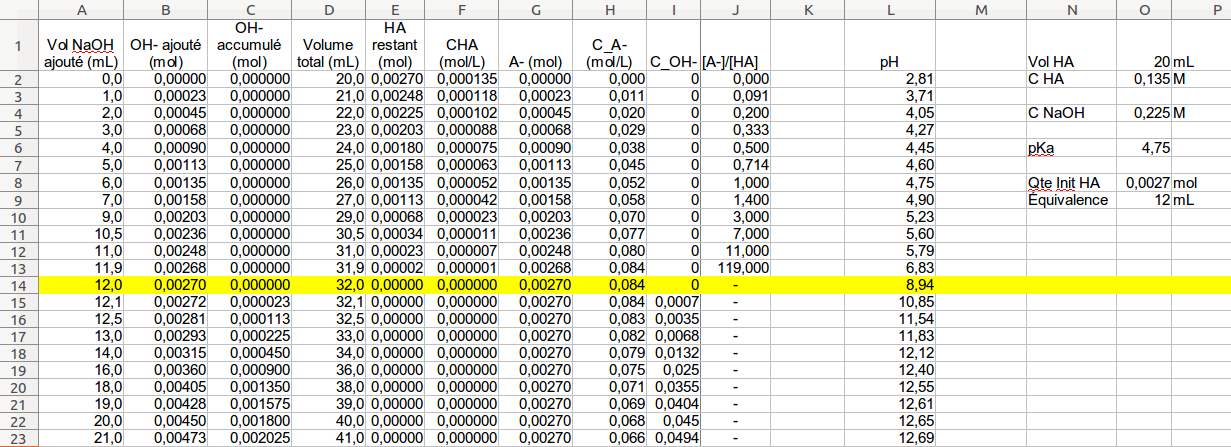
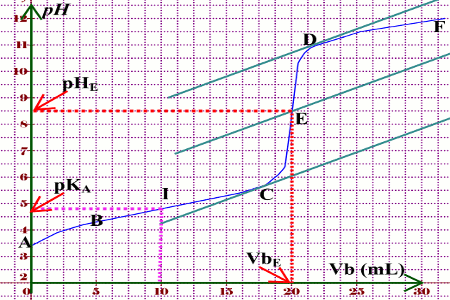
§ 7 (suite) Titrages acide-base
Le pH du point d'équivalence est encore égal à 7 Le titrage d'une base faible par un acide fort est également le symétrique du cas du titrage d'un acide faible |
|
Déterminer si un acide est fort ou faible
Un acide est fort s'il de dissocie totalement lors de sa mise en solution On a alors la relation [H3O+]=C • Un acide est faible s'il se dissocie |
Selon leur structure : on distingue deux catégories d'acide :
Selon leur structure : on distingue deux catégories d'acide :
1Les hydracides ou acides binaires, composés d'un non-métal et d'hydrogène : HnX ;2Les oxoacides ou acides ternaires, composés d'un non-métal ou d'un métal de transition fortement oxydé, associé à des atomes d'hydrogène et d'oxygène : HnXOm.
Comment savoir si un acide est fort ou faible pH ?
Comment savoir si on a un acide fort ou faible ? On peut savoir si on a un acide fort ou faible à partir de sa dissociation : S'il se dissocie totalement en solution, il s'agit d'un acide fort.
S'il ne se dissocie que partiellement, il est considéré comme un acide faible.
Comment calculer le pH d'un mélange acide faible base forte ?
Si l'on admet que les ions OH– provenant de la dissociation de la base conjuguée de notre acide faible sont en quantité négligeable par rapport à ceux provenant de la solution titrante de base forte, on a simplement : pH = 14 + log { ctitr⋅"titr / c0 }.
Comment définir un acide fort ?
Un acide fort est un acide réagissant totalement avec l'eau.
Si sa concentration est c, alors .
Un acide faible AH réagit avec l'eau selon une réaction limitée .
Une base forte réagit avec l'eau selon une réaction totale.
|
Déterminer si un acide est fort ou faible
On connait le pH et la concentration de la solution. Pour savoir si l'acide est fort ou faible il faut : 1. Déterminer [H3O+] par la relation [H3O+]=10-pH |
|
PH et pKa
Une solution contenant un acide fort a un pH inférieur à celui d'une solution de même concentration d'un acide faible. ([HCl] 0.1 M pH < 1; [CH3COOH] 0.1 M |
|
§ 7 (suite) Titrages acide-base
Un indicateur est un acide faible dont la forme acide HIn est caractérisé par Titrage d'un acide fort par une base forte. pH ! "a = V0 / (V0 + Vtitr). |
|
Chapitre 1 Acides et bases
faible ssi la dissociation est une réaction équilibrée ssi pKa > 0. Dans le cas d'un acide fort totalement dissocié dans l'eau |
|
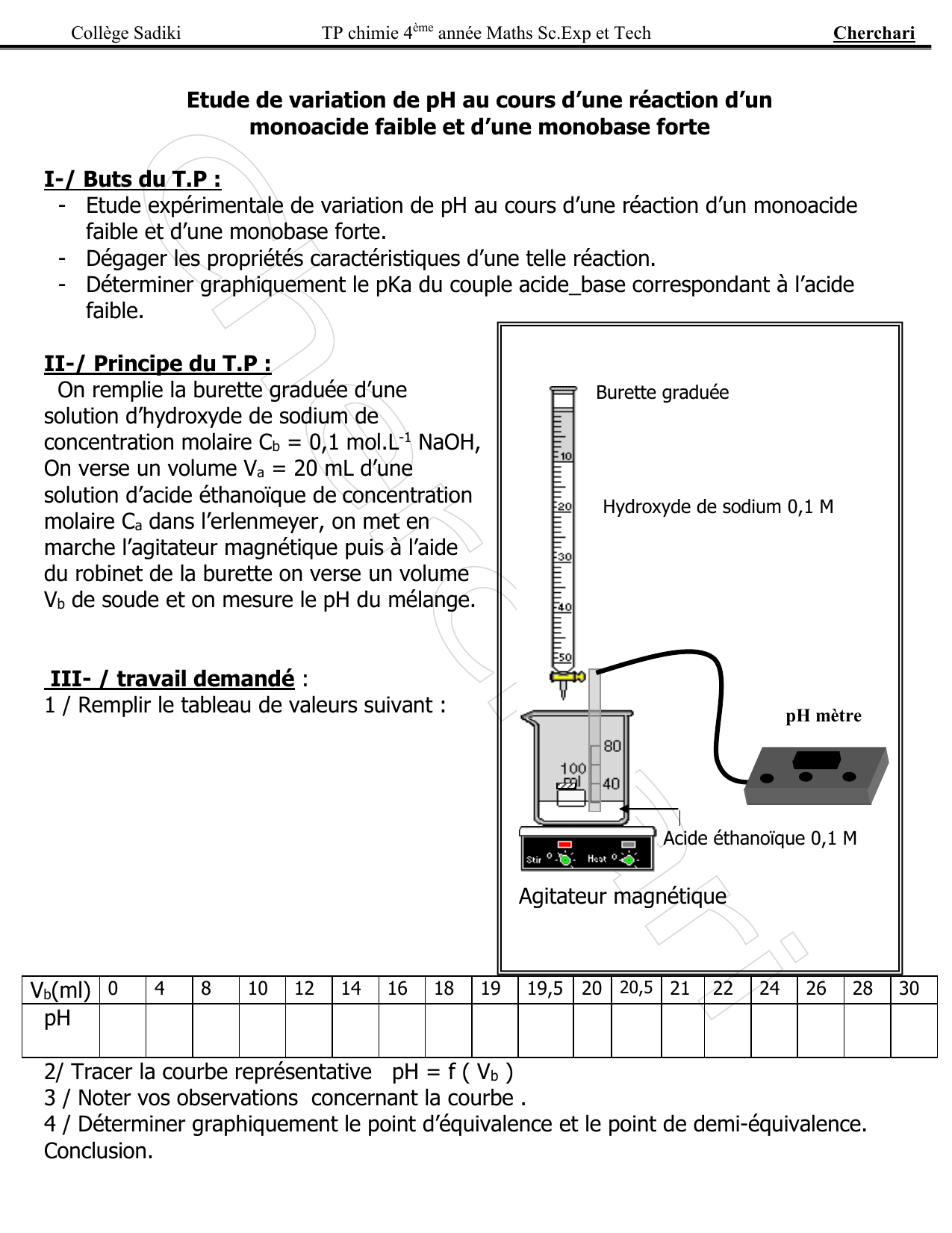
Chapitre n°…. : Notion dacides et de bases fortes et faibles TP n
Objectifs bac : Pratiquer une démarche expérimentale pour : -Mesurer le pH d'une solution. -Identifier le caractère fort ou faible d'un acide. |
|
VI..Etude sommaire des mélanges
2) Acide fort 1 + acide faible 2. On calcule souvent le pH en négligeant l'acide faible. Cette approximation grossière n'est justifiée que si l'apport |
|
Dosages acidobasiques
9 feb 2018 chera par exemple la concentration d'un acide (fort ou faible) ... sique (pH couleur d'un indicateur coloré |
|
Fiche de synthèse n°2 : réactions acido-basiques en solution aqueuse
Le pH d'une solution contenant un acide faible AH et sa base conjuguée A? est dissocié dans l'eau le pH d'une solution d'acide fort de concentration. |
|
TD1b : Acides et bases suite
Le pH de la solution d'acide benzoïque (acide faible) est acide mais supérieur au pH de la solution d'acide fort de même concentration : pH = 3 |
|
Fiche de révisions sur les acides et les bases
Exemples de réactions de dissolution de bases et d'acides forts : • L'acide nitrique )ONH( pH +=. 3°) Solution d'acide faible de concentration molaire 1. |
|
Révisions sur les acides et les bases - Nicole Cortial
Exemples de réactions de dissolution de bases et d'acides forts : • L'acide pH += 3°) Solution d'acide faible de concentration molaire 1 C 1 Clog pH −≠ |
|
PH et pKa - Eli Zysman-Colman
Une solution contenant un acide fort a un pH inférieur à celui d'une solution de même concentration d'un acide faible ([HCl] 0 1 M, pH < 1; [CH3COOH] 0 1 M, |
|
COURS DE CHIMIE GENERALE Semestre 1 SVI - Université Cadi
CALCUL DE PH DES SOLUTIONS AQUEUSES 2 1 Cas d'un acide fort 2 2 Cas d'un acide faible 2 3 Cas d'une base forte 2 4 |
|
VIEtude sommaire des mélanges
acide fort 2 Le pH se calcule en sachant que les deux acides sont entièrement ionisés La réaction entre un acide fort et une base faible est complète si la |
|
Chapitre 1 Acides et bases
acide si son pH est inférieur à 7, i e [H3O+]> 10−7 mol L−1 (à 25◦C) ; — basique si Dans le cas d'un acide fort, totalement dissocié dans l'eau, la concentration finale L'acide conjugué d'une base faible est un acide faible Exemples : |
|
Le pH 3 Le pH des acides et bases forts - théorie - 2014
A la fin de ce chapitre vous devrez être capable de • Déterminer si une espèce chimique est un acide fort, un acide faible, une base forte ou une base faible |
|
Calcul du PH
Solution de deux acides forts A, H et A,H (CA, CA) 8- pH d'une solution d'une base faible très diluée la concentration [BH]n'est plus négligée devant Co |
|
§ 7 (suite) Calcul du pH de solutions - EPFL
Si la concentration d'un acide faible HA ou d'une base faible B en solution est suffisamment grande et leur pH d'une solution d'un acide fort Soit une solution |
|
§ 7 (suite) Titrages acide-base - EPFL
Un indicateur est un acide faible dont la forme acide HIn est caractérisé par une Titrage d'un acide fort par une base forte pH "a = V0 / (V0 + Vtitr) pH = – log |