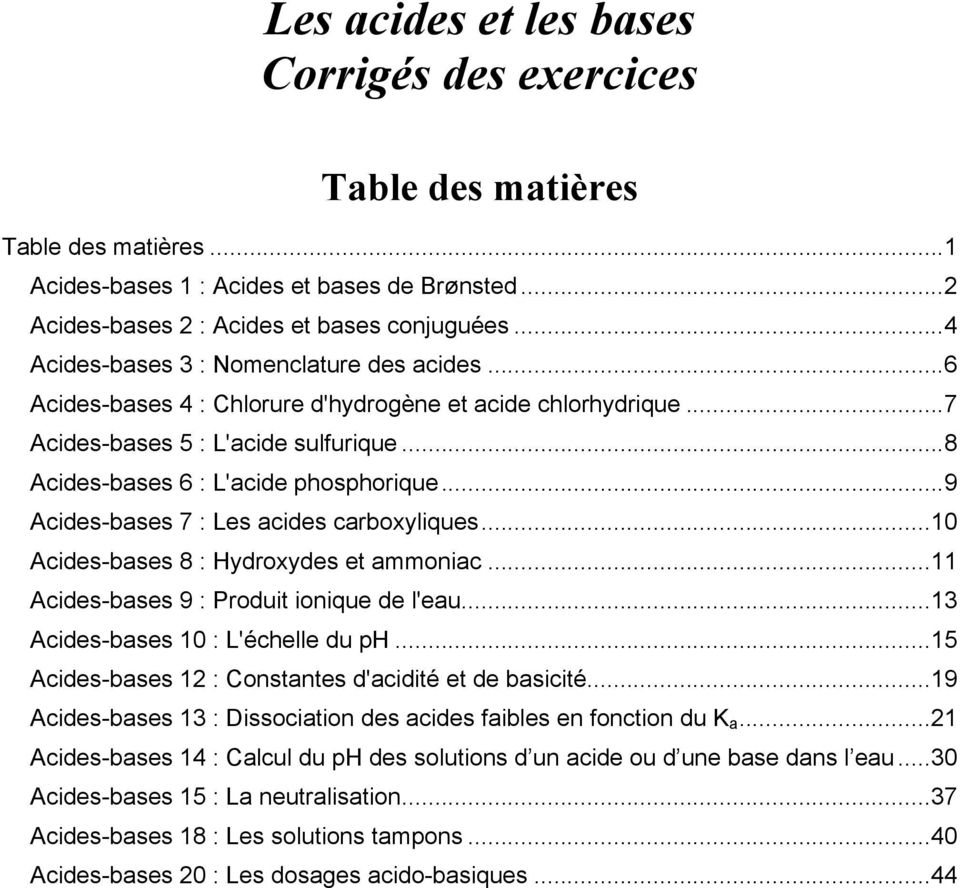
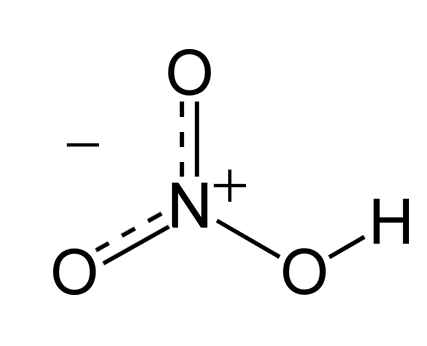
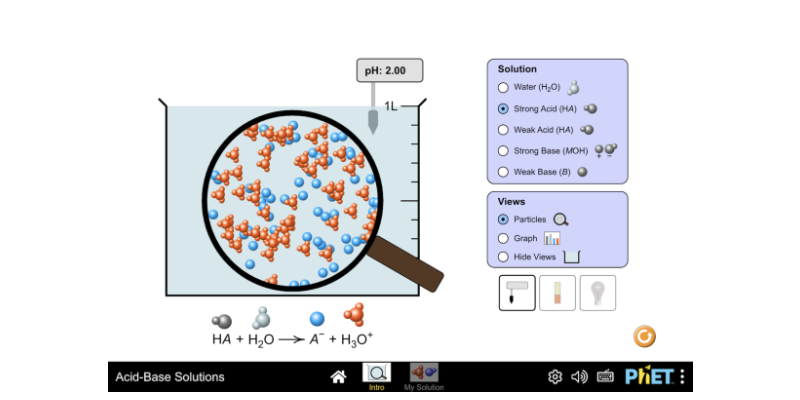
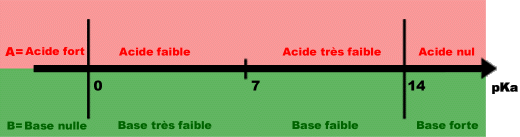
acide fort ou faible ph
|
PH et pKa
Une solution contenant un acide fort a un pH inférieur à celui d'une solution de même concentration d'un acide faible ([HCl] 0 1 M pH < 1; [CH3COOH] 0 1 M pH |
|
Déterminer si un acide est fort ou faible
Pour savoir si l'acide est fort ou faible il faut : 1 Déterminer [H3O+] par la relation [H3O+]=10-pH ( voir fiche précédente ) 2 Comparer cette valeur à |
Quelle est la formule du pH d'un acide faible ?
L'acide méthanoïque (L'acide méthanoïque (appelé aussi acide formique) est le plus simple des acides), l'acide éthanoïque et les autres acides carboxyliques sont des acides faibles.
Quel est le pH acide ?
Un pH inférieur à 7 indique que l'eau est acide alors qu'un pH supérieur à cette valeur indique qu'il s'agit d'une eau alcaline.
La baisse d'une unité de pH implique que l'acidité est multipliée par un facteur 10.
|
Déterminer si un acide est fort ou faible
On connait le pH et la concentration de la solution. Pour savoir si l'acide est fort ou faible il faut : 1. Déterminer [H3O+] par la relation [H3O+]=10-pH |
|
§ 7 (suite) Titrages acide-base
Un indicateur est un acide faible dont la forme acide HIn est caractérisé par Titrage d'un acide fort par une base forte. pH ! "a = V0 / (V0 + Vtitr). |
|
PH et pKa
Une solution contenant un acide fort a un pH inférieur à celui d'une solution de même concentration d'un acide faible. ([HCl] 0.1 M pH < 1; [CH3COOH] 0.1 M |
|
Chapitre 1 Acides et bases
faible ssi la dissociation est une réaction équilibrée ssi pKa > 0. Dans le cas d'un acide fort totalement dissocié dans l'eau |
|
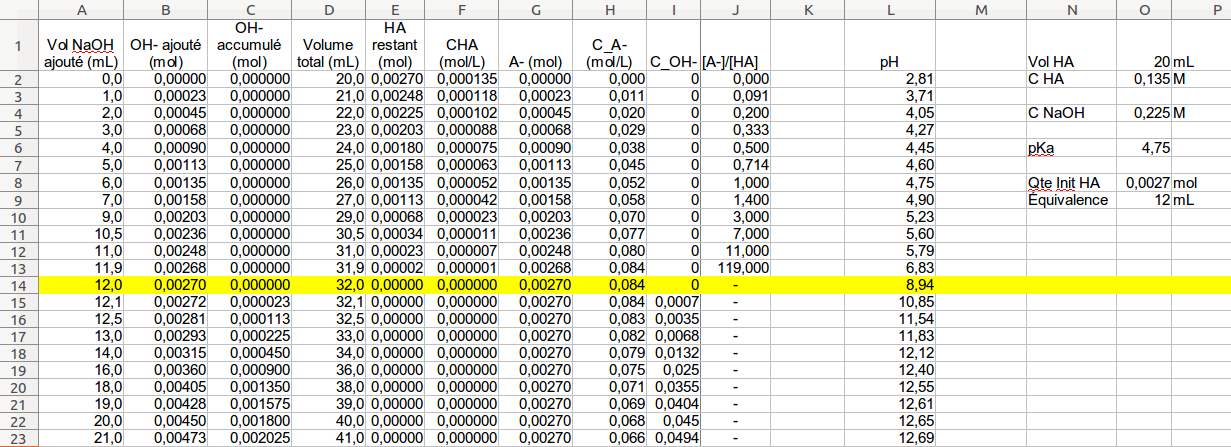
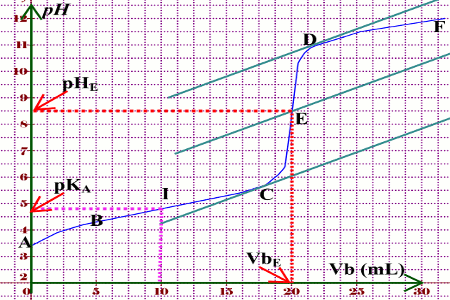
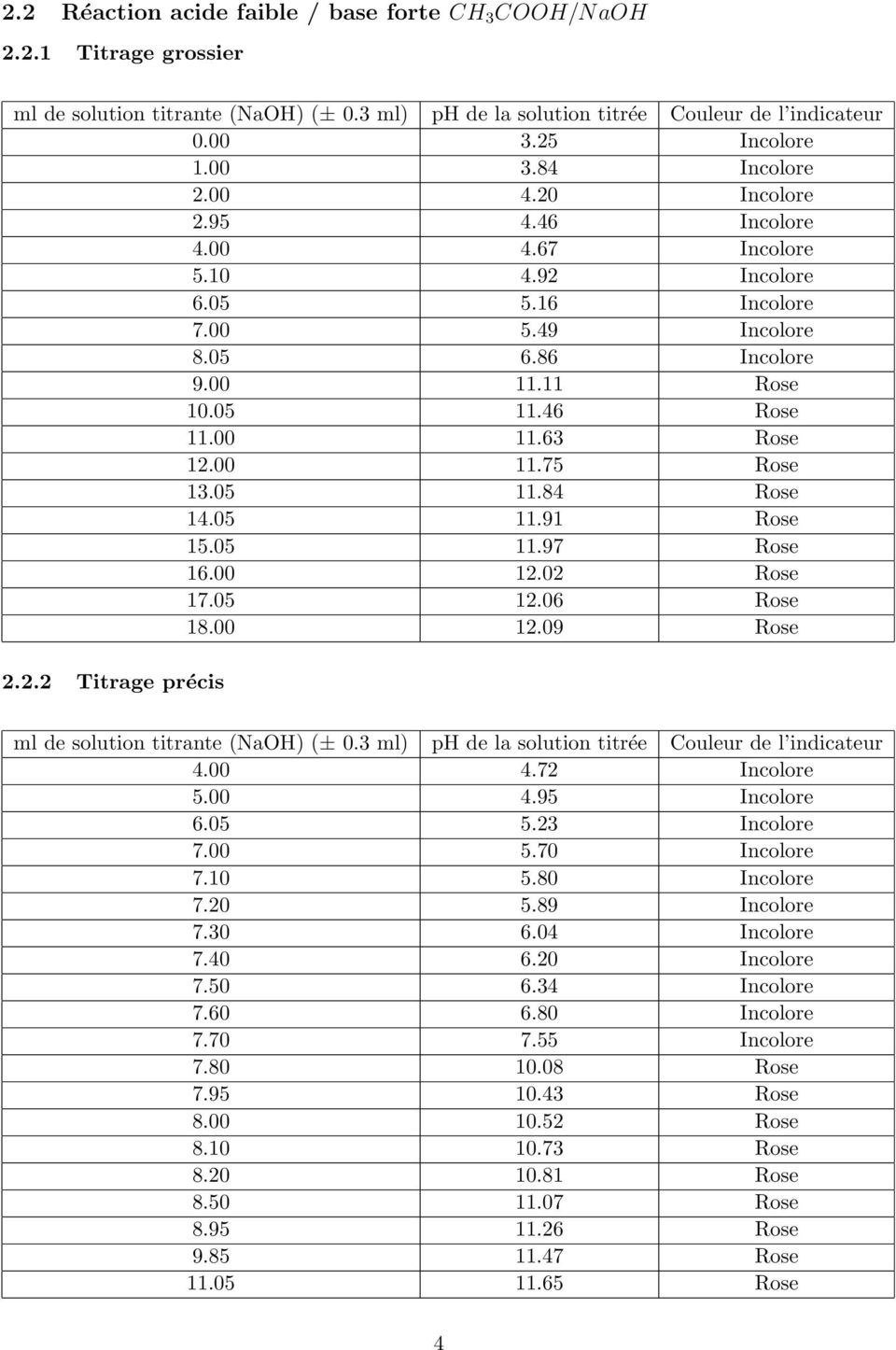
Dosage acide faible – base forte
pH a bb aa bb a. ?. +. = ?. +. = dosage d'un acide faible (pKa=3 ca=0.01 mol.L-1) par une base forte (cb=0.01 mol.L-1) x = n base versé / n acide initial. |
|
Solutions tampons
Par contre lors du dosage d'un acide faible |
|
Fiche de révisions sur les acides et les bases
Exemples de réactions de dissolution de bases et d'acides forts : • L'acide nitrique )ONH( pH +=. 3°) Solution d'acide faible de concentration molaire 1. |
|
Concours de Réorientation Session 2014 Corrigé de lépreuve de
L'acide le plus fort est celui qui possède le pKa le plus faible : HCOOH -le pH à l'équivalence. subit une diminution (la dilution tend le pHE vers 7). |
|
COURS DE CHIMIE GENERALE Semestre 1 SVI
2. CALCUL DE PH DES SOLUTIONS AQUEUSES. 2.1. Cas d'un acide fort. 2.2. Cas d'un acide faible. 2.3. Cas d'une base forte. 2.4. Cas des bases faibles. 2.5. |
|
Déterminer si une base est fort ou faible
Pour savoir si la base est forte ou faible il faut : acide. Concentration ( mol.L-1 ). pH. [HO-] ( mol.L-1 ). Faible ou forte. |
|
Déterminer si un acide est fort ou faible - archimede
On connait le pH et la concentration de la solution Pour savoir si l'acide est fort ou faible, il faut : 1 Déterminer [H3O+] par la relation [H3O+]=10-pH ( voir fiche |
|
Révisions sur les acides et les bases - Nicole Cortial
Exemples de réactions de dissolution de bases et d'acides forts : • L'acide pH += 3°) Solution d'acide faible de concentration molaire 1 C 1 Clog pH −≠ |
|
PH et pKa - Eli Zysman-Colman
Une solution contenant un acide fort a un pH inférieur à celui d'une solution de même concentration d'un acide faible ([HCl] 0 1 M, pH < 1; [CH3COOH] 0 1 M, |
|
COURS DE CHIMIE GENERALE Semestre 1 SVI - Université Cadi
CALCUL DE PH DES SOLUTIONS AQUEUSES 2 1 Cas d'un acide fort 2 2 Cas d'un acide faible 2 3 Cas d'une base forte 2 4 |
|
Chapitre 1 Acides et bases
acide si son pH est inférieur à 7, i e [H3O+]> 10−7 mol L−1 (à 25◦C) ; — basique si Dans le cas d'un acide fort, totalement dissocié dans l'eau, la concentration finale L'acide conjugué d'une base faible est un acide faible Exemples : |
|
VIEtude sommaire des mélanges
acide fort 2 Le pH se calcule en sachant que les deux acides sont entièrement ionisés La réaction entre un acide fort et une base faible est complète si la |
|
Le pH 3 Le pH des acides et bases forts - théorie - 2014
A la fin de ce chapitre vous devrez être capable de • Déterminer si une espèce chimique est un acide fort, un acide faible, une base forte ou une base faible |
|
PH - UNF3S
Calculer le pH de solutions d'un acide faible HA (pKa = 3,75) aux Quelle est la masse de NaOH (base forte, M = 40 g mol-1) qu'il faut dissoudre pour obtenir 1 |
|
§ 7 (suite) Calcul du pH de solutions - EPFL
Si la concentration d'un acide faible HA ou d'une base faible B en solution est suffisamment grande et leur pH d'une solution d'un acide fort Soit une solution |
|
Calcul du PH
Solution de deux acides forts A, H et A,H (CA, CA) 8- pH d'une solution d'une base faible très diluée la concentration [BH]n'est plus négligée devant Co |