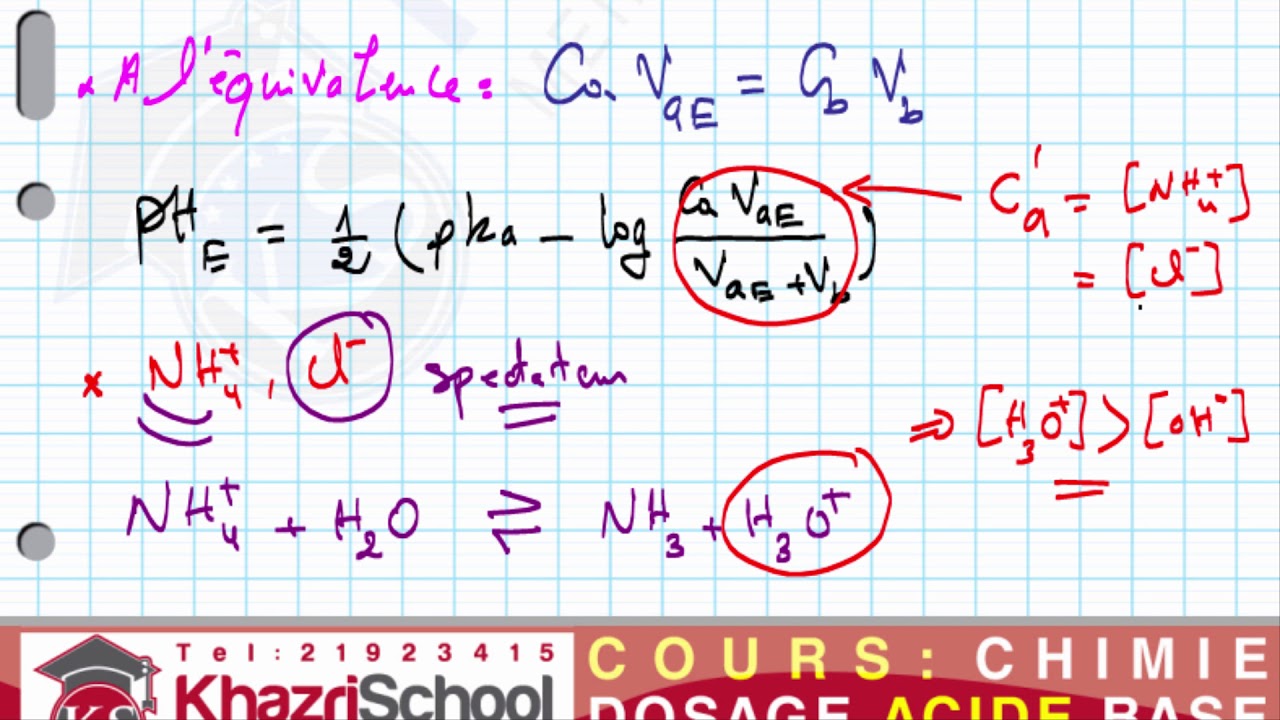calcul ph acide faible base forte
|
Méthodes de calcul des pH
base forte b < a base faible et acide conjugué b = a acide faible b > a acide faible et acide fort Pour a moles d’un triacide et b moles de base forte b < a acide et base conjuguée 1 b = a sel acide a < b < 2a acide et base conjuguée b = 2a sel acide 2a < b < 3a acide et base conjuguée b = 3a sel acide b > 3a base faible et base forte log BH |
|
§ 7 (suite) Calcul du pH de solutions
pH d’une solution d’une base forte L’ionisation d’une base forte B est complète : B + H 2O → BH+ + OH– Bilan de charges: [OH–] = [H 3O+] + [BH+] (2) [H 3O+] = – 1/ 2 c b + √ 1/ 4 c b2 + K e· (c0)2 Tant pour l’acide fort que pour la base forte la solution générale se simplifie pour le cas où K |
|
§ 7 (suite) Titrages acide-base
quantité négligeable par rapport à ceux provenant de la solution titrante de base forte on a simplement : pH = 14 + log { c titr⋅\" titr / c0} 166 Courbe de titrage d’un acide faible pH = pK a + log { ! / (1–!) } Titrage d’un acide faible par une base forte point d’équivalence pH = 7 + 1/ 2 pK a + 1/ 2 log ( c a· \" a / c0) pH |
|
CARNETS DU TUTO CHIMIE ACIDES/BASES EN SOLUTION AQUEUSE PARTIE 2
2 2 Lien entre et force des acides/bases -Si 01 : l’acide ou la base est faible-Si 09 : l’acide ou la base est forte - Si 01 09 : l’acide ou la base est de force moyenne |
|
ème année LES TITRAGES ACIDES-BASES
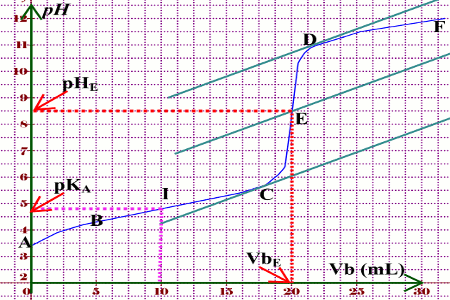
Ce qui est commun à toutes les courbes de neutralisation c'est le fait que le point d'équivalence est un point d'inflexion de la courbe; Ce qui différencie les courbes c'est entre autres leur allure au voisinage immédiat du point d'équivalence c'est-à-dire la variation du pH: ◼ Elle est très brusque et couvre une zone de pH assez grande si l'a |
Comment calculer le dosage d'un acide faible par une base faible ?
Le dosage d'un acide faible par une base faible est peu précis. La forme de la courbe d'une part et sa position d'autre part renseignent sur la force. C'est ainsi qu'un acide est d'autant plus faible que la courbe est plus haute, la base est d'autant plus faible que la courbe est plus basse.
Comment calculer la concentration de l’acide ?
L’indicateur doit être bien choisi, il faut que son pKi soit le plus voisin possible du pH théorique au point d’équivalence. Sa zone de virage couvrant une zone de pH théorique. pH = - log CA = - log 1 pH = - log C’A, C’A représente la quantité résiduelle d’H+ La concentration de l’acide diminue au fur et à mesure du titrage
Comment calculer le pH d’un acide acétique ?
Le pH est déterminé par la position de l’équilibre de dissociation de l’acide acétique. Après addition de 50ml de NaOH, la moitié de l’acide a été neutralisé par NaOH donc les concentrations CH3COOH et CH3COO- sont égales. Ce pH de demi-neutralisation mérite d’être signalé car il permet la détermination du pKa de l’acide faible.
Quelle est la différence entre un acide fort et une base forte ?
Un acide fort étant totalement dissocié en solution, la concentration en ion H3O+ dans la solution est alors égale à la concentration C de l'acide. Une base forte réagit totalement en solution, la concentration en ion HO – dans la solution est alors égale à la concentration C b de la base.
VIII. Conséquences pratiques:
Ce qui est commun à toutes les courbes de neutralisation, c'est le fait que le point d'équivalence est un point d'inflexion de la courbe; Ce qui différencie les courbes, c'est, entre autres, leur allure au voisinage immédiat du point d'équivalence, c'est-à-dire la variation du pH: ◼ Elle est très brusque et couvre une zone de pH assez grande si l'a
On peut conclure que:
Le dosage d'un acide fort par une base forte est possible avec une grande précision; Le dosage est encore réalisable avec une bonne précision quand un seul des antagonistes est faible; Le dosage d'un acide faible par une base faible est peu précis. IX- Intérêt des courbes de neutralisation: facmed.univ-constantine3.dz
1)1) Appréciation de la force des acides ou des bases:
La forme de la courbe d'une part et sa position d'autre part renseignent sur la force. C'est ainsi qu'un acide est d'autant plus faible que la courbe est plus haute, la base est d'autant plus faible que la courbe est plus basse. facmed.univ-constantine3.dz
2) Détermination des pKa:
Il est possible de connaître le pKa en mesurant le pH à la demi neutralisation. facmed.univ-constantine3.dz
X) Quelques applications des titrages acido-basiques
Les titrages acido-basiques sont utilisés pour doser les innombrables espèces inorganiques, organiques, et biologiques, qui possèdent des propriétés acides ou basiques intrinsèques. De nombreuses autres applications tout aussi importantes impliquent la conversion préalable de l'analyte en acide (ou une base) par un traitement chimique approprié, su
a) Analyse élémentaire :
Azote = l'azote est présent dans de nombreuses substances qui concernent la recherche, l'industrie, et l'agriculture comme par exemple les acides aminés, les protéines, les médicaments de synthèse, les engrais etc
b) Dosage des substances inorganiques :
De nombreuses substances inorganiques peuvent être dosées par titrage par un acide fort ou par une base forte : Sels d'ammonium, nitrates, nitrites, carbonates et mélange de carbonates. L'analyse qualitative et quantitative des constituants d'une solution contenant des carbonates seuls ou mélangés constitue un exemple intéressant de l'application d

Calcul de pH : FORMULES & CONDITIONS

Titrage dun acide faible par une base forte (suite)

Titrage dun acide faible par une base forte
|
Dosage acide faible – base forte
Dosage acide faible – base forte un acide suffisamment faible et pas trop dilué ... x=0 ; vb=0 ; solution d'acide faible. )clog. pK(. 2. 1. pH. |
|
§ 7 (suite) Titrages acide-base
Un indicateur est un acide faible dont la forme acide HIn est caractérisé par Titrage d'un acide fort par une base forte. pH ! "a = V0 / (V0 + Vtitr). |
|
COURS DE CHIMIE GENERALE Semestre 1 SVI
CALCUL DE PH DES SOLUTIONS AQUEUSES. 2.1. Cas d'un acide fort. 2.2. Cas d'un acide faible. 2.3. Cas d'une base forte. 2.4. Cas des bases faibles. |
|
VI..Etude sommaire des mélanges
rendre compte en calculant les pH des deux acides dans la solution finale comme La réaction entre un acide faible et une base forte est complète si la ... |
|
Solutions tampons
Cela implique que la pente de la courbe de son dosage pH-métrique soit concentration en base forte de la solution d'acide faible dosée (dans le bécher) ... |
|
PH et pKa
pH d'une solution de base forte. pH = 14 + log [B]. 8. Calcul de pH. Formule générale pour le pH de solutions d'acide/base faible: [H3O+] = Ka. |
|
§ 7 (suite) Calcul du pH de solutions
Si la concentration d'un acide faible HA ou d'une base faible B en solution est suffisamment grande et leur pKa ou pKb également suffisamment grand la fraction. |
|
Chapitre 1 Acides et bases
La base conjuguée d'un acide fort est dite “indifférente dans l'eau” 6) Un indicateur coloré de pH est un acide faible dont les formes acide et basique ... |
|
TRAVAUX PRATIQUES DE CHIMIE DES SOLUTIONS
TP N°2 : DOSAGE ACIDE FAIBLE - BASE FORTE PAR PH-METRIE ET Calculer la concentration de la solution diluée (après ajout de l'eau distillée) et. |
|
Calculs de pH : limites de validité des formules usuelles
Étant délicates voire impossible à résoudre |
|
Dosage acide faible – base forte
Dosage acide faible – base forte Acide faible HA : constante d'acidité Ka titré Ceci implique que l'acide ne soit pas trop fort ou trop dilué pour que sa |
|
COURS DE CHIMIE GENERALE Semestre 1 SVI - Université Cadi
CALCUL DE PH DES SOLUTIONS AQUEUSES 2 1 Cas d'un acide fort 2 2 Cas d'un acide faible 2 3 Cas d'une base forte 2 4 Cas des bases faibles 2 5 |
|
Le pH 6 Le dosage des solutions dacides et des bases faibles
Calculer la concentration de l'espèce dosée à partir de Ve ou du pH initial de la Concentration initiale d'acide fort (utilisée pour doser la base faible) CA |
|
VIEtude sommaire des mélanges
acide faible 2 Nous admettons sans démonstration la formule suivante: Chapitre VI 85 La réaction entre un acide fort et une base faible est complète si la |
|
PH et pKa - Eli Zysman-Colman
pH d'une solution de base forte pH = 14 + log [B] 8 Calcul de pH Formule générale pour le pH de solutions d'acide/base faible: [H3O+] = Ka (([AH] - [H3O+] + |
|
§ 7 (suite) Calcul du pH de solutions - EPFL
des couples acide-base présents: acide(s) ou base(s) faibles, autoprotolyse de Soit une solution aqueuse d'un acide fort HA de concentration analytique ca |
|
Calcul du PH
A AMZIANE 2- pH d'une solution d'acide fort très diluée Le calcul du pH des solutions repose sur deux systèmes 4- pH d'une solution base forte très diluée |
|
Informatique Titrage acide/base - Cours dinformatique
17 avr 2013 · Dans le cas du titrage d'un acide fort par une base forte, partir de là, calculer le volume de la solution NaOH à ajouter pour obtenir la |
|
Chapitre 1 Acides et bases
La base conjuguée d'un acide fort est dite “indifférente dans l'eau”, i e cette Voici par exemple l'alanine, de formule générale CH3 – CH(NH2)–COOH : |
|
Formules de Phpdf - Proximus
(On parle alors de base protonée) Il suffit de remplacer Ka par Kb et pKa par pKb 2 Acides forts Soit un acide fort On a les réactions : ( ) |