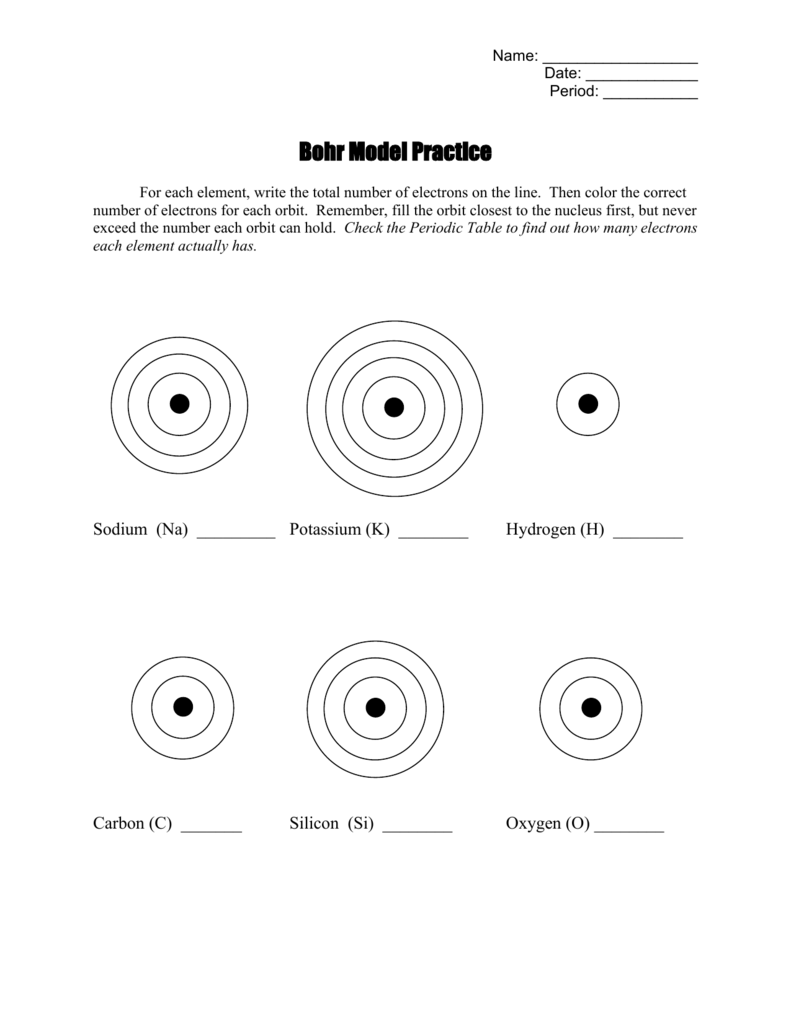
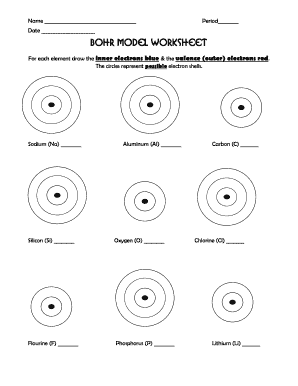
Modèle de Bohr
|
Modèle de Bohr (1913) - lcpmr
Modèle planétaire: l'électron décrit une trajectoire (orbite) circulaire -Quantification des niveaux d'énergie (Modèle de Bohr) Cours 2/3 -Le Photon |
|
CHAPITRE III : QUANTIFICATION DE LENERGIE
Le modèle de Bohr est une théorie physique cherchant à comprendre la constitution d'un atome et plus particulièrement celui de l'hydrogène et des ions |
|
Chimie Générale
%2520II%2520ET%2520III%2520Chimie%2520G%25C3%25A9n%25C3%25A9rale.%2520COURS%2520M%25C3%25A9deine%2520.pdf |
|
Chapitre 10: Atome de Bohr - ALlu
2 Modèle de Bohr : étude des orbites de l'atome H Avertissement ! Bien que le modèle ait permis de faire des calculs corrects pour l'atome d'hydrogène |
|
DL n 14 : Atome de Bohr
Ce modèle aujour- d'hui obsolète ne permit pas d'expliquer les spectres des autres atomes Une nouvelle physique fut nécessaire : la physique quan- tique |
|
Modèle de Bohr Objectif
Modèle de Bohr Objectif: - Trouver une expression de l'énergie de l'atome qui reproduise les spectres de raies expérimentaux Hypothèses: |
|
Niels Bohr le père de latome - BibNum
D'après ce modèle les électrons dans leur mouvement circulaire autour du noyau atomique devraient donc émettre un rayonnement perdre leur énergie et tomber |
|
TD N°3 Le Modèle de Bohr - lptms
Le Modèle de Bohr Niels Bohr 1885-1962 Prix Nobel en 1922 "pour son apport dans l'étude de la structure des atomes et des irradiations qui en émanent" |
|
LE MOD`ELE DE BOHR - solution
r Le moment cinétique est donc perpendiculaire au plan du mouvement, et sa composante selon z vaut L = rp = rmv Le mod`ele de Bohr donne donc la |
|
LE MOD`ELE DE BOHR
LE MOD`ELE DE BOHR Il a été découvert expérimentalement qu'un atome n' émet et n'absorbe de la lumi`ere qu'`a des fréquences bien définies Ceci ne peut |
|
DL n 14 : Atome de Bohr
Dans le mod`ele de Bohr, l'atome d'hydrog`ene est un syst`eme `a deux corps ponctuels constitué d'un noyau, le proton de masse mp et charge électrique +e, |
|
Mod`ele historique de Bohr de latome dhydrog` - cpge maroc
C o n c o u r s C o m m u n p o ly te c h n iq u e — -P h y s iq u e s p é c ifi q u e - M P - 2 0 1 8 – h ttp ://c p g e m a r o c c o m Concours Commun |
|
Introduction `a la mécanique quantique
4 3 Discussion critique du mod`ele de Bohr 24 4 4 Fonctions d'onde de l'électron dans l'atome d'hydrog`ene 25 5 L' équation |
|
1 De la mécanique classique `a la quantique
n1,n2 = 1, 2, 3, 4 (15) constante de Rydberg: RH = 109680 cm−1 (ν est un nombre d'onde ) Mod`ele de Bohr Hypoth`ese de Bohr quantification de L = mvr |
|
Physique Atomique Dr Taha Rouabah
Le mod`ele de Bohr est présenté en premier lieux pour l'étude de l'atome d' Hydrog`ene et des atomes `a un seul électron (atomes hydrogenoıde) Une ana- |
|
Cours de Physique du Solide 2020-2021 Matériaux & Ingénierie des
Le mod`ele de Rutherford (mouvement circulaire uniforme) donne un spectre continu et l'atome n'est pas stable Mod`ele de Bohr : • Mod`ele de Bohr |
|
Atome, mécanique quantique - Thomas Boyer-Kassem
Mod`ele de Bohr 1914 — Expérience de Franck et Hertz 1916 — Expériences de Millikan sur l'effet photo-électrique 1923 — Effet Compton 1924 — Théorie |