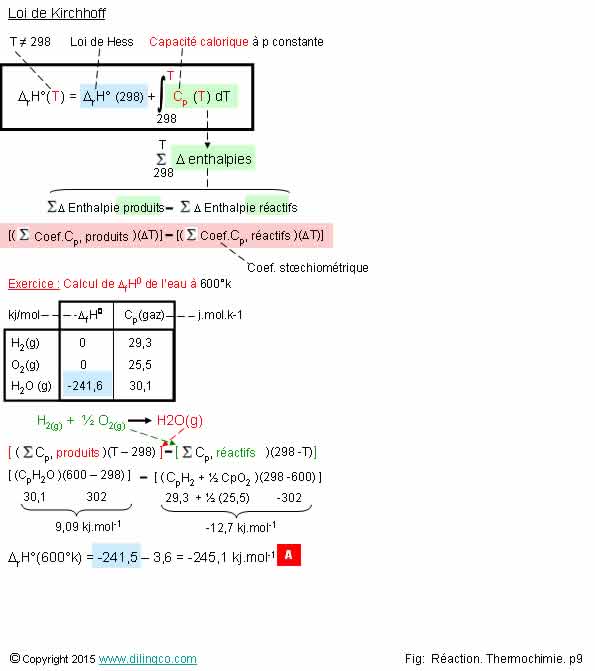
calculer l'enthalpie standard de réaction ? 298 k
Ce rapport, , la valeur de l'enthalpie de formation de l'O3(g) peut être utilisée comme un facteur de conversion pour trouver la chaleur produite lorsque 1 mole d'O3(g) est formée, ce qui est l'enthalpie de formation de l'O3 (g) : Par conséquent, ΔHf° [O3 (g) ] = + 143 kJ/mol.
Comment calculer ∆ G ?
ΔG = ΔG� + R.T.ln K
ΔG = variation de l'enthalpie (énergie) libre du système réactionnel, ΔG° = variation de l'enthalpie libre standard définie comme ci-dessus.
|
Exemples denthalpies standard
(298K) = -871.6 kJ/mol. • Réaction d'oxydo-réduction et calcul de l' enthalpie de formation de Cu2+ connaissant l'enthalpie de la réaction. |
|
Solutions de la série N°3 (exercice 34 et 5) (Thermodynamique)
Calculer l'enthalpie standard ?H°r298K de la réaction suivante : CO (g)+ 3H2(g) ? CH4(g) + H2O (l) a) En déduire la valeur de l'énergie interne ?U°r |
|
Universit du Maine
14 mars 2006 L'enthalpie standard de formation de l'ammoniac vaut à 298K : ?fH°(NH3) = -4619. kJ/mol. 1) Calculer l'énergie interne standard de la réaction ... |
|
THERMOCHIMIE Application du premier principe à la réaction
On se propose de calculer l'avancement lorsque 1mole de H2 a réagit On donne: Enthalpie standard de la réaction ?rH°298K = -570 |
|
Exercice 1 On considère la réaction du combustion du bore 2B (s) +
5- Calculer l'enthalpie standard de formation de C3H8 (g) à 298 K. Données : - Masses molaires (g.mol-1) : C : 12. H : 1. |
|
Chimie PCSI
Calculer la variation d'enthalpie ?H lors d'une transformation chimique à T L'enthalpie standard de réaction à 298 K vaut ?rH°(298K) = - 607 kJ.mol-1. |
|
Reaction chimique - Thermodynamique - Cinétique
Calculer ? sachant que la réaction est totale. Quel est le réactif limitant ? Les enthalpies molaires standard sont données dans les tables à 298K. |
|
Enthalpie libre Equilibres chimiques
II-1-Enthalpie libre standard de formation ?fG°T à pression atmosphérique et 298°K on a : ?rG°298 = + 164 kJ/mol >0. La réaction de formation de ... |
|
PC 2022 – 2023 Lycée La Martinière Monplaisir TC1 – Application
Exercice TC1-4 : Enthalpies standard de réaction (*). 1. Calculer les enthalpies standard des réactions suivantes à 298 K (après avoir attribué les bons. |
|
Chimie PCSI
Que valent les enthalpies standard de formation du magnésium Mg(s) et du dioxygène gazeux ? 2. Calculer l'enthalpie standard de la réaction à 298 K. La réaction |
|
Enthalpie de Formation Enthalpie de Formation Supplément
Calculer l'enthalpie standard de la réaction à 298K et 523K 2 La température de vaporisation du méthanol est de 337K Proposer un cycle thermodynamique, |
|
Thermodynamique de la transformation chimique - Frédéric Legrand
On dispose des enthalpies des réactions suivantes (à 298 K) : 298 K Pour calculer l'enthalpie standard d'une réaction chimique, il suffit de combiner les Écrivons la condition d'équilibre (appelée aussi loi d'action des masses), en mettant |
|
PREMIER PRINCIPE DE LA THERMODYNAMIQUE ENERGIE
d'état U IV 4 Transformation à pression constante : l'enthalpie, fonction d'état Calculer la variation de l'énergie interne standard de la réaction ΔrU°298K L' équation qui traduit la loi d'action de masse peut être généralisée aux systèmes |
|
Exercices : 15 - Thermochimie
Calculer l'enthalpie standard de réaction `a 125 ◦C Conclure La voie industrielle d'obtention du MTBE utilise l'action du méthanol sur l'isobut`ene température de 298 K, l'enthalpie libre standard de la réaction vaut −21 kJ · mol −1 1 |
|
Faculté des Sciences Meknès Cours THERMOCIMIE-EQUILIBRES
état normal à 25°C (298K) et sous P = 1 atm) est égal à zéro On peut calculer l' enthalpie standard de la réaction à partir des enthalpies standards Deux chimistes Guldberg et Waag ont établis une loi dite loi d'équilibre ou loi d'action de |
|
1/11 Données numériques : Masses molaires atomiques (en gmol
Enthalpie standard de vaporisation de l'acide éthanoïque à 298 K : 23,7 kJ mol Calculer l'enthalpie standard ainsi que l'entropie standard de la réaction de B- IV 3 1 L'acide barbiturique est préparé par action du malonate de diéthyle sur |
|
La thermodynamique chimique + les équilibres chimiques
2 2 1 Détermination des enthalpies molaires standard de réaction : loi de HESS 14 4 1 LOI D'ACTION DE MASSE OU LOI DE GULDBERG ET WAAGE Calculer la chaleur de combustion ∆H°r, 298K de l'acide oxalique solide (C 2 H 2 |