vitesse de réaction formule
C'est quoi la vitesse d'une réaction ?
La vitesse de réaction correspond à la variation de la quantité de réactifs ou de produits en fonction du temps.
Les vitesses de réactions sont l'objet d'étude de la cinétique chimique.Quelle est l'unité de la vitesse de réaction ?
pour une réaction de premier ordre, la constante de vitesse possède les unités s−1 ; pour une réaction de deuxième ordre, les unités sont L·mol−1·s−1 (ou M−1·s−1) ; et pour le troisième ordre, les unités sont L2·mol−2·s−1 (ou M−2·s−1).
Quelle est la loi de vitesse ?
En général, la loi de vitesse peut s'exprimer sous la forme d'un produit de deux fonctions : v = k .
- On peut déterminer la valeur de k en effectuant une même réaction à différentes températures.
On obtient ainsi une série de mesures rassemblant k = f(t).
La méthode des vitesses relatives permet de déterminer l'ordre de réaction par rapport à chacun des réactifs.
|
Loi de vitesse dune réaction chimique
Pour une réaction impliquant 2 réactifs A et B ; tel que aA + bB = Produits ; les mesures expérimentales ont montré que la vitesse de réaction est |
|
Cinétique chimique : introduction
s?1. Détermination graphique de la vitesse de réaction. La vitesse de réaction est la tangente en un point de la courbe |
|
Thème : Cinétique chimique Fiche 5 : Vitesse de réaction
Vitesse volumique de réaction v : dérivée par rapport au temps de demi réaction est une définition implicite |
|
Cinétique chimique
1.8 Expression d'une équation cinétique et d'une loi de vitesse intégrée. 2. Détermination de l'ordre d'une réaction. 2.1 Méthode intégrale; 2.2 Méthode du |
|
Génie de la Réaction Chimique: les réacteurs homogènes
14 juil. 2022 Vitesses de réaction chimique ... Exercice : QCU - Dépendance de la vitesse de réaction ... La formule d'itération est :. |
|
Cinétique chimique - vitesse de réaction
La cinétique chimique s'intéresse à l'évolution au cours du temps d'une réaction. I. Vitesse d'une réaction chimique. 1. Définition des vitesses. Vitesse de |
|
Reaction chimique - Thermodynamique - Cinétique
L'équation de la réaction chimique doit donc être équilibrée. C'est le gaz parfait associé (de même formule chimique) pur et sous la pression de ... |
|
Courbes courant-potentiel
Courant et vitesse de réaction; conventions de signe du courant Eeq donné par la formule de Nernst et dépendant des activités des espèces présentes et ... |
|
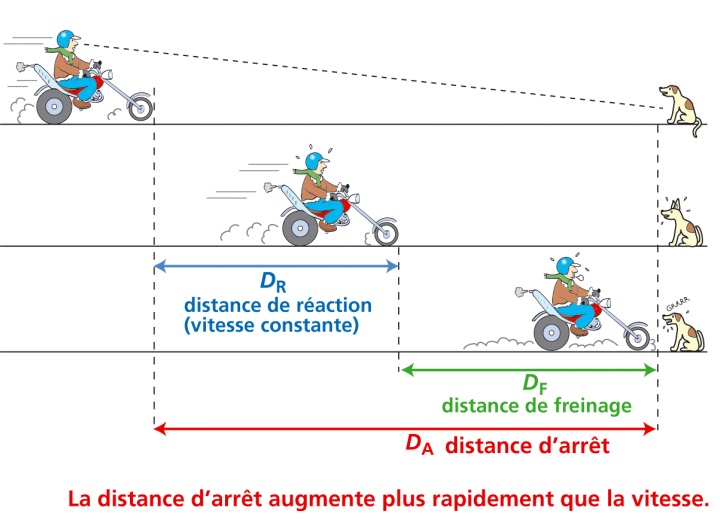
Vitesse et distance darrêt - Mathématiques 3e
fiches pédagogiques du livret : Vitesse et distance d'arrêt ; Réaction Utiliser une formule (vitesse). ... La distance de réaction est de 52 |
|
La chimie
Exemple: Écrivez l'expression de la vitesse de la réaction suivante: k est la constante de vitesse pour la réaction ... on peut modifier la formule. |
|
Thème : Cinétique chimique Fiche 5 : Vitesse de réaction - Studyrama
La vitesse de réaction augmente en général si la concentration d'un réactif augmente • La vitesse de réaction diminue globalement quand l'avancement augmente ( |
|
Cinétique chimique
1 7 Cinétique de réactions d'ordre 1 proches de l'équilibre On définit une vitesse de réaction unique: k = constante de vitesse de la réaction |
|
Loi de vitesse dune réaction chimique
Si on double la concentration d'un réactif la réaction est : - d'ordre 0 si on n'observe aucun effet sur la vitesse - d'ordre 1 si la vitesse double - d' |
|
Cinétique chimique : introduction
Cette vitesse volumique de réaction est toujours positive et ne dépend pas de l'espèce chimique Elle est exprimée en mol L?1 s?1 Détermination graphique de la |
|
Cinétique chimique - vitesse de réaction
La vitesse de formation d'un constituant chimique A est égale à la dérivée par rapport au temps de sa quantité de matière Sa vitesse de disparition est égale à |
|
La cinétique chimique - La chimie
les données suivantes déterminez la loi de vitesse et la constante de vitesse de cette réaction Expérience [A] initiale [B] initiale vitesse initiale (M/s) |
|
VITESSE DE RÉACTION
la situation à l'équilibre décrite par une constante thermodynamique d'équilibre K° que la thermodynamique permet de calculer • la vitesse avec laquelle le |
|
Chapitre 2 VITESSE DUNE REACTION CHIMIQUE Matheleve
Comparaison de la rapidité des transformations chimiques Vitesse moyenne d'une réaction chimique Vitesse instantanée d'une réaction chimique Autres |
|
Vitesse de réaction retour - Chimie au Triolet
À pression constante (système ouvert) on appelle vitesse de réaction « le nombre 3- Écris l'équation chimique de la réaction sachant que la formule du |
|
Chapitre 1 :Vitesses de réaction - Melusine
Chapitre 1 : Vitesses de réaction Cinétique chimique Page 1 sur 9 I Système œ réaction chimique A) Système physique ou chimique |
Comment calculer la vitesse de réaction ?
La vitesse moyenne de la réaction équivaut à déterminer graphiquement la valeur de la pente de la sécante coupant la courbe en deux endroits, alors que la vitesse instantanée est déterminée par la pente de la tangente qui passe par un point précis de la courbe.Quelle est l'expression de la vitesse générale de la réaction ?
Pour que la vitesse d'une réaction soit la même peu importe la substance choisie pour l'exprimer, on utilise la formule de la vitesse générale de réaction. Soit la réaction chimique suivante: N2(g)+3H2(g)?2NH3(g).Comment calculer constante de vitesse k ?
L'unité de la constante de vitesse k peut être déterminée par une analyse dimensionnelle (la dimension d'une grandeur se note entre crochets). Ainsi, [k] = T-1 (T : symbole dimensionnel d'un temps). Nous pouvons en déduire que, pour une réaction d'ordre global n = 1, l'unité usuelle de k est : s-1.- On peut déterminer la valeur de k en effectuant une même réaction à différentes températures. On obtient ainsi une série de mesures rassemblant k = f(t). La méthode des vitesses relatives permet de déterminer l'ordre de réaction par rapport à chacun des réactifs.
Comment calculer la vitesse d'une réaction chimique ?
C'est quoi la vitesse d'une réaction ?
Comment calculer la constante de vitesse de réaction ?
. L'unité de la constante de vitesse k peut être déterminée par une analyse dimensionnelle (la dimension d'une grandeur se note entre crochets).
. Ainsi, [k] = T-1 (T : symbole dimensionnel d'un temps).
. Nous pouvons en déduire que, pour une réaction d'ordre global n = 1, l'unité usuelle de k est : s-1.
Quelle est la loi de vitesse ?
|
Actions du vent sur les bâtiments selon lEurocode 1 - Educnet
10 mai 2014 · La vitesse de vent moyen vm (z) est nécessaire pour calculer le coefficient structural cscd La vitesse du vent est modifiée par : – la hauteur z (en |
|
COURS DE MÉCANIQUE - Jobs - SNCB
la somme de toutes les forces (forces d'action et forces de réaction) qui agit sur le Nous savons que la vitesse au sol est donnée par la formule : v = hg |
|
Aérodynamique (portance - traînée)
(Conso spécifiques : autonomie, rayon d'action) Finesse Newton (N) La portance d'un avion en vol à la vitesse de 360 km/h est de 24 000 Newtons et sa Utiliser la formule de meilleure pente de plané : Fin max = Cz / Cx ) Résolution : A |
|
Mécanique - matheuxovh
La vitesse instantanée est constante et elle peut se déterminer en calculant la pente du Une force est une grandeur vectorielle qui représente l'action qu'un b) Etablir la formule donnant le temps t que mettent les bulles pour remonter à la |
|
LAIR ET LAÉRAULIQUE
Vitesse moyenne et pressions 3 7 L'action du tirage Nous n'utiliserons ici que l'échelle Celsius, mais, dans les formules, le «degré» d'écart de température |
|
CALCULS PNEUMATIQUE ELEVE
La poussée théorique est déterminée à l'aide de la formule La vitesse du piston d'un vérin pneumatique est fonction de la résistance rencontrée, de la |
|
FORCE DUN VERIN VITESSE DE SORTIE VITESSE DE SORTIE
DEBIT NECESSAIRE avec D,d,t ts temps de sortie en seconde te temps d'entrée L course en mm Q = D L 21 220 ts sortie 2 Q = (D -d ) L 21 220 te entrée 2 |
|
PHYSIQUE DES FLUIDES
20 juil 2001 · intensité que son poids P dont l'action se répartit sur toute la surface S1 ou S2 ou S3 en contact de cette formule on tire la vitesse du piston |
|
CHAPITRE I : FORCES ET MOUVEMENTS
1) Détermination graphique de la vitesse moyenne et instantanée VI- La troisième loi : le principe des actions réciproques (action/réaction) |
























![PDF] Exercices d'électronique de puissance en PDF - électronique PDF] Exercices d'électronique de puissance en PDF - électronique](https://www.cours-gratuit.com/images/remos_downloads/detail/107/id-10796.10796.pdf-006.jpg)