ordre d'une réaction chimique
|
Cinétique chimique
Des réactions sont élémentaires lorsqu'elles s'effectuent sans étapes intermédiaires L'ordre par rapport à chaque réactif est alors égal au coefficient |
|
Loi de vitesse dune réaction chimique
Si on double la concentration d'un réactif la réaction est : - d'ordre 0 si on n'observe aucun effet sur la vitesse - d'ordre 1 si la vitesse double - d' |
Comment déterminer l'ordre d'une réaction ?
Trouvez quel est l'ordre d'une réaction quand la vitesse de celle-ci double si l'on multiplie par deux la concentration de l'un des réactifs.
Sachez que si l'on double la concentration d'un réactif et que cela multiplie par deux la vitesse de réaction, cela signifie que ce réactif est du premier ordre.Comment savoir si une réaction est d'ordre 0 1 ou 2 ?
Si on double la concentration d'un réactif, la réaction est : - d'ordre 0 si on n'observe aucun effet sur la vitesse - d'ordre 1 si la vitesse double - d'ordre 2 si la vitesse quadruple.
Lorsqu'on connaît l'ordre de réaction de chacun des réactifs, il devient possible de calculer la constante de vitesse k.C'est quoi une réaction d'ordre 2 ?
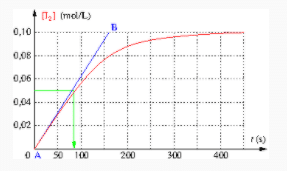
Pour une réaction d'ordre 2, le temps de demi-vie est donc inversement proportionnel à la concentration.
Voir figure ci-dessous : Le temps de demi-vie d'une réaction du second ordre est inversement proportionnel à la concentration du réactif.- Les réactions d'ordre 0 sont des réactions dont la vitesse ne dépend pas de la concentration des réactifs, la vitesse est donc constante.
|
Loi de vitesse dune réaction chimique
La constante de proportionnalité k est appelée constante de vitesse qui dépend de la température. Les exposants p et q sont les ordres partiels de réaction. |
|
Cinétique chimique
=ordres partiels / réactifs A et B. + =ordre global de la réaction. |
|
Reaction chimique - Thermodynamique - Cinétique
L'équation de la réaction chimique doit donc être équilibrée. On définit alors les coefficients Leur valeur est de l'ordre de quelques dizaines de. |
|
Génie de la Réaction Chimique: les réacteurs homogènes
14 lug 2022 III - Notions de base du Génie de la Réaction Chimique ... résolution d'une équation différentielle du premier ordre ; chimie : notions de ... |
|
La chimie
Exemple: La demi-vie d'une réaction d'ordre 1 est de 84.1 min. Calculez la constante de vitesse de la réaction. • Solution: 1. 4. 1. 3. |
|
Fiche de présentation et daccompagnement Niveau Terminale
améliorer la compréhension des réactions chimiques. une espèce colorée mais pour accéder à l'ordre de la réaction un certain nombre de calculs sont ... |
|
TP N° 2 Détermination expérimentale de lordre dune réaction I
La vitesse d'une réaction chimique est directement proportionnelle au produit des concentrations des réactifs. Soit la réaction élémentaire : A+B?C. Avec. V = |
|
Cinétique chimique
REACTION D'ORDRE 2. 4. DETERMINATION DES ORDRES PARTIELS : METHODE DE LA DEGENERESCENCE DE L'ORDRE OU. METHODE |
|
Détermination de lordre dune réaction
On souhaite déterminer les ordres partiels et la constante de vitesse k. Page 2. Cas où v = k.[A]p. Il existe plusieurs |
|
Cinétique chimique - vitesse de réaction
La vitesse de formation d'un constituant chimique A est égale à la dérivée par Une réaction admet un ordre si l'expérience montre qu'à une température ... |
|
Cinétique chimique
1 7 Cinétique de réactions d'ordre 1 proches de l'équilibre Lorsque l'équilibre chimique est atteint une réaction directe et sa réaction |
|
Détermination de lordre dune réaction
Détermination de l'ordre d'une réaction La vitesse d'une réaction s'exprime éventuellement en fonction des concentrations : ? des réactifs |
|
4 détermination expérimentale de lordre dune réaction
On peut déterminer un ordre global ou des ordres partiels en jouant sur les concentrations initiales — En introduisant les réactifs en proportion |
|
Loi de vitesse dune réaction chimique
Si on double la concentration d'un réactif la réaction est : - d'ordre 0 si on n'observe aucun effet sur la vitesse - d'ordre 1 si la vitesse double - d' |
|
La cinétique chimique - La chimie
la cinétique chimique s'intéresse à la vitesse à laquelle s'effectue les réactions chimiques • la vitesse de réaction est la variation de la concentration |
|
CINETIQUE CHIMIQU EE SPÉ MP
Le système - ou réacteur – est le siège d'une réaction chimique : cette dernière est Une réaction admet un ordre si l'expérience montre qu'à température |
|
Cinétique chimique - Chimie en PCSI
REACTION AVEC OU SANS ORDRE ; ORDRE PARTIEL ET GLOBAL -? ORDRE INITIAL ET COURANT 11 Etudier la vitesse d'une réaction chimique qui rend compte de la |
|
Cinétique chimique - Chimie en PCSI
Préciser les ordres partiels et l'ordre global de chacune des réactions suivantes Réaction chimique Loi de vitesse expérimentale Ordre partiel par |
|
Cours-Cinétique-chimiquepdf
La cinétique chimique est l'étude de la vitesse des réactions chimiques Les ordres de réaction ne sont pas nécessairement les coefficients |
|
CINETIQUE CHIMIQUE - KOUTOUBIA Prepas
II Ordre d'une réaction 1) Loi de Van't Hoff Van't Hoff a fait le raisonnement suivant : Soit une réaction totale : A+B ? C+D+ |
Quel est l'ordre de la réaction ?
On dit alors que la réaction admet un ordre et l'on appelle ordre de réaction la somme des exposants : ? = ? + ?. L'exposant ? est l'ordre partiel de la réaction par rapport à l'esp? A, ? est l'ordre partiel de la réaction par rapport à l'esp? B.Comment connaître l'ordre d'une réaction chimique ?
L'ordre global d'une réaction chimique correspond à la somme des ordres de chacun de ses réactifs. Vous n'avez donc qu'à faire le total des exposants de tous les réactifs pour trouver l'ordre de votre réaction chimique.C'est quoi une réaction d'ordre 1 ?
Pour une loi de vitesse d'ordre 1, la concentration d'un produit de réaction au cours du temps suit une exponentielle croissante partant de zéro et qui tend vers une valeur limite horizontale (doc. 1). La vitesse de formation du produit est une exponentielle décroissante qui tend vers zéro (doc. 2).- On peut donc vérifier qu'une réaction est d'ordre deux en s'assurant que sa vitesse est proportionnelle au carré de la concentration.
Comment déterminer l'ordre d'une réaction chimique ?
. Il existe deux manières de faire, soit tu passes par l'équation chimique si elle est simple soit tu utilises les concentrations et les vitesses de réaction pour trouver l'ordre.
Comment savoir si une réaction est d'ordre 0 1 ou 2 ?
C'est quoi une réaction d'ordre 1 ?
Comment savoir si une réaction est d'ordre 2 ?
|
Cinétique chimique - UNF3S
Savoir définir et déterminer l'ordre d'une réaction chimique, la dégénérescence de l'ordre – Loi empirique d'Arrhenius, énergie d'activation • Savoir exprimer et |
|
Cinétique chimique - Chimie en PCSI
REACTION AVEC OU SANS ORDRE ; ORDRE PARTIEL ET GLOBAL -‐ ORDRE très générale, la cinétique chimique est l'étude de la vitesse des réactions |
|
Cinétique chimique - Chimie en PCSI
REACTION D'ORDRE 2 4 DETERMINATION DES ORDRES PARTIELS : METHODE DE LA DEGENERESCENCE DE L'ORDRE, OU METHODE |
|
Cinétique chimique
, =ordres partiels / réactifs A et B + =ordre global de la réaction , peuvent être entiers, fractionnaires ou nuls Cette loi fut proposée par van t 'Hoff |
|
2007
La vitesse d'une réaction chimique est la variation de concentration d'un produit en Avec la constante de vitesse k, x et y sont les ordres partiels de la réaction |
|
Cours de chimie g´en´erale Pr´eparation au concours B - u-psudfr
I 1 3 Ordre d'une réaction Définition Souvent, la vitesse volumique d'une réaction réaction chimique dépend de la concentration des réactifs Dans certains cas |
|
Cinétique chimique - Lycée dAdultes
Suivi expérimental de la vitesse de réaction et temps de demi-réaction • Loi de vitesse d'une réaction d'ordre 1 (Vidéo3) 1 1 Facteurs cinétiques et catalyse |
|
Etude de quelques réactions dordre simple
c) Etude expérimentale d'une réaction d'ordre 1 Par un dosage on parvient à déterminer l'évolution de la concentration en espèce chimique a en fonction du |