acide fort ou acide faible
|
Fiche de révisions sur les acides et les bases
HN est un acide faible ! acide : espèce chimique capable de libérer un (ou plusieurs) proton (s) base : espèce chimique capable de capter |
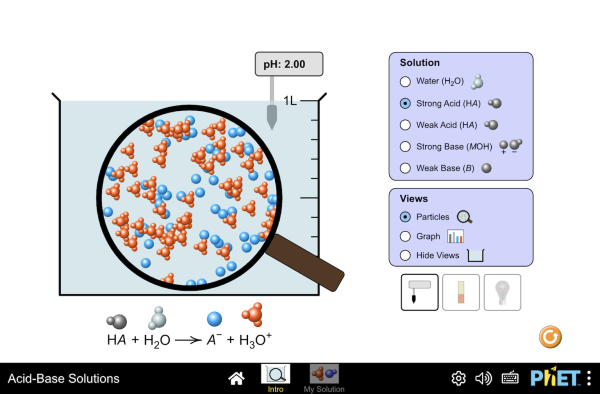
Comment savoir si on a un acide fort ou faible ?
On peut savoir si on a un acide fort ou faible à partir de sa dissociation : S'il se dissocie totalement en solution, il s'agit d'un acide fort.
S'il ne se dissocie que partiellement, il est considéré comme un acide faible.L'acide méthanoïque (L'acide méthanoïque (appelé aussi acide formique) est le plus simple des acides), l'acide éthanoïque et les autres acides carboxyliques sont des acides faibles.
Quel sont les acides forts ?
Parmi les acides forts, on trouve :
l'acide chlorhydrique, solution aqueuse du chlorure d'hydrogène. l'acide sulfurique. l'acide nitrique. l'acide iodhydrique, solution aqueuse de l'iodure d'hydrogène ;l'acide bromhydrique, solution aqueuse du bromure d'hydrogène ;l'acide perchlorique ;l'acide chlorique ;Comment savoir quel acide est le plus fort ?
Ainsi, les acides plus forts auront une constante d'acidité plus grande.
On peut alors dire que lorsque la force de l'acide augmente, la constante d'acidité augmente également.
Donc, pour identifier l'acide qui est le plus fort, nous devons identifier l'acide qui a la plus grande valeur de �� ��.
|
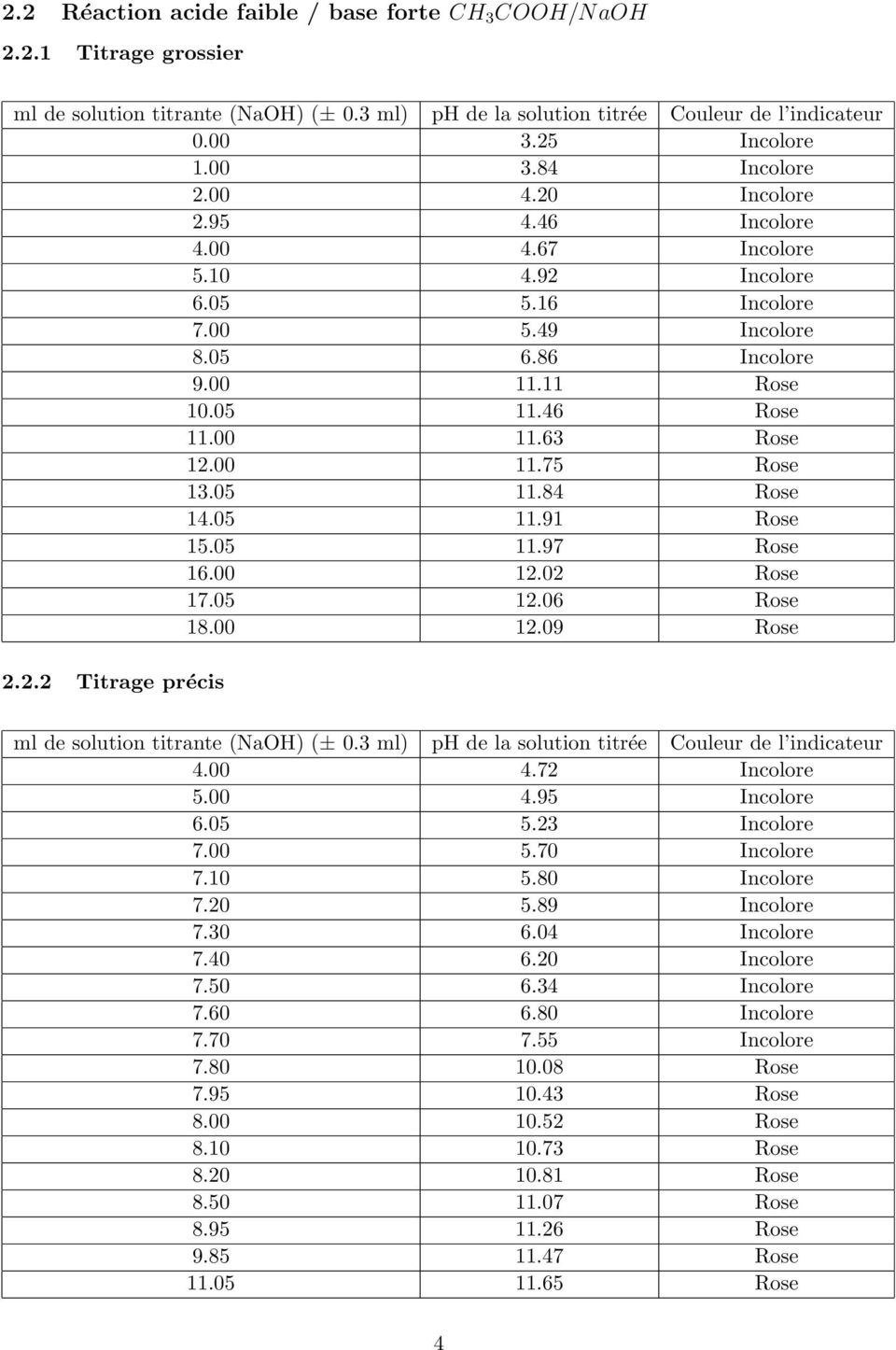
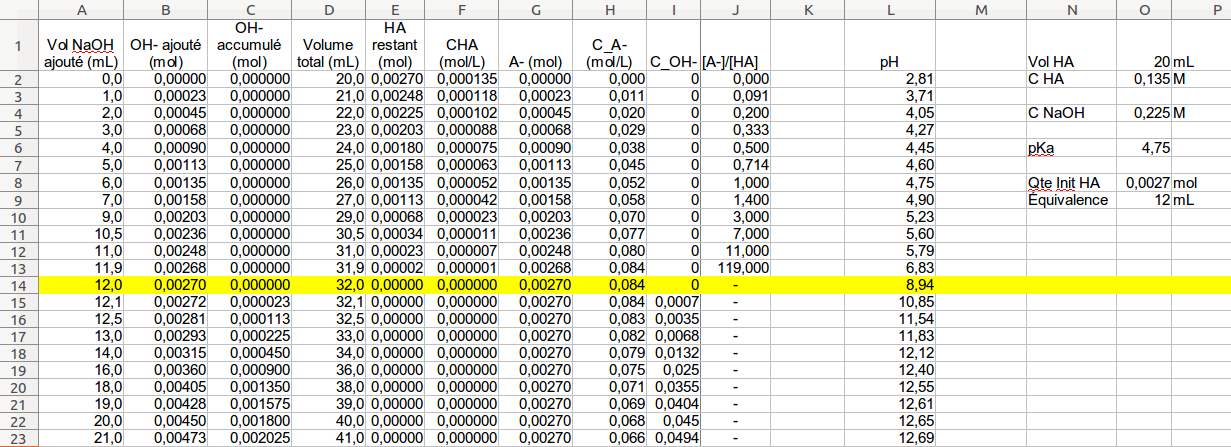
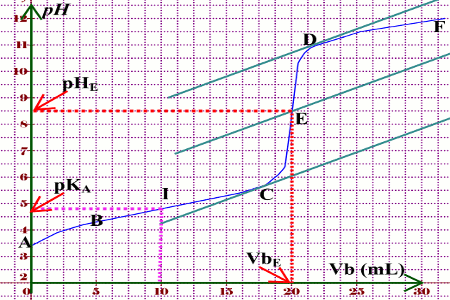
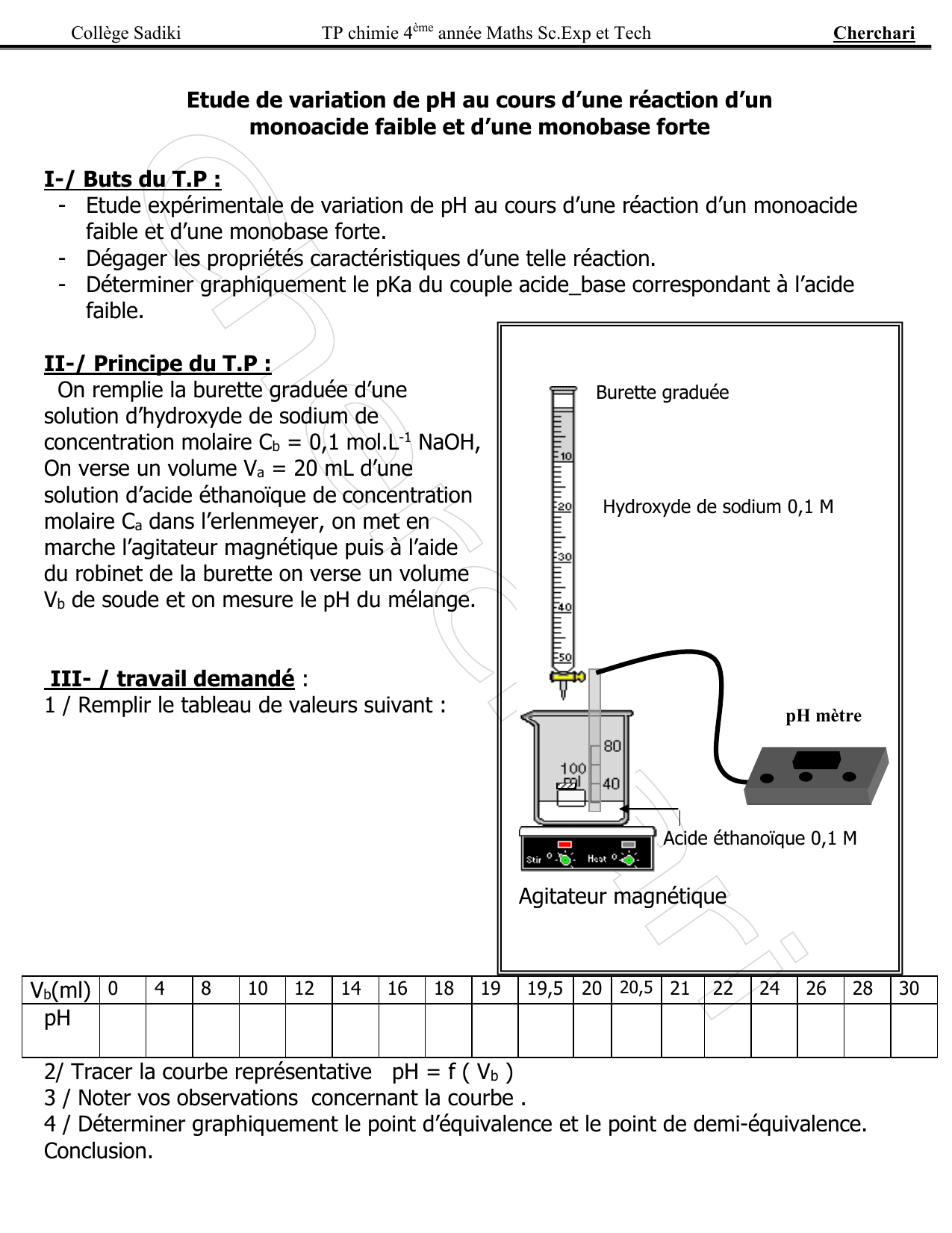
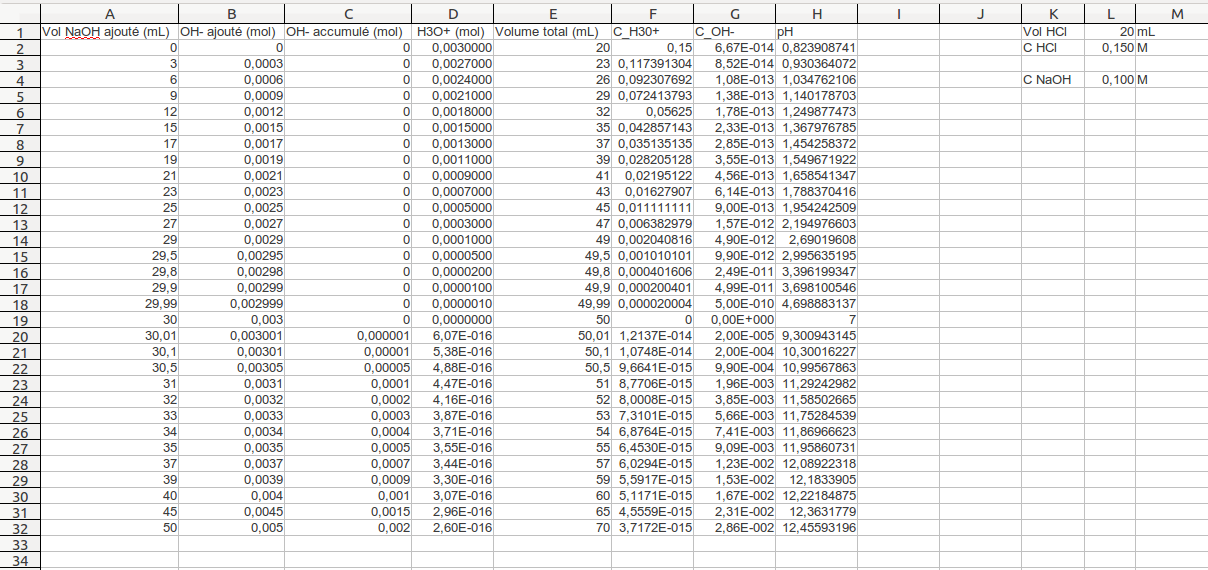
§ 7 (suite) Titrages acide-base
Considérons le titrage d'une solution d'un acide faible tel que l'acide acétique par exemple |
|
Fiche de révisions sur les acides et les bases
donc la base la plus forte dans l'eau. Les couples acide faible / base faible ont tous des constantes d'acidité comprises entre 1 et. 14. 10. |
|
Chapitre 1 Acides et bases
L'acide conjugué d'une base faible est un acide faible. Exemples : 1) L — définition d'un acide fort/faible d'une base forte/faible;. — propriétés d ... |
|
Acide phosphorique
L'acide phosphorique est un triacide minéral. La première fonction est celle d'un acide fort la deuxième celle d'un acide faible et la troisième celle d'un |
|
VI..Etude sommaire des mélanges
2) Acide fort 1 + acide faible 2. On calcule souvent le pH en négligeant l En solution aqueuse les acides forts fournissent intégralement l'acide fort. H3O. |
|
Fiche de synthèse n°2 : réactions acido-basiques en solution aqueuse
Dans le cas d'un acide fort celui-ci étant totalement dissocié dans l'eau |
|
7. Transferts de protons Equilibres acide-base
Les acides faibles fournissent en solution aqueuse une concentration d'ions H3O+ inférieure à celle que fournissent les acides forts à la même concentration |
|
Chapitre n°…. : Notion dacides et de bases fortes et faibles TP n
-Identifier le caractère fort ou faible d'un acide. -Calculer une incertitude. Contexte du sujet: Nous désirons vérifier expérimentalement que l'acide |
|
PHYSIOLOGIE DE LEQUILIBRE ET DU DESEQUILIBRE
couple sera très efficace pour lutter contre les acides forts. De l'association d'une base faible et d'un sel de cette base par un acide fort et dans ce cas |
|
Déterminer si un acide est fort ou faible
Un acide est fort s'il de dissocie totalement lors de sa mise en solution. On a alors la relation. [H3O+]=C. • Un acide est faible s'il se dissocie |
|
Déterminer si un acide est fort ou faible
On connait le pH et la concentration de la solution. Pour savoir si l'acide est fort ou faible il faut : 1. Déterminer [H3O+] par la relation [H3O+]=10- |
|
COURS DE CHIMIE GENERALE Semestre 1 SVI
Cas d'un mélange d'un acide fort et d'un acide faible. Page 4. 3. 2.6. Cas d'un mélange de deux acides faibles. |
|
§ 7 (suite) Titrages acide-base
Considérons le titrage d'une solution d'un acide faible tel que l'acide acétique par exemple |
|
VI..Etude sommaire des mélanges
l'acide faible possède une constante d'acidité et une concentration assez faibles) La réaction entre un acide fort et une base faible est complète si la. |
|
Fiche de révisions sur les acides et les bases
donc la base la plus forte dans l'eau. Les couples acide faible / base faible ont tous des constantes d'acidité comprises entre 1 et. 14. 10. |
|
Acide phosphorique
L'acide phosphorique est un triacide minéral. La première fonction est celle d'un acide fort la deuxième celle d'un acide faible et la troisième celle d'un |
|
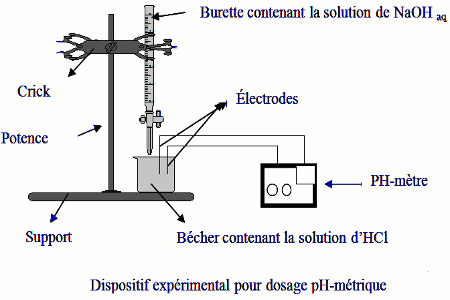
Dosage acide faible-base forte
Dosage acide faible – base forte. Les relations établies classiquement le sont pour : ? un acide suffisamment faible et pas trop dilué. |
|
Fiche de synthèse n°2 : réactions acido-basiques en solution aqueuse
Soit un acide faible AH qui réagit avec l'eau selon la réaction d'équation : Dans le cas d'un acide fort celui-ci étant totalement dissocié dans l'eau |
|
Dosage acide faible – base forte
Dosage acide faible – base forte. Les relations établies classiquement le sont pour : ? un acide suffisamment faible et pas trop dilué. |
|
7. Transferts de protons Equilibres acide-base
Les acides faibles fournissent en solution aqueuse une concentration d'ions H3O+ inférieure à celle que fournissent les acides forts à la même concentration |
|
Révisions sur les acides et les bases - Nicole Cortial
donc la base la plus forte, dans l'eau Les couples acide faible / base faible ont tous des constantes d'acidité comprises entre 1 et 14 10 |
|
COURS DE CHIMIE GENERALE Semestre 1 SVI - Université Cadi
CALCUL DE PH DES SOLUTIONS AQUEUSES 2 1 Cas d'un acide fort 2 2 Cas d'un acide faible 2 3 Cas d'une base forte 2 4 |
|
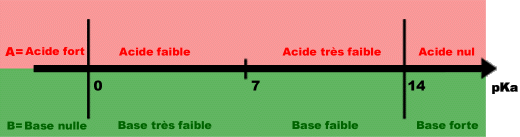
PH et pKa - Eli Zysman-Colman
pKa = -log Ka Plus la valeur de pKa est faible, plus le Ka est grand, plus l'acide est fort 4 Table de pKa http://evans harvard edu/ pdf /evans_pKa_table pdf |
|
VIEtude sommaire des mélanges
2) Acide fort 1 + acide faible 2 On calcule souvent le pH en négligeant l'acide faible Cette approximation grossière n'est justifiée que si l'apport d'ions |
|
Chapitre 1 Acides et bases
faible ssi la dissociation est une réaction équilibrée ssi pKa > 0 Dans le cas d'un acide fort, totalement dissocié dans l'eau, la concentration finale |
|
Transformations chimiques en solution aqueuse - Chimie en PCSI
7 II – LA REACTION ACIDE/BASE 8 1 LES ACIDES FORTS ET LES BASES FORTES 8 2 LES ACIDES FAIBLES ET LES BASES FAIBLES : CONSTANTE |
|
Les acides et bases en solution aqueuse - Groupe Transition
Coefficient d'ionisation (de dissociation) d'un acide ou d'une base faible Pourcentage effet, HCl est un acide fort totalement ionisé en solution aqueuse |
|
Propriétés des acides et des bases
•pKa faible « Ka élevé : acide fort •pKa élevé « Ka faible : acide Les acides faibles en solution aqueuse se dissocient seulement partiellement, la majorité des |
|
Dosage acide faible – base forte
1 Dosage acide faible – base forte Les relations établies classiquement le sont pour : ▫ un acide suffisamment faible et pas trop dilué, ▫ ou un acide pas trop |