acide fort pka
|
Chapitre 1 Acides et bases
Un acide est dit : — fort dans l'eau ssi il est totalement dissocié dans l'eau ssi Ka > 1 ssi pKa < 0; — faible ssi la dissociation est une réaction équilibrée |
|
Réactions acido-basiques en solution aqueuse
α est une grandeur comprise entre 0 et 1 Α = 1 correspond à un acide totalement dissocié donc fort Exemple : Pour un acide faible de pKa = 5 et C0 = 10- |
|
PH et pKa
Constante d'acidité pKa = -log Ka Plus la valeur de pKa est faible plus le Ka est grand plus l'acide est fort 4 Table de pKa http://evans harvard edu/ pdf |
Comment savoir si un acide est fort ou faible avec pKa ?
Le pKa, quant à lui, est une constante d'acidité qui révèle la tendance d'une molécule à libérer un proton (H+) dans une solution.
Plus le pKa est bas, plus l'acide est fort, car il a une forte propension à libérer des protons.Quel est le pH d'un acide fort ?
Un acide fort est un acide dont la réaction d'hydrolyse est totale : l'acide AH est complétement dissocié dans l'eau.
Base forte : Une base forte est une base dont la réaction d'hydrolyse est totale.
La flèche simple « → » indique que la réaction chimique est totale, elle ne peut s'effectuer que dans un seul sens.Comment interpréter le pKa ?
Pour interpréter le pKa : Si le pKa est près de zéro, la substance est acide.
Si le pKa est près de 14, la substance est basique.
|
§ 7 (suite) Titrages acide-base
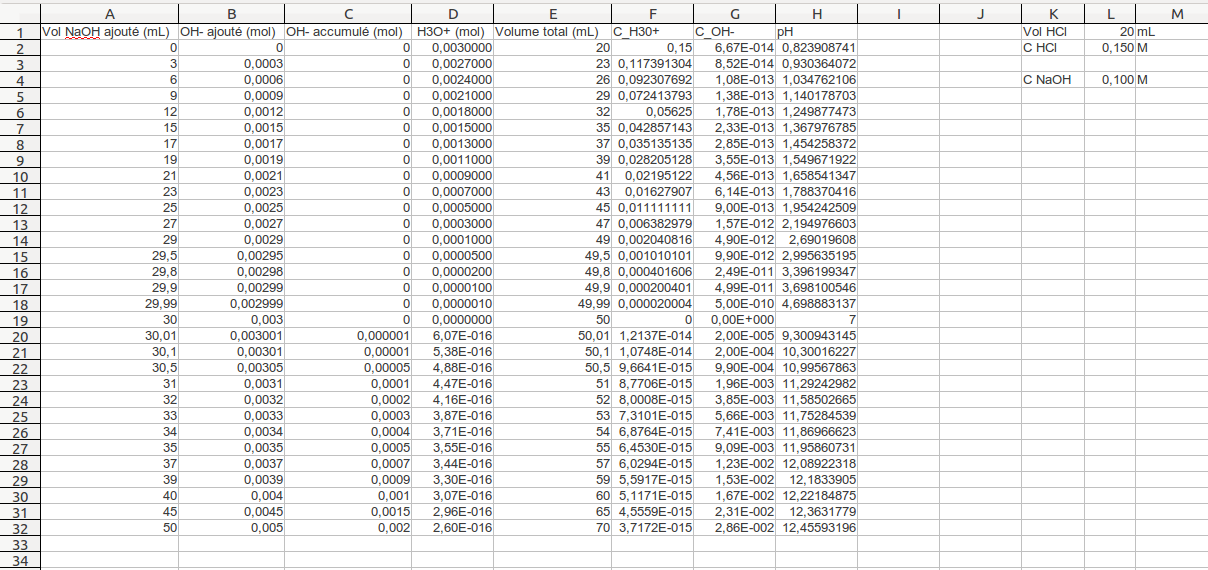
A titre d'exemple considérons le titrage d'une solution d'acide carbonique H2CO3 de concentration ca = 0.1 M par une base forte |
|
PH et pKa
Plus la valeur de pKa est faible plus le Ka est grand |
|
§ 7 (suite) Calcul du pH de solutions
Si la concentration d'un acide faible HA ou d'une base faible B en solution est suffisamment grande et leur pKa ou pKb également suffisamment grand |
|
Chapitre 1 Acides et bases
faible ssi la dissociation est une réaction équilibrée ssi pKa > 0. Dans le cas d'un acide fort totalement dissocié dans l'eau |
|
Fiche de synthèse n°2 : réactions acido-basiques en solution aqueuse
Lien entre le pH et le pKa d'un couple. Le pH d'une solution contenant un acide faible AH et sa base conjuguée A? est lié au pKa du couple AH/A?par la |
|
7. Transferts de protons Equilibres acide-base
HCl est un acide fort. Son hydrolyse (réaction avec Plus un acide sera fort plus la valeur de Ka sera élevée et plus celle de pKa sera faible. |
|
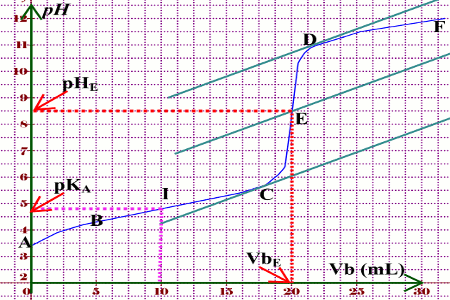
Dosage acide faible – base forte
un acide suffisamment faible et pas trop dilué Acide faible HA : constante d'acidité Ka ... dosage d'un acide faible (pKa=3 |
|
Untitled
Une solution aqueuse saturée d'acide sulfhydrique H?S (aq) de concentration analytique l'acide faible conjugué: pH = '/2 (pka-logca). PH = 05.9 |
|
Physique-chimie
Cette situation se retrouve pour des acides appartenant à des couples de pKa négatifs. Ces acides sont qualifiés de forts. Un acide est dit fort si la |
|
PH et pKa - Eli Zysman-Colman
pKa = -log Ka Plus la valeur de pKa est faible, plus le Ka est grand, plus l'acide est fort 4 Table de pKa http://evans harvard edu/ pdf /evans_pKa_table pdf |
|
Chapitre 1 Acides et bases
faible ssi la dissociation est une réaction équilibrée ssi pKa > 0 Dans le cas d'un acide fort, totalement dissocié dans l'eau, la concentration finale |
|
Propriétés des acides et des bases
contraires : •pKa faible « Ka élevé : acide fort •pKa élevé « Ka faible : acide faible Les acides forts en solution aqueuse se dissocient complètement Acide fort |
|
Force des acides et des bases - Lycée dAdultes
Inversement, plus le pKA d'un couple est faible (ou sa constante KA forte), plus l' acide est fort et la base faible Figure 4 4 – Échelle de constante d'acidité et de |
|
§ 7 (suite) Calcul du pH de solutions - EPFL
Si la concentration d'un acide faible HA ou d'une base faible B en solution est suffisamment grande et leur pKa ou pKb également suffisamment grand, |
|
§ 7 (suite) Titrages acide-base - EPFL
Un indicateur est un acide faible dont la forme acide HIn est caractérisé par une pH = pKa HIn + H2O In– + H3O+ Ka = [In–]⋅[H3O+] / ( [HIn]⋅c0 ) Exemple |
|
COURS DE CHIMIE GENERALE Semestre 1 SVI - Université Cadi
2 5 Cas d'un mélange d'un acide fort et d'un acide faible Constantes d'acidité et pKa des couples acide/base usuels, en solution aqueuse, à 25°C Acide |
|
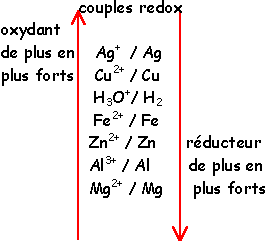
Révisions sur les acides et les bases - Nicole Cortial
Exemples de réactions de dissolution de bases et d'acides forts : • L'acide pKA H3O + H2 O H2 O OH - KA Bases de plus en plus fortes Acides de plus en |