la calorimetrie
|
La calorimétrie et ses applications actuelles
Ceci nous amène à préférer définir aujourd'hui la calorimétrie comme la mesure de l'énergie thermique produite ou absorbée par un système Quels sont les |
Quel est le principe de la calorimétrie ?
La calorimétrie est science qui s'occupe des mesures des quantités de chaleur.
Elle repose sur le principe de l'égalité des échanges de chaleur : lorsque deux corps n'échange que de la chaleur, la quantité de chaleur gagnée par l'un est égale à celle perdue par l'autre (en valeur absolue).Comment calculer la calorimétrie ?
Appliquons alors la relation de calorimétrie:∑ Qi = 0.
Q1 + Q2 + Q3 + Q4 = 0 .
La mesure de te, permet de déterminer la chaleur Latente de fusion de la glace L(fus).Quel est le but de la calorimétrie ?
La calorimétrie est une méthode permettant de mesurer le changement d'enthalpie d'une réaction en mesurant le changement de température que la réaction provoque.
Le changement d'enthalpie est le changement de chaleur d'une réaction à pression constante.- La calorimétrie est une technique qui consiste à réaliser une transformation dans un système adiabatique et à mesurer les variations de température qui accompagnent cette transformation.
De ces variations de température, on peut déduire les chaleurs de réaction associées à la transformation.
|
La calorimétrie et ses applications actuelles
Le terme calorimètre proposé par Lavoisier dans son Traité élémentaire de chimie (1789 |
|
Plan Principes de la calorimétrie Calorimétrie électromagnétique (1/4)
Calorimétrie. VII. Electronique et système d'acquisition. VIII.Détecteurs de physique des hautes énergie. P. Puzo / 2007-2008. |
|
Calorimétrie
avoisier et Berthelot : deux grands noms de la chimie que nous associons immanquablement |
|
Thermodynamique - Calorimétrie
(m: masse du corps ; C : capacité calorifique et c : chaleur massique). Page 3. 3. • Valeur en eau du calorimètre (ou masse en eau) « ? » : C'est la masse d'eau |
|
La calorimétrie des procédés et de la sécurité
Mots-clés Calorimétrie d'adsorption chimique des gaz catalyseurs métalliques |
|
1) Principes de la calorimétrie 2) Calorimètre 3) La sonde
- La méthode des mélanges: Le transfert thermique à mesurer échauffe une masse d'eau déterminée. 2) Calorimètre. Les expériences ont lieu dans une enceinte |
|
La calorimétrie indirecte : un outil précis trop peu utilisé
12 fév. 2012 Mots clés Calorimétrie indirecte · Dépense énergétique ·. Calories · Soins intensifs. Abstract Indirect calorimetry is recognized as the ... |
|
La calorimétrie et la santé
calorimétrie. Résumé. Cet article illustre l'apport de la titration calorimétrique isotherme (ITC) de l'analyse calorimétrique différentielle. |
|
Relation fondamentale de la calorimétrie
Page 1. 1. Page 2. 2. Page 3. 3. Page 4. 4. |
|
Calorimétrie
ment suivie par calorimétrie. En effet en considérant que l'énergie thermique mesurée est proportionnelle au taux de réticulation (ou de conversion) |
|
3 Calorimétrie F2School
La calorimétrie est la partie de la thermodynamique qui a pour objet la mesure des quantités de chaleur Ce sont p ex les quantités de chaleur nécessaires |
|
IPSA cours de physique II CALORIMETRIE + DILATATION 2014
Le calorimètre constitue un système thermodynamique isolé il n'y a donc pas d'échange de matière et d'énergie (travail ou chaleur) avec le milieu extérieur |
|
Calorimetriepdf - Faculté des Sciences de Rabat
Toute mesure d'un effet thermique par calorimétrie quel que soit le protocole expérimental choisi nécessite un étalonnage du calorimètre (détermination de ?) |
|
La calorimétrie et ses applications actuelles
Ceci nous amène à préférer définir aujourd'hui la calorimétrie comme la mesure de l'énergie thermique produite ou absorbée par un système Quels sont les |
|
Relation fondamentale de la calorimétrie
Page 1 1 Page 2 2 Page 3 3 Page 4 4 |
|
CALORIMETRIE
CALORIMÉTRIE I : NOTION DE QUANTITÉ DE CHALEUR Soient deux même quantités d'eau à la même température t1 Chauffons l'une des deux avec un |
|
Calorimètre - CONATEXcom
Calorimètre Description Permet de déterminer la capacité calorifique de corps solides et liquides d'étudier la relation |
|
Calorimétrie - Cours 5 pdf - ALLO ACADEMY
Calorimétrie Physique Cours Résumé Exercices corrigés Examens corrigés Travaux dirigés td Travaux pratiques TP Devoirs Contrôle pdf |
|
Calorimétrie
7 Calculer la chaleur de combustion du carbone sachant qu'en brûlant 3 g de carbone dans un calorimètre en cuivre de 1500 kg rempli de 2000 kg d'eau |
|
Thermodynamique - Calorimétrie
(m: masse du corps ; C : capacité calorifique et c : chaleur massique) Page 3 3 • Valeur en eau du calorimètre (ou masse en eau) « ? » : C'est la masse d'eau |
| Quelques notions élémentaires sur la calorimétrie - Cortial |
| Quelques notions élémentaires sur la calorimétrie - Cortial |
| Mesures calorimétriques : méthode des mélanges - Cortial |
| TP de thermodynamique n°1 : Calorimétrie - F2School |
| La calorimétrie Partie I - Institut national de physique |
|
TP 12 : Calorimétrie
23 sept 2009 · Faire un dernier graphe avec ces capacités calorifiques totales en fonction de la masse d'eau Page 3 Groupe 9 TP 12 : Calorimétrie 23 9 2009 |
|
TP de thermodynamique n°1 : Calorimétrie - PCSI-PSI AUX ULIS
En déduire µ la valeur en eau du calorimètre V - Détermination de la capacité thermique massique d'un solide On dispose plusieurs types de solides : du |
|
1) Principes de la calorimétrie 2) Calorimètre
calorimétrie est la partie de la thermodynamique qui consiste à mesurer les On définit la valeur en eau μ du calorimètre comme la masse d'eau fictive qu'il |
|
Calorimétrie quasi adiabatique pour bétons : facteurs d - Ifsttar
Ce calorimètre et sa méthode d'essai ont été mis au point car les tentatives pour déduire la chaleur dégagée dans le béton à partir d'essais sur pâtes de ciment ou |
|
La calorimetrie
Cours de Physique II Calorimétrie-Dilatation 2014-2015 3/26 Chapitre un : Notion de quantité de chaleur 1 1 Température 1 1 1 Equilibre thermique 1 1 2 |
|
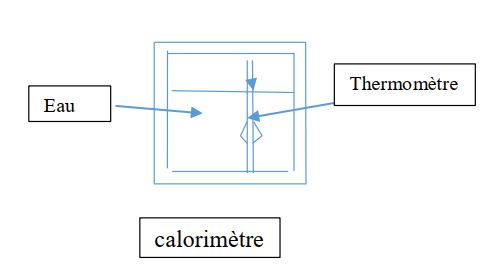
Chapitre 6 :Capacités thermiques, calorimétrie
Chapitre 6 : Capacités thermiques, calorimétrie Thermodynamique Page 1 sur 5 I Enthalpie, capacité thermique isobare A) Enthalpie Pour un système qui |






















![Exercice Calorimétrie 2 - [PDF Document] Exercice Calorimétrie 2 - [PDF Document]](https://www.mt.com/ca/fr/home/products/L1_AutochemProducts/Reaction-Calorimeters-RC1-HFCal/_jcr_content/productlinetabs/overviewpltoppar/standalonemoodimage__0/image.webImage.file.png)