tp dilution
|
Protocole pour réaliser une dilution
On dispose d'une solution mère de concentration Cmère = 5 mol L-1 On désire fabriquer un volume Vfille = 50 mL d'une solution de concentration Cfille = 2 |
|
Santé-TP n°7 : Préparation dune solution Dilution
Santé-TP n°7 : Préparation d'une solution Dilution Page 2 Voir protocole expérimental fourni sur la paillasse Questions 1-Par simple observation à l'œil |
|
TP C6 Dilution
Objectifs : - Déterminer la valeur d'une concentration en masse à l'aide d'une gamme d'étalonnage (mesure de masse volumique) |
|
TP N° 2 : Préparation dune solution par dissolution ou par dilution
Diluer 10 fois une solution revient à diviser sa concentration par 10 la diluer 100 fois revient à diviser sa concentration par 100 On parle aussi de dilution |
|
TP n°9 de chimie : Préparation dune solution par dilution
Une dilution est une technique de préparation de solution (appelée solution fille) par ajout de solvant dans une première solution (appelée solution mère) |
|
TP verrerie /dissolution / dilution
TP verrerie /dissolution / dilution Documents joints : - TP - Fiches RN chimie - Sécurités + pictogrammes - Fiche verrerie • Pré-requis : - La quantité de |
|
TP-Préparation dune solution de concentration donnée par dilution
TP-Préparation d'une solution de concentration donnée par dilution Objectifs : -Connaître le principe d'une dilution -Réaliser des dilutions successives 1 |
|
TP-Préparation dune solution par dilution
TP-Préparation d'une solution par dilution Objectifs : -savoir utiliser et connaître le matériel adapté à une dilution -savoir calculer la concentration |
Comment faire une dilution en TP ?
Réaliser une dilution consiste à diminuer la concentration molaire d'une solution en ajoutant de l'eau (le solvant).
La solution initiale utilisée est appelée la solution mère.
Le volume prélevé de la solution mère sera noté Vi et sa concentration molaire Ci.
La solution finale préparée est appelée la solution fille.C'est quoi diluer 10 fois ?
Diluer 10 fois une solution revient à diviser sa concentration par 10, la diluer 100 fois revient à diviser sa concentration par 100.
On parle aussi de dilution au dixième, au centième. 10 et 100 représente le facteur de dilution.Comment utiliser la formule de dilution ?
La dilution
1La dilution est un procédé utilisé pour diminuer la concentration d'une solution en y ajoutant du solvant sans changer la quantité de soluté.
2) Pour faire une solution d'eau salée deux fois moins concentrée que la solution initiale, il faut doubler la quantité de solution en ajoutant du solvant.
3) C1⋅V1=C2⋅V2.- On appelle cela une dilution au dixième.
Dans ce cas, il est possible d'effectuer le calcul de volume V0 à prélever de la solution mère plus rapidement : pour 100 mL de solution fille à obtenir, il faut prélever V0 = 10 mL de solution mère, soit 10 fois moins.
Ce calcul est valable pour tous les facteurs de dilution.
|
Santé-TP n°7 : Préparation dune solution. Dilution
Il souhaite la diluer pour obtenir un volume V1 = 100 mL d'une solution S1 de concentration massique : cm1 = 5 |
|
TP-Préparation dune solution de concentration donnée par dilution.
TP-Préparation d'une solution -Réaliser des dilutions successives. ... Réaliser une dilution consiste à diminuer la concentration molaire d'une solution ... |
|
TP N° 2 : Préparation dune solution par dissolution ou par dilution.
Diluer 10 fois une solution revient à diviser sa concentration par 10 la diluer 100 fois revient à diviser sa concentration par 100. On parle aussi de dilution |
|
TP Chimie n° 3
- Savoir calculer la concentration molaire la masse volumique et le facteur de dilution de la solution obtenue. 2 Présentation. On dispose d'une solution mère |
|
TP C6 Dilution
TP C6. Dilution. NOMS : Chapitre 2C. Livre page 38. Objectifs : - Déterminer la valeur d'une concentration en masse à l'aide d'une gamme d'étalonnage ( |
|
TP : Dosage du vinaigre
dilution au 1/10ème du vinaigre commercial. Cette solution diluée sera notée SA. 2) Dosage par la solution d'hydroxyde de sodium : Dans un bécher de 100 mL |
|
TP-Préparation dune solution par dilution
Objectifs : -savoir utiliser et connaître le matériel adapté à une dilution. -savoir calculer la concentration molaire de la solution obtenue. 1-Préparation d' |
|
TP CHIMIE-1 & TP CHIMIE-2
TP II : Le dosage acido-basique (cas d'un acide fort par une base forte) . Figure I-8 : Schéma explicatif sur la méthode indirecte (par dilution). |
|
Protocole pour réaliser une dilution
On dispose d'une solution mère de concentration Cmère = 5 mol.L-1. On désire fabriquer un volume. Vfille = 50 mL d'une solution de concentration Cfille = 2 |
|
TP Chimie I
TP-N°03. PREPARATION de SOLUTIONS AQUEUSES. Par DISSOLUTION et DILUTION A la fin du TP vider tous les récipients |
|
TP-Préparation dune solution de concentration donnée par dilution
TP-Préparation d'une solution de concentration donnée par dilution Objectifs : -Connaître le principe d'une dilution -Réaliser des dilutions successives |
|
Santé-TP n°7 : Préparation dune solution Dilution
Diluer une solution c'est ajouter du solvant pour obtenir une solution moins concentrée 3-En vous aidant du matériel disponible et du mode opératoire fourni |
|
TP verrerie /dissolution / dilution - Physique et Chimie
TP verrerie /dissolution / dilution Documents joints : - TP - Fiches RN chimie - Sécurités + pictogrammes - Fiche verrerie • Pré-requis : |
|
TP N° 2 : Préparation dune solution par dissolution ou par dilution
Diluer 10 fois une solution revient à diviser sa concentration par 10 la diluer 100 fois revient à diviser sa concentration par 100 On parle aussi de dilution |
|
TP Chimie n° 3
Diluer une solution aqueuse consiste en lui ajoutant de l'eau distillée à obtenir une solution moins concentrée Diluer 10 fois une solution revient à diviser |
|
TP C6 Dilution - Labo TP
TP C6 Dilution NOMS : Chapitre 2C Livre page 38 Objectifs : - Déterminer la valeur d'une concentration en masse à l'aide d'une gamme d'étalonnage ( |
|
PREPARATION DE SOLUTIONS
TP N°2 de Chimie 1 PREPARATION DES SOLUTIONS ET CALCUL D'INCERTITUDE BUTS DU TP a Préparation d'une solution à partir d'un soluté solide et dilution |
|
TP9 PREPARATION DUNE SOLUTION PAR DILUTION I Définitions
Diluer une solution aqueuse consiste en lui ajoutant de l'eau distillée à obtenir une solution moins concentrée Vocabulaire : Diluer 10 fois une solution |
|
TP n°9 de chimie : Préparation dune solution par dilution
Une dilution est une technique de préparation de solution (appelée solution fille) par ajout de solvant dans une première solution (appelée solution mère) |
|
TP Chimie 2 Préparation de solutions aqueuses • Par dissolution d
Verser la solution à diluer dans un becher (a) Prélever le volume calculé à l'aide d'une pipette jaugée munie d'un pipeteur (a et b) |
Comment faire une dilution en TP ?
Réaliser une dilution consiste à diminuer la concentration molaire d'une solution en ajoutant de l'eau (le solvant). La solution initiale utilisée est appelée la solution mère. Le volume prélevé de la solution mère sera noté Vi et sa concentration molaire Ci. La solution finale préparée est appelée la solution fille.Quel est le protocole de dilution ?
Les étapes de la dilution sont donc les suivantes : On prélève un volume de solution mère avec une pipette. On verse ce volume dans une fiole jaugée d'un volume égal à celui de solution fille désirée. On complète avec de l'eau distillée jusqu'au trait de jauge.Quel est le principe de la préparation des solutions ?
Afin de préparer la solution à la concentration demandée, il faut connaître le volume de la solution à préparer et la quantité de soluté nécessaire pour la faire. De manière générale, le volume est déterminé par la fiole jaugée dans laquelle on prépare la solution. Toutefois, la masse n'est généralement pas mentionnée.- Pour préparer ou diluer une solution à partir d'un volume donné de liquide on commence par prélever ce volume à la pipette graduée. On transfère ensuite le contenu de la pipette dans la fiole en maintenant la pipette verticale et en mettant sa pointe au contact de la fiole inclinée à 45°.
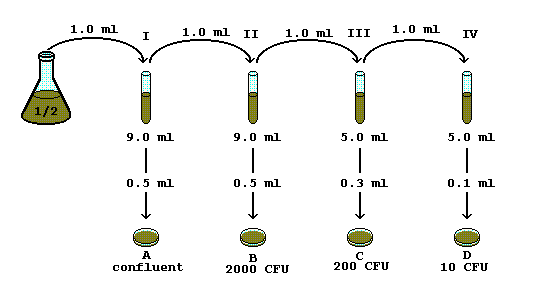
| LAB 9 SERIAL DILUTION POUR PLATES AND ENUMERATION OF BACTERIA |
| Syphilis Serologic Testing - Guidelines for Interpretation |
| Santé -TP n°7 : Préparation d’une solution Dilution |
| TP-Préparation d'une solution de concentration donnée par |
| Measurement of Cellulase Technical Report - NREL |
| TP n°3 : Dissolution et dilution |
| Searches related to tp dilution filetype:pdf |
|
Dilution - Aix - Marseille
m L d'une solution de concentration c = c0/10 à partir d'une solution m ère de concentration c0 Préparer une solution de concentration donnée par dilution |
|
Objectif Facteur de dilution Vocabulaire spécifique à la dilution
C'est un nombre qui caractérise la dilution réalisée On dilue x fois signifie que le facteur de dilution vaut x (et pas qu'on réalise x dilutions successives) |
|
Protocole pour réaliser une dilution
Protocole pour réaliser une dilution Etape 1 : Mettre la solution mère dans un bécher A l'aide d'une pipette jaugée de Vpipette mL, munie d'un dispositif |
|
MÉTHODE CHIMIQUE DE DILUTION PROCÉDÉ PAR INTÉGRATION
La méthode traditionnelle de dilution consiste à injecter dans la rivière un débit constant et par- faitement connu q d'une solution concentrée de bichromate à la |
|
Solutions - Concentrations
Dilution Exercice [Solution p 14] Une solution a une concentration massique de 40 g/L Dans une fiole jaugée de 250 mL, on verse 20 mL de cette solution et |
|
(Corr de TP n°7préparation solutiondilution)
Il souhaite la diluer pour obtenir un volume V1 = 100 mL d'une solution S1 de concentration massique : cm,1 = 5,0 g L-1 Comment aider le jardinier à préparer |
|
Densité dun solide - Préparation dune solution - Dilution ENONCE
A partir d'une solution commerciale d'acide nitrique de densité d = 1,33 et de pourcentage en acide nitrique : 52, 5 , on veut préparer, par dilution, V2 = 1 litre |
|
Protocole de dilution - Idexx
L'analyseur de biochimie Catalyst Dx* permet de réaliser des dilutions automatisées (il mélange l'échantillon et le diluant pour vous) et des dilutions manuelles ( |
|
Limite de linéarité Importance de la dilution - CSCQ
➢ Comprendre l'importance de la dilution avec un échantillon de CQE 1 Domaine de linéarité Le domaine de linéarité correspond à la zone de mesure où le |




























![Complete Quran for Dilution 16 Page PDF - [PDF Document] Complete Quran for Dilution 16 Page PDF - [PDF Document]](https://fieldresearch.msf.org/bitstream/handle/10144/600287/Shanks%20et%20al%20-%202015%20-%20Dilution%20testing%20using%20rapid%20diagnostic%20tests%20in%20a%20HIV%20diagnostic%20algorithm.pdf.jpg?sequence\u003d4\u0026isAllowed\u003dy)







