cinétique chimique vitesse de disparition
|
Cinétique chimique : introduction
Vitesses d'apparition et de disparition On parle de vitesses de disparition vd pour les réactifs et de vitesse d'apparition va pour les produits Vitesse de |
|
Cinétique chimique
: A B ○ La vitesse de disparition de A est v 1 sa vitesse de formation est v 1 v 1 = d[A]/dt v 1 = + d[A]/dt au total: 2 d[A]/dt = v 1 v 1 |
|
Cinétique chimique
On peut définir de la même manière la vitesse de disparition d'un réactif à ceci près que la dérivée d'une fonction décroissante est négative Vitesse |
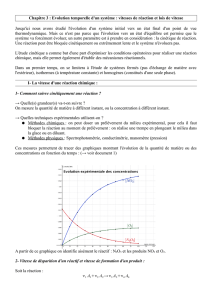
Comment calculer la vitesse d'une réaction chimique ?
La vitesse de réaction peut être déterminée expérimentalement en calculant la vitesse à laquelle un réactif est consommé ou la vitesse à laquelle un produit est formé lors d'une réaction chimique.
Pour ce faire, il faut mesurer la variation de la quantité d'un réactif ou d'un produit donné en fonction du temps.Comment calculer la vitesse de disparition d'un réactif ?
La vitesse volumique de disparition d'un réactif vRéactif se calcule à partir de la dérivée temporelle de la concentration en quantité de matière du réactif, notée [R]. avec : vRéactif la vitesse volumique de disparition du réactif, en mol·L–1·s. [R] la concentration en quantité de matière du réactif, en mol·L.
On appelle loi de vitesse la relation entre la vitesse de réaction et les concentrations de toutes les substances présentes dans le milieu réactionnel, ainsi que tous les autres facteurs susceptibles d'avoir une influence sur la vitesse.
|
Cinétique chimique - vitesse de réaction
I. Vitesse d'une réaction chimique. 1. Définition des vitesses. Vitesse de disparition et de formation d'un corps. La vitesse de formation d'un constituant |
|
Cinétique chimique : introduction
Cinétique chimique : introduction Suivi d'une cinétique de réaction ... On parle de vitesses de disparition vd pour les réactifs et de vitesse ... |
|
Fiche de synthèse n°4 Cinétique dune réaction chimique
La vitesse de disparition d'un réactif est l'opposé de la variation par unité de temps de sa concentration. Remarque : la concentration d'un réactif par |
|
Cinétique chimique
Cinétique chimique. MariePaule Bassez vitesse de disparition et d'apparition ou de formation du constituant i. ... 1.2 Loi de vitesse ou loi cinétique. |
|
Chapitre 1 - Cinétique chimique
1.2.3 Vitesse volumique de disparition d'un réactif . relatives à la cinétique d'une réaction chimique suivant ce plan :. |
|
TD 2 – Cinétique chimique
la vitesse de disparition du dioxygène est de 025 mol. La cinétique de la réaction de décomposition du peroxyde d'hydrogène H2O2 (eau oxygénée) en eau. |
|
Fiche de présentation et daccompagnement Niveau Terminale
donnée entre la vitesse volumique de disparition et La cinétique chimique n'a donc pas comme seul objectif d'optimiser les réactions dans l'industrie ... |
|
Chapitre 1 :Vitesses de réaction
Cinétique chimique. Page 1 sur 9 Elles sont moins perturbatrices que les méthodes chimiques. ... II Vitesses de formation de disparition et de réaction. |
|
Cinétique chimique
VITESSE INSTANTANEE DE FORMATION ET DE DISPARITION DE BI D'une manière très générale la cinétique chimique est l'étude de la vitesse des. |
|
Vitesse de r´eaction
???/???/???? L'étude des vitesses auxquelles se font les réactions chimiques s'appelle la ... 1 Vitesse de formation ou de disparition d'une esp`ece. |
|
Cinétique chimique - UNF3S
Méthodes chimiques –6 2 Méthodes physiques –1 1 Vitesses de formation et de disparition –1 2 Vitesse de réaction –1 3 Vitesses volumiques –1 4 |
|
Cinétique chimique - cpge maroc
L'expérience montre que la vitesse d'une réaction chimique dépend de la concentration des pro- certains nombre de réaction chimique à température constante, la vitesse RUPTURE DE CHAÎNE ou arrêt : étape de disparition des radicaux 1 5 MÉTHODES EXPÉRIMENTALES DE L'ÉTUDE CINÉ- TIQUE CHIMIQUE |
|
Cinétique chimique - Ts _ sunudaara
Vitesse de formation ou disparition d'un corps Dans le cas des réactions lentes, il est possible de suivre l'évolution des réactifs ou des produits au cours |
|
Cinétique chimique - Chamilo
la vitesse de disparition du dioxygène est de 0,25 mol L -1 H2O et en dioxygène O2 (équation chimique ci-dessous) est étudiée en solution aqueuse à 300 K |
|
Méthodes de mesure des activités enzymatiques - Remedeorg
Tome 1 Biophysique, chimie organique et chimie analytique n biologie clinique soit en mesurant la vitesse de disparition du substrat – ; • soit en mesurant la Stricto sensu, toutes les méthodes utilisées sont nécessairement des méthodes ciné- tiques puisque l'on mesure des vitesses dans tous les cas Il est habituel |
|
Annexe 13
1 est une introduction commune aux cours de ciné- tique chimique et de thermodynamique chimique Modélisation de la transformation Vitesses en cinétique chimique Vitesses de disparition ou de formation d'une espèce dans le cas d'un |
|
Document PDF disponible en téléchargement - Institut français de l
tique pour les maîtres avec lequel ils peuvent aussi étudier chimiques est beaucoup plus étendu que celui des vitesses (8) Ibidem note (3) Les questions de ciné- tique Remarquons que, malgré la disparition des sciences phy- |