cinétique chimique vitesse de réaction
|
Cinétique chimique : introduction
Cette vitesse volumique de réaction est toujours positive et ne dépend pas de l'espèce chimique Elle est exprimée en mol L‐1 s‐1 Détermination graphique de la |
Comment calculer la vitesse d'une réaction chimique ?
La grandeur v i = d n i d t est appelée vitesse de transformation du constituant .
C'est une grandeur algébrique positive dans le cas des produits, négative dans le cas des réactifs.1Calcul de la vitesse initiale de la réaction. v1=k⋅[x]⋅[y]2. v1=kxy2.
2) Calcul de la nouvelle vitesse de la réaction. v2=k⋅[2x]⋅[2y]2. v2=k⋅2x⋅4y2. v2=8kxy2.
3) Comparaison des deux vitesses.
Comment déterminer la constante de vitesse d'une réaction ?
L'unité de la constante de vitesse k peut être déterminée par une analyse dimensionnelle (la dimension d'une grandeur se note entre crochets).
Ainsi, [k] = T-1 (T : symbole dimensionnel d'un temps).
Nous pouvons en déduire que, pour une réaction d'ordre global n = 1, l'unité usuelle de k est : s-1.
|
Cinétique chimique - vitesse de réaction
La cinétique chimique s'intéresse à l'évolution au cours du temps d'une réaction. I. Vitesse d'une réaction chimique. 1. Définition des vitesses. Vitesse de |
|
Cinétique chimique : introduction
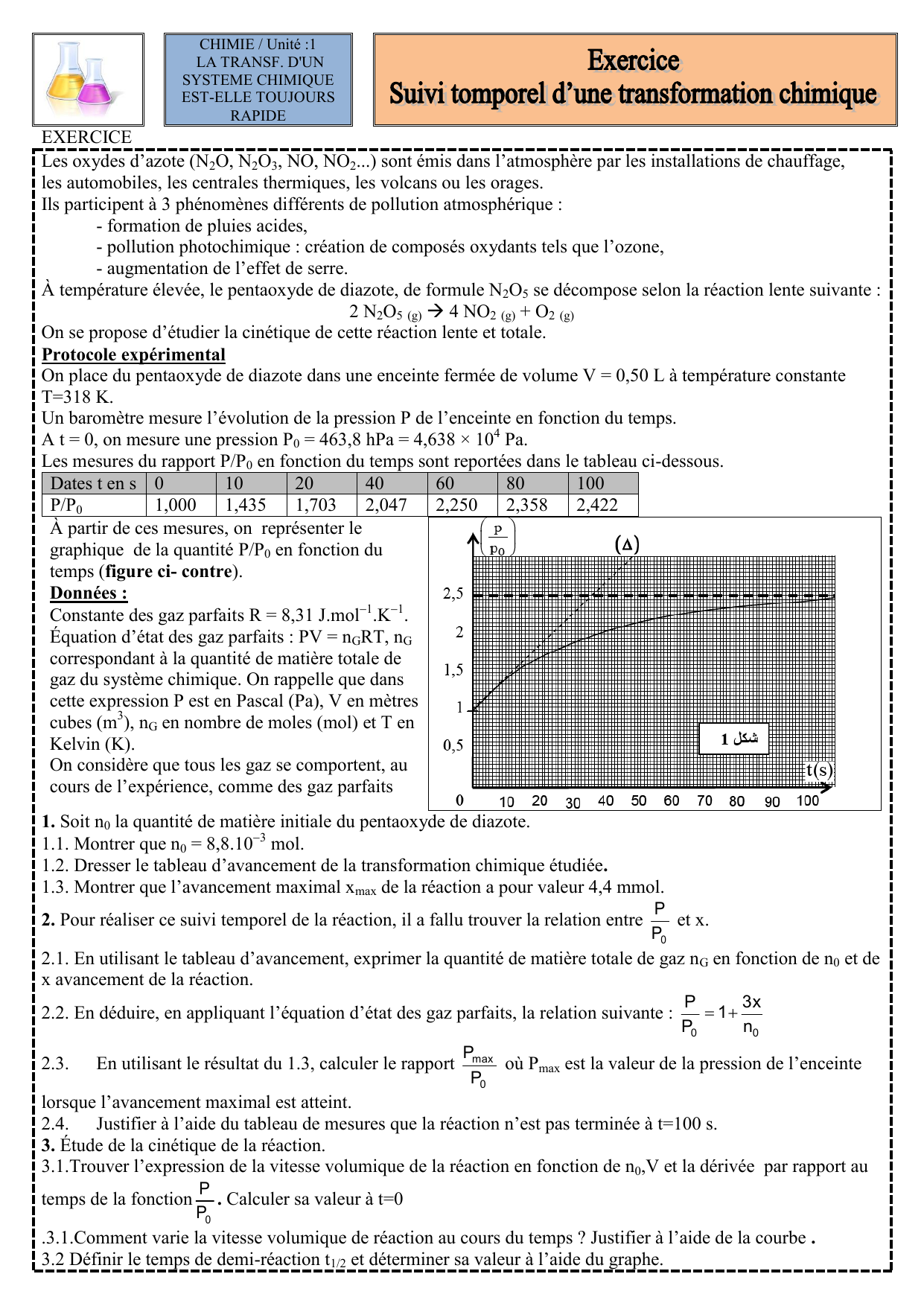
s?1. Détermination graphique de la vitesse de réaction. La vitesse de réaction est la tangente en un point de la courbe |
|
Chapitre 1 :Vitesses de réaction
Cinétique chimique. Page 1 sur 9. I Système œ réaction chimique. A) Système physique ou chimique II Vitesses de formation de disparition et de réaction. |
|
Cinétique chimique
1.8 Expression d'une équation cinétique et d'une loi de vitesse intégrée. 2. Détermination de l'ordre d'une réaction. 2.1 Méthode intégrale; 2.2 Méthode du |
|
Loi de vitesse dune réaction chimique
chimique. Ils ne peuvent être déterminés que de façon expérimentale. Facteurs influençant la vitesse d'une réaction. On appelle facteurs cinétiques les |
|
CHAPITRE 2 : LA CINÉTIQUE CHIMIQUE ; VITESSES ET
Certaines variables peuvent accélérer ou ralentir les réactions : - La concentration des réactifs; la vitesse augmente généralement en fonction de la. |
|
La chimie
la cinétique chimique s'intéresse à la vitesse à laquelle s'effectue les réactions chimiques. • la vitesse de réaction est la variation de la concentration. |
|
Fiche de synthèse n°4 Cinétique dune réaction chimique
Nous les appellerons les réactions lentes. La cinétique chimique est l'étude de la vitesse des réactions. 1. Vitesse d'apparition d'un produit |
|
Cinétique chimique – vitesse de réaction
Cinétique chimique – vitesse de réaction. 1. Combien de temps va-t-il falloir pour faire réagir 450 g de CaCO3(s) avec du HCl(aq) si la vitesse de réaction |
|
Thème : Cinétique chimique Fiche 5 : Vitesse de réaction
Facteur cinétique : grandeur physique qui influence la vitesse de réaction. Les facteurs cinétiques sont la température du milieu réactionnel la concentration |
|
Cinétique chimique - UNF3S
La loi de vitesse est une relation mathématique entre la vitesse de la réaction et les concentrations des différentes espèces • 2 2 Exemples de lois de vitesse – |
|
Loi de vitesse dune réaction chimique
La pente de la courbe d'évolution [B]=f(t) est égale à une constante cinétique apparente, kapp (proportionnel à k) Il y a aussi dégénérescence d'ordre dans le cas |
|
Cinétique chimique - Chimie en PCSI
Comment étudier la vitesse de cette réaction ? Voilà ce que nous allons étudier I – VITESSES D'UNE REACTION CHIMIQUE 6 1 |
|
Cinétique chimique
1 7 Cinétique de réactions d'ordre 1 proches de l'équilibre 1 8 Expression d'une équation cinétique et d'une loi de vitesse intégrée 2 Détermination de l'ordre |
|
Cinétique chimique - Lycée dAdultes
Cinétique chimique 1 1 Facteurs cinétiques et catalyse ou moins grande vitesse selon la nature de la réaction chimique et les conditions expérimentales |
|
Cinétique chimique
Avec k: constante de vitesse et p, q ordres partiels par rapport aux réactifs Ai1 et Ai2 La somme p + q = α ordre global de la réaction Remarques : • l'ordre partiel p |
|
CINETIQUE CHIMIQU EE SPÉ MP
En général, la vitesse des réactions chimiques décroît au fur et à mesure de leur avancement La constante de vitesse k augmente avec la température : en |