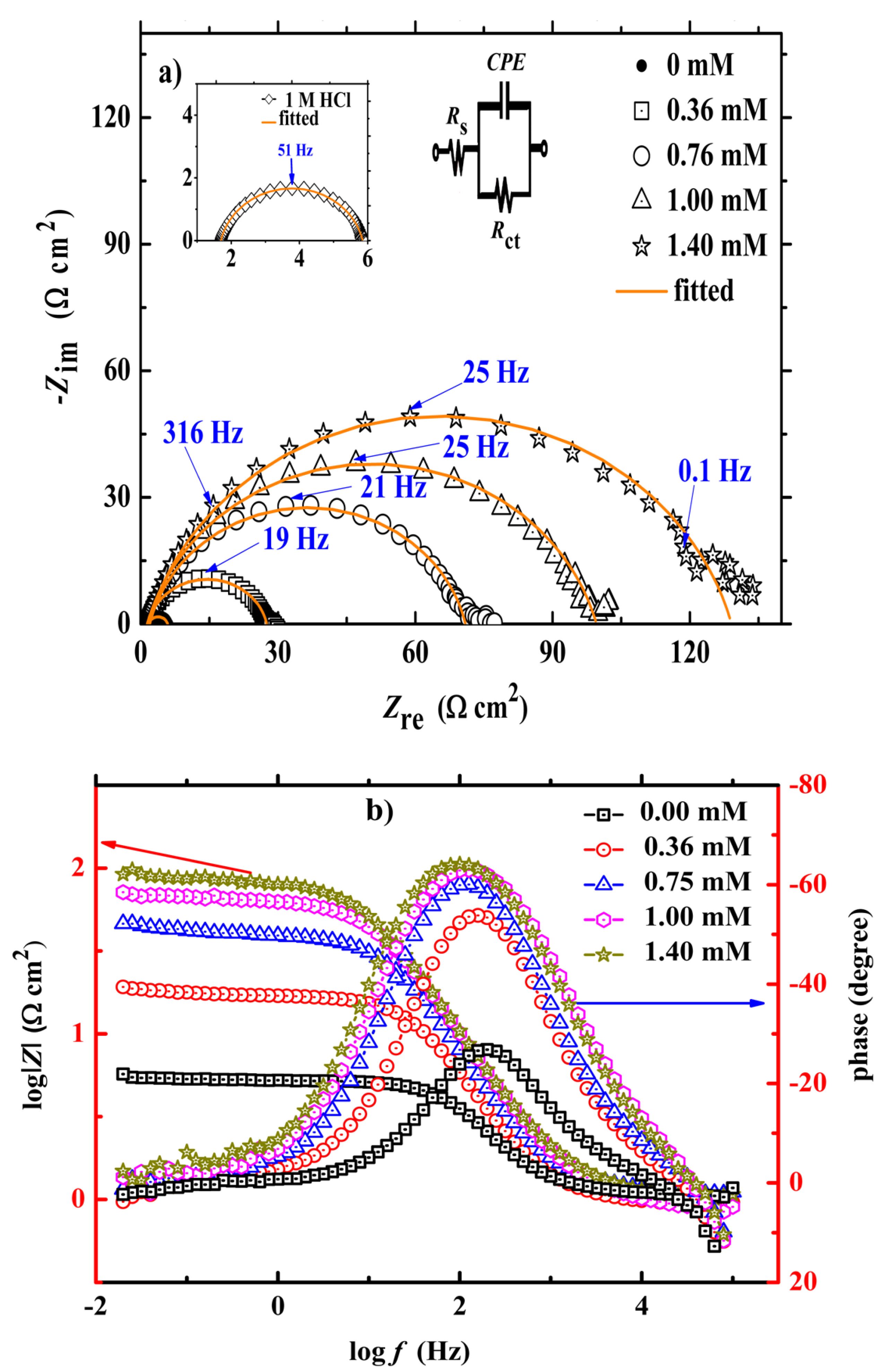
Electrochimie corrosion
|
26 Électrochimie et corrosion
(F) La corrosion est l'attaque destructive que subit un métal par une réaction chimique ou électrochimique avec l'environnement La formation de rouille sur le |
|
COURS DE CORROSION
- Corrosion électrochimique (humide) - Corrosion biochimique - Corrosion accompagnée d'érosion (mécanique) 2 1 Corrosion chimique (sèche) Il |
La corrosion n'est qu'un retour à l'état « naturel » d'oxyde pour ces métaux façonnés par l'intervention humaine.
La corrosion des métaux est dans la grande majorité des cas une réaction électrochimique (une oxydoréduction), faisant intervenir la pièce manufacturée et l'environnement comme réactifs.
Comment se produit la corrosion ?
III Comment se forme la corrosion ? La corrosion se forme par dégradation d'une surface le plus souvent de nature métallique, à température ambiante, sous l'effet des agents atmosphériques ou de produits chimiques.
La corrosion des métaux est un phénomène naturel.
C'est quoi la corrosion électrochimique ?
La corrosion est un processus électrochimique qui détériore le métal en réagissant avec l'environnement.
Le processus de corrosion détériore le fer à l'intérieur de l'acier, entraînant la perte de ses principales caractéristiques telles que la dureté ou la résistance.
L'oxyde ferrique ou la rouille consomme le métal.
Quels sont les facteurs qui affectent la corrosion ?
Trois éléments sont nécessaires pour que la corrosion se produise : un électrolyte, une surface métallique exposée et un accepteur d'électrons.
La corrosion peut être évitée en supprimant l'une de ces conditions.
|
La Corrosion - UNF3S - CAMPUS NUMERIQUES
L'allure des courbes renseigne sur les différentes réactions électrochimiques mises en jeu pour des potentiels donnés Figure 4 : Courbe de polarisation : principe |
|
Filière sciences de la matière Cours délectrochimie SMC Semestre 5
Conduit à un potentiel de corrosion situé dans le diagramme tension-pH où le métal est actif et un courant de corrosion Ex1 : le fer dans une solution acide pH =1 |
|
Électrochimie et corrosion III - Archimer - Ifremer
chose courante dans un laboratoire “Corrosion” Enregistrer l'évolution d'un potentiel d'abandon en fonction du temps, obtenir la relation densité de courant- poten |
|
Électrochimie et corrosion à léchelle des microstructures
Électrochimie et corrosion à l'échelle des microstructures Tous les processus de corrosion localisée sont contrôlés par un couplage galvanique qui va |
|
Chapitre 4 :La corrosion
C'est la corrosion en l'absence totale d'eau Dans la suite, on ne considère que la corrosion humide (la corrosion sèche a B) Protection électrochimique |
|
Etude électrochilnique de la Corrosion Sous Contrainte dalliages
I-1-1-b Phénoménologie de la corrosion sous contrainte des matériaux ductiles CHAPITRE III : Etude électrochimique de la CSC des alliages Cuivre-Zinc |










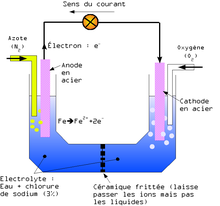








.jpg)










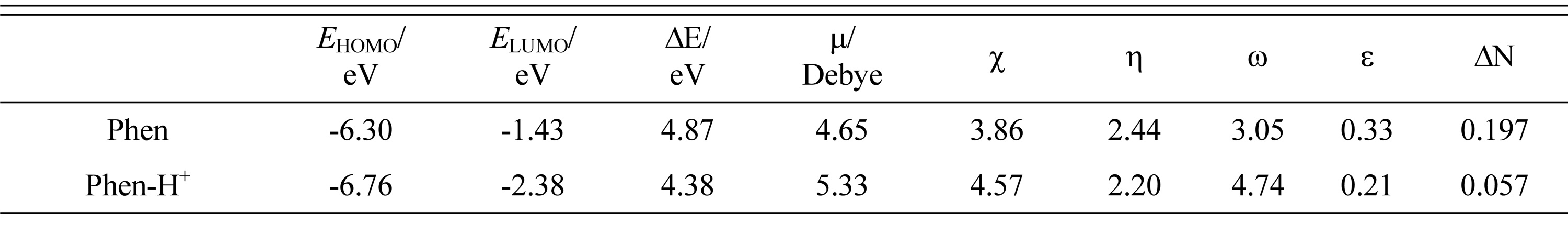







-3_POLY.jpg)