ajuster les nombres stoechiométriques des équations suivantes
|
A C2H6O + 3 O2 → 3 H2O + 2 CO2 b 2 Fe + 3 Zn → 3 Zn + 2 Fe c
EXERCICE N°2 : Ajuster les nombres stœchiométriques des équations suivantes si nécessaire : a C2H6O + 3 O2 → 3 H2O + 2 CO2 b 2 Fe 3+ + 3 Zn → 3 Zn 2+ + |
|
Ajuster les nombres stœchiométriques dune équation bilan
Objectif : définir une démarche pour écrire correctement une équation bilan en ajustant correctement les nombres stœchiométriques I Exemple : On va chercher à |
|
Chapitre 6 Réaction chimique et dosage – Séance 2 1 Équilib
Une équation chimique doit toujours être écrite avec ses nombres stoechiométriques ajustés Cela traduit la conservation des |
|
Equilibrer les équations suivantes : a) b) c) d) → 5 CO2 + 4 H2O e
Ajuster les nombres stœchiométriques des équations chimiques ci-dessous relatives aux principales réactions alors mises en jeu ; C8H18 représente les |
|
EXERCICES-Bilan-de-la-matièrepdf
1) Ecrire l'équation de cette réaction et ajuster les nombres stoechiométriques 2) Préparer le tableau d'avancement de la réaction 3) Tout le gaz ayant |
Comment ajuster la stoechiométrie des équations chimiques ?
On ajuste une nouvelle fois le coefficient stœchiométrique d'un élément non équilibré, du côté des réactifs ou des produits.
On équilibre ensuite l'élément carbone.
Pour cela, il faut écrire un coefficient stœchiométrique de 2 pour \\ce{CO2}, ainsi il y aura 2 atomes de carbone des deux côtés.Comment trouver le nombre Stoechiométrique ?
Le nombre (ou facteur) stœchiométrique d'une espèce chimique dans une réaction chimique donnée est le nombre qui précède sa formule dans l'équation considérée (un, à défaut).
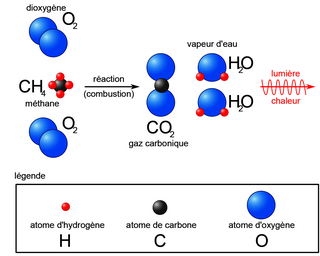
Dans l'exemple précédent : CH4 + 2 O2 → CO2 + 2 H2O.Comment ajuster une réaction ?
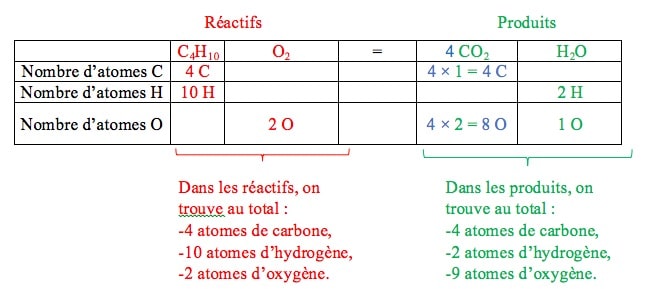
Pour que l'équation soit ajustée, il faut qu'il y ait le même nombre d'atomes de chaque type dans les réactifs et les produits, donc la différence entre le nombre d'atomes de carbone se trouvant dans les réactifs et le nombre d'atomes de carbone se trouvant dans les produit doit être nulle.
- Étapes pour équilibrer une équation chimique
Compte le nombre d'atomes pour chaque élément des deux côtés de l'équation. Équilibre les atomes un par un en ajoutant un coefficient de réaction devant les formules jusqu'à ce que l'équation soit équilibrée.
Utilise les symboles d'état corrects dans l'équation.
|
Ajuster les nombres stœchiométriques dune équation bilan.
Ajuster les nombres stœchiométriques d'une équation bilan. Les nombres (ou coefficients) stœchiométriques sont là pour faire en sorte que la loi de |
|
Ré visions sur lé bilan duné transformation chimiqué Exércicés sur
Cette notion d'équation bilan est très importante en chimie car elle traduit ce qui se passe Ajuster les nombres stœchiométriques des équation suivantes. |
|
Equilibrer les équations suivantes : a) b) c) d) ? 5 CO2 + 4 H2O e
Exercices : équation-bilan. I- Equilibrer les équations suivantes : Ajuster les nombres stœchiométriques des équations chimiques ci-dessous. |
|
Seconde AE28 Bilan de matière et réactif limitant
Ajuster les nombres stœchiométriques de l'équation de la recette du sandwitch au fromage. répondre aux questions suivantes :. |
|
SESSION 2006
Recopier les demi-équations suivantes puis ajuster les nombres stœchiométriques. O2. + H+. + e -. ? H2O. C6H5CHO + H2O ?. C6H5COOH + H+. |
|
Travaux dirigés de Chimie n° 1
Exercice 1 : Ajuster une équation chimique. Ajuster les nombres stœchiométriques des équations suivantes : a. C2H6(g). |
|
Ajuster léquation dune réaction chimique
Modélisation d'une transformation chimique par une équation de réaction. d'ajustement en faisant varier les nombres stœchiométriques. |
|
Méthodologie Equation de réaction chimique
2èmeétape : On ajuste les nombres stœchiométriques afin d'avoir autant Equilibrer les équations de réactions chimiques suivantes en ajustant les nombres ... |
|
Exercices de chimie équations bilan
en quantité de matière. 3. Équations chimiques correctes. Les nombres stœchiométriques des équations chimiques suivantes ont-ils été correctement ajustés ? |
|
A. C2H6O + O2 ? H2O + CO2 b. Fe + Zn ? Zn + Fe c. CaCO3 + H +
Ecrire l'équation chimique ajustée de chacune EXERCICE N°2 : Ajuster les nombres stœchiométriques des équations suivantes si nécessaire :. |
|
Wifeo - Ajuster les nombres stœchiométriques dune équation bilan
Objectif : définir une démarche pour écrire correctement une équation bilan en ajustant correctement les nombres stœchiométriques I Exemple : On va chercher à |
|
Comment ajuster les nombres stœchiométriques ? - Maxicours
Comment ajuster les nombres stœchiométriques ? · 1 Écriture de l'équation chimique · 2 Réalisation de l'ajustement des nombres stœchiométriques · 3 |
|
Exercices : équilibrer les équations chimiques
NH3 + O2 NO + H2O Réponses CO + Fe3O4 CO2 + Fe Cu2S + Cu2O Cu + SO2 CH4 + H2O CO2 + H2 NaCl + H2SO4 HCl + Na2SO4 H2SO4+ H2O H3O+ + SO42- |
|
Ajuster des nombres stoechiométriques Méthode - Kartable
Avis 45 |
|
Equilibrer les équations suivantes : a) b) c) d) ? 5 CO2 + 4 H2O e
Ajuster les nombres stœchiométriques des équations chimiques ci-dessous relatives aux principales réactions alors mises en jeu ; C8H18 représente les |
|
Méthodologie Equation de réaction chimique - WordPresscom
2èmeétape : On ajuste les nombres stœchiométriques afin d'avoir autant Equilibrer les équations de réactions chimiques suivantes en ajustant les nombres |
|
Ajuster léquation dune réaction chimique - Eduscol
Exemple : On considère l'équation modélisant la combustion du carbone : xC + yO2 ? zCO2 avec y z étant les nombres stœchiométriques La molécule de dioxyde |
|
Exercices de chimie équations bilan - ACCESMAD
en quantité de matière 3 Équations chimiques correctes Les nombres stœchiométriques des équations chimiques suivantes ont-ils été correctement ajustés ? |
|
Exercices
Ex 13 – Ajuster des équations Recopier et ajuster avec des nombres stœchiométriques corrects les équations des réactions chimiques suivantes : |
|
Exercices
Etablir les demi-équations redox des couples suivants en présence d'ions hydrogène : Ecrire l'équation de la réaction avec les nombres stœchiométriques |
Comment ajuster la stoechiométrie des équations chimiques ?
On commence par l'élément chimique qui est présent en plus grande quantité. On ajuste son coefficient stœchiométrique du côté des réactifs ou des produits. Il vaut mieux équilibrer en dernier l'élément chimique qui apparaît dans le plus grand nombre d'esp?s chimiques.Comment calculer les nombres stoechiométriques ?
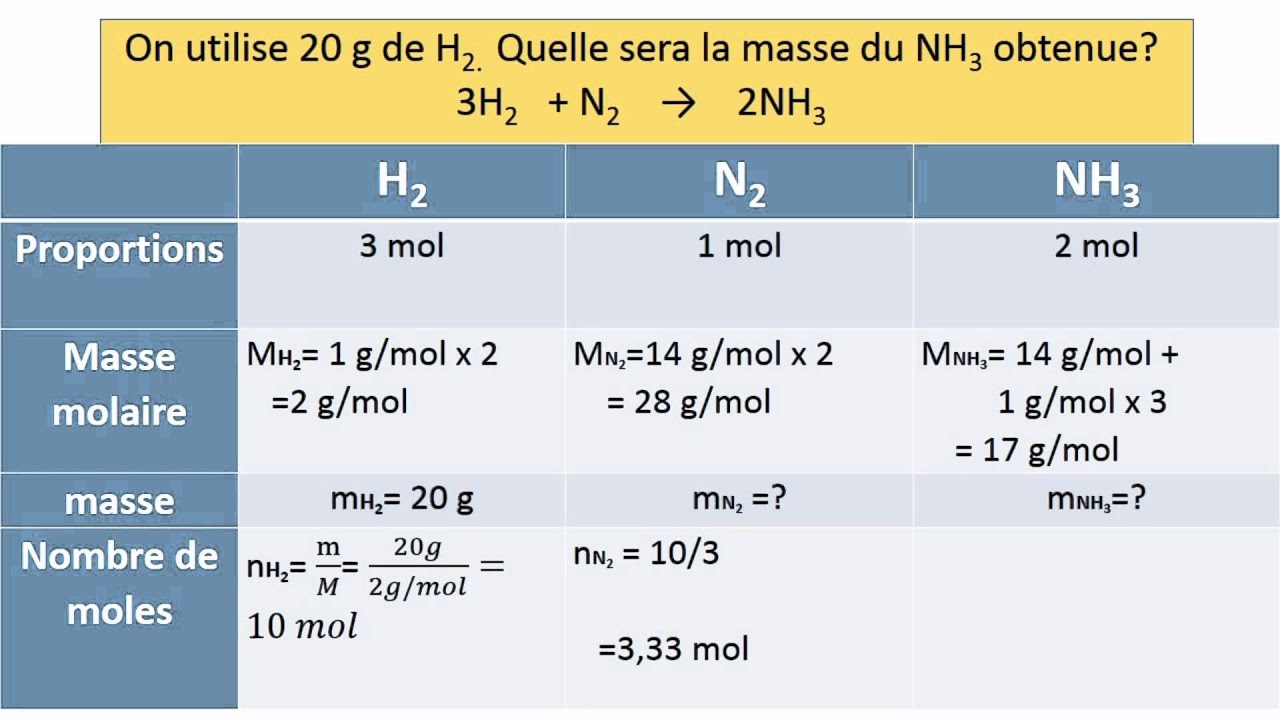
Il faut faire un produit croisé entre le nombre de moles de la réaction équilibrée et le nombre de moles utilisées dans la réaction. Considérant l'équation équilibrée, il est logique le nombre de moles soit le même pour H2O H 2 O et H2 , car, dans l'équation équilibrée, il y autant de moles de chacune des molécules.Comment ajuster des equations de réactions ?
Pour équilibrer une équation de réaction chimique, il faut s'assurer de placer les bons coefficients stœchiométriques devant les molécules de l'équation, pour qu'il y ait autant d'atomes à gauche qu'à droite de la fl?he.- Un mélange est stœchiométrique si les réactifs sont tous entièrement consommés à l'état final, c'est donc le mélange le plus efficace. Le tableau d'avancement relatif à une réaction chimique permet de déterminer si, à partir des quantités initiales des réactifs, le mélange est stœchiométrique.
| Ajuster les nombres stœchiométriques - wifeocom |
| Ajuster les nombres stœchiométriques - wifeocom |
| Exércicés sur la transformation chimiqué |
| Première S Ecole Alsacienne Ajuster une équation d'oxydo |
| Chapitre 8 : Modélisation des transformations chimiques |
| Searches related to ajuster les nombres stoechiométriques des équation filetype:pdf |
Comment ajuster les nombres stœchiométriques d'une équation bilan ?
- Ajuster les nombres stœchiométriques d'une équation bilan.
. Les nombres (ou coefficients) stœchiométriques sont là pour faire en sorte que la loi de Lavoisier soit respectée lors de l'écriture de l'équation bilan, c'est-à-dire que les éléments chimiques se conservent en nature et en nombre lors d'une transformation.
Comment calculer le sens d'une équation?
- -x 1 ---------------------------------------------------------------------------------------------------- 6 Br 2(aq) + 12 OH - (aq) ?10 Br- (aq) + 2 BrO 3 - (aq) + 6 H 2 O (le sens ?est déterminé par l'expérience) On simplifie ensuite pour avoir l'écriture de l'équation la plus simple :