équation de dissolution exercice PDF Cours,Exercices ,Examens
|
Concentration et solutions électrolytiques Correction
Exercice 1 : Une masse = 171 de sulfate d'aluminium solide est dissoute dans 2- Ecrire l'équation de dissolution 3- En déduire les concentrations |
|
Cours et exercices de chimie des solutions
Dans cet exercice on négligera toute réaction acido-basique des ions avec l'eau n: le nombre d'électron échangé aux cours de la réaction Qmax = Nmax(e |
|
Exercices de chimie de révision et de préparation au programme de
Exercice 3 : équation rédox Ecrire les ½ équations des couples : • ion équation de dissolution La concentration de cette solution est c = 500 10-2 mol |
|
Exercices de physique-chimie Première Spécialité
Exercice 16 Écrire l'équation de réaction de dissolution dans l ?eau de chacun des composés ioniques suivants 1 le chlorure de cuivre (II) CuCl2(s) 2 l |
Comment trouver l'équation de dissolution ?
L'équation de dissolution dans l'eau du chlorure de potassium est : KCl (s)→ K+ (aq) + Cl– (aq) b.
D'après l'équation de dissolution : n(KCl) = n(K+ (aq)) = n(Cl– (aq)).
Donc n(K+ (aq)) = n(Cl– (aq)) = n = 2,50 mmol.Comment trouver le pH d'une solution ?
Le pH d'une solution est lié à la concentration en quantité de matière d'ions oxonium.
Les relations entre le pH et la concentration en quantité de matière d'ions oxonium sont pH = –log[H3O+] et [H3O+] = 10–pH.Comment savoir si une solution est électriquement neutre ?
Si l'on reprend l'exemple de la dissolution du Chlorure de sodium, on constate que l'ion Na+ porte une charge positive tandis que l'ion Cl- porte une charge négative.
Cela nous donne alors une charge positive et une charge négative : la charge globale est donc nulle et la solution est électriquement neutre.- Écrire l'équation chimique équilibrée de la réaction.
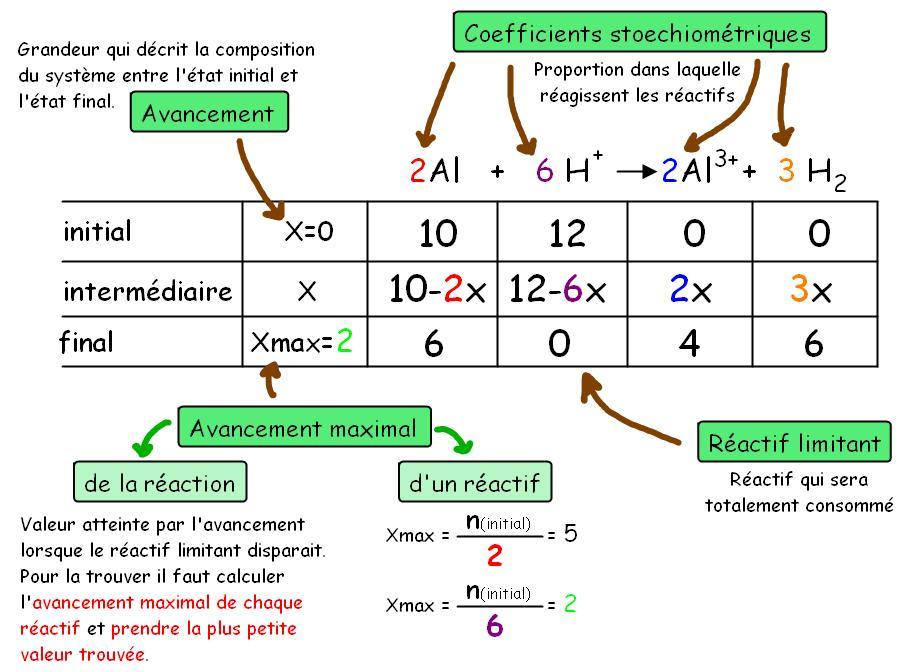
Calculer la quantité de produit formé à partir de chaque réactif en utilisant les coefficients stœchiométriques.
Comparer les quantités de produit formé pour chaque réactif.
Le réactif qui produit la plus petite quantité de produit est le réactif limitant.
|
Exercices de révisions : Physique-chimie
cours désigne l'état du système en cours d'évolution pour divers Exercice n°2 : Quantité de matière et tableau d'avancement ... selon l'équation :. |
|
Correction exercices Précis de Physique-Chimie chapitre1 à 4
Physique-Chimie ainsi que sur la correction des exercices n'hésitez pas à m'en faire part en Exercice 1 : Équations de dissolution et de précipitation. |
|
EXERCICES
Exercice 5. Exercice 6. Exercice 7 2 Dissolution des solides ioniques. Exercice 1. Exercice 2 ... L'équation chimique de la dissolution est. AlCl3(s). |
|
Cours et exercices de chimie des solutions
quantité maximale de ce constituant que le solvant peut dissoudre. l'équation (1) ne reflète pas une réaction chimique réelle ; on l'appelle parfois la ... |
|
Génie de la Réaction Chimique: les réacteurs homogènes
14 juil. 2022 Exercice : Reformage du méthane à la vapeur d'eau ... plan du cours ... dans les exercices qu'il est préférable de retrouver l'équation ... |
|
Physique Chimie
8 févr. 2017 Le chapitre 5 du manuel de Cycle 4 « Dissolution des gaz dans l'eau » ... Des exercices simples pour s'entraîner regroupés par. |
|
Td corriges biochmv 2014-2015.pdf
Exercices 2014-2015 Dans un bécher dissoudre ce composé dans de l'eau ... EXERCICE 2 : Avant de réaliser une manipulation de Biochimie |
|
LES REACTIONS DE PRECIPITATION Exercice 1 (Daprès BTS BT
CORRECTION EXERCICES DE REVISION : LES REACTIONS DE PRECIPITATION. Exercice 1 Equation de dissolution de l'hydroxyde de cuivre (II) dans l'eau pure :. |
|
COURS DE CHIMIE Avec EXERCICES
chapitre aux questions des exercices d'auto-évaluation. Solvatation : Il s'agit d'un phénomène physico-chimique observé lors de la dissolution. |
|
Dosages par titrage direct 10 Extraits de sujets corrigés du bac S
encadrer l'équation de la réaction support du titrage si elle est donnée. EXERCICE 2 – UN EXEMPLE DE CHIMIE VERTE : LA SYNTHÈSE DE L'IBUPROFÈNE. |
| Exercices de la Séquence n°16 Séparation et purification |
| Ecrire l'équation de dissolution d'un solide - Kartable |
Comment faire une équation de dissolution ?
- Écrire l'équation de dissolution On écrit l'équation de dissolution en dessinant une flèche orientée vers la droite et en indiquant la formule du solide ionique à sa gauche et les formules des ions, précédées de leurs coefficients stœchiométriques (égaux à leurs indices dans la formule du solide), à droite.
Quels sont les équations de dissolution totale dans l'eau?
- EXERCICE 1 : Équations de dissolution Écrire les équations de dissolution totale dans l'eau des solides ioniques suivants : – le bromure de sodium NaBr – le chlorure de fer (III) FeCl 3 – le permanganate de potassium KMnO 4 – le thiosulfate de sodium Na 2 S 2 O 3 – le nitrate de cuivre Cu(NO 3 2 EXERCICE 2 : Polarisation de liaisons 1.
Quels sont les exercices de dissolution d'un solide ionique ?
- Paru dans ▶ Exercices - Dissolution d'un solide ionique : Première Exercice 01 : Dissolution de chlorure d baryum. On prépare une solution aqueuse de chlorure de baryum. Ecrire l’équation de dissolution dans l’eau du chlorure de baryum de formule Exercice 02 : Le bromure de potassium.
Comment calculer la dissolution d'un atome dans l'eau ?
- Compléter l'équation de dissolution du \\ (CuSO_ {4}\\) dans de l'eau : \\ [ CuSO_ {4} \\longrightarrow ... + ... \\] On écrira la réaction dans son intégralité et en utilisant le symbole \\ ( \\longrightarrow \\) du clavier virtuel. Déterminer le nombre de liaisons covalentes que cet atome peut établir.
|
Exercices corrigés
L-1 1 – Écrire les formules des solides phosphate de potassium et sulfate de potassium puis les équations de dissolution correspondantes 2 – Nommer |
|
Exercices de révisions : Physique-chimie
Exercice n°2 : Quantité de matière et tableau d'avancement Le diiode I2 3 En déduire l'équation de la réaction étudiée (réaction de dismuation) Un élève a préparé cette solution par dissolution du solide dans 100,0 mL d'eau distillée |
|
Cours et exercices de chimie des solutions
quantité maximale de ce constituant que le solvant peut dissoudre Exercices Exercice 1 Dans une fiole jaugee de 250 ml, on met : 25 ml de solution de NaCl |
|
Oxydoréduction – corrigé des exercices Table des matières
Le réducteur est Zn, qui s'oxyde en Zn2+ L'oxydant est H+ qui va se réduire en H2 L'équation de l'oxydation est : Zn Zn2+ + |
|
Structure de la matière Chimie 1 –Cours & Exercices - DSpace
En général, on peut écrire une équation qui montre le bilan d'une réaction Le solvant est toute substance liquide qui a le pouvoir de dissoudre d'autres |
|
Précipitation et dissolution Précipitation et - Étienne Thibierge
6 mar 2018 · Précipitation et dissolution Exercices Exercice 1 : Calculs de solubilité [♢00] Calculer la solubilité du chlorure d'argent (pKs(AgCl) = 9,7) et |
|
Physique - Chimie - CHTOUKAPHYSIQUE
de concentration de Exercices type bac Conductance d'une solution d'acide méthanoïque On réalise la dissolution de l'acide méthanoïque dans l'eau, et ce, |
|
CORRECTION EXERCICES DE REVISION : LES REACTIONS DE
Exercice 2 (D'après BTS BT 2010 Produit de solubilité) 1 Solubilité de l' hydroxyde de cuivre (II) dans l'eau pure à 25°C 1 1 Equation de dissolution de |
|
Chimie minérale systématique II Métaux et semi-métaux - UniNE
Précipitation et dissolution complexante successive des sels d'argent formule idéalisée : en vérité MnO1 7-2 0 (la largeur de phase étant due à la présence |
|
18 - Quelques solubilités - Chimie - PCSI
Page 1 sur 4 Corrigé exercice 18 Dissolution d'un solide ionique à ions indifférents dans l'eau pure et raisonner sur l'équation de dissolution simple : RD : |