acetate de sodium > chimie mineral et organique
|
Chimie générale avancée I: Introduction à la Chimie Organique
La Chimie Organique à l’EPFL Chimie générale avancée I et II (Jerome Waser) Principles Acids and Bases Structures Addition Elimination and Substitution reactions BA1-2 Introduction Lab (2 days) OBL Fonctions/Réactions Organiques I (Jieping Zhu) Thermodynamic Kinetics Carbonyls Rearrangements |
|
COURS ET EXERCICES DE CHIMIE MINERALE
Cours et exercices de chimie minérale 2 • le 3tritium H (ou T) présent seulement en quantité infime dans l'hydrogène naturel (un atome de tritium pour 10 18 atomes d’hydrogène) Le noyau est constitué d’un proton et de deux neutrons il est radioactif et se transforme en 3 He par émission d'un électron (radioactivité β − |
|
MÉCANISMES RÉACTIONNELS EN CHIMIE ORGANIQUE
La chimie organiqueest la chimie du carbone et de l’hydrogène Elle recense l’ensemble des réactions chimiques permettant de construire le squelette carboné d’une molécule ou de modifier ses groupements fonctionnels On considère que la chimie organique a débuté en 1828 grâce à la synthèse de l’urée par Friedrich Wöhler |
Quelle est la formule chimique de l’acétate de sodium ?
Acétate de sodium : FDS (Fiches de données de sécurité), certificats d’analyse (CoA) et de qualité (CoQ), dossiers, brochures et autres documents disponibles. Nº CAS: 127-09-3 Numéro CE: 204-823-8 Masse molaire: 82.03 g/mol Formule chimique: CH₃COONa Formule de Hill: C₂H₃NaO₂ Grade: ACS,Reag. Ph Eur ACS,Reag.
Quelle est la masse volumique de l'acétone de sodium ?
Masse volumique 1,52 g·cm-3(anhydre, 20 °C)[5], 1,42 g·cm-3(trihydrate, 20 °C)[5] T°d'auto-inflammation 607 °C[5] Point d’éclair > 250 °C(anhydre, coupelle fermée)[5] Précautions SIMDUT[6],[7] Acétate de sodium : Produit non contrôlé Ce produit n'est pas contrôlé selon les critères de classification du SIMDUT. Acétate de sodium trihydraté :
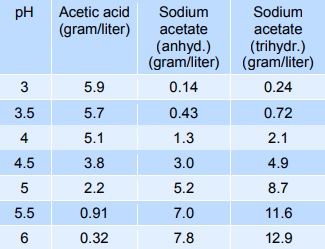
Quelle est la solubilité de l'acide de sodium ?
122 °C(trihydrate) Solubilité 365 g·l-1(eau, 20 °C))[5] Masse volumique 1,52 g·cm-3(anhydre, 20 °C)[5], 1,42 g·cm-3(trihydrate, 20 °C)[5] T°d'auto-inflammation 607 °C[5] Point d’éclair > 250 °C(anhydre, coupelle fermée)[5] Précautions SIMDUT[6],[7] Acétate de sodium : Produit non contrôlé
Quels sont les couples acido-basiques fréquents en chimie organique ?
pKa de couples acido-basiques fréquents en chimie organique. Définition – Nucléophile : espèce ou site d’une molécule pouvant former une liaison en donnant deux électrons. Les sites nucléophiles possèdent au moins un doublet non liant (bases de Lewis) et sont assez électronégatifs ou liés à un atome très peu électronégatif (effet inductif).
|
CHIMIE ORGANIQUE - CORE
nus artificiellement à l'aido des minéraux, une telle détinition par chimie organique l'étude de tous les composés renfermant le t ~ 32, c'est-à-dire que la molécule d'acide acétique l'acide sulfurique, ou être attaqué par le sodium 15 |
|
CHIMIE ORGANIQUE (SUITE)
Référence de ce document : Cours de chimie Organique - G Dupuis - Lycée seuls réactifs organiques, ainsi que de tous les réactifs minéraux et solvants jugés l'iodure ou l'acétate de sodium selon des réactions du second ordre : |
|
PDF 2,55 Mo - INRS
Par exemple, cherchez à sodium (hydroxyde de) au lieu de potassium Lorsque de l'acétylène barbote dans un mélange d'acétate de cuivre (Il) Ann der Chemie, 270, 1892, pp 59- 60 De nombreux acides organiques ou minéraux (ex |
|
29 Produits chimiques organiques
ticipent à la fois de la chimie inorganique et de la chimie organique relèvent du Cha- Acétate d'éthyle (ester de l'acide acétique du no 2915 et de l'alcool éthy- lique) Métahydroxybenzoate de sodium (sel de l'acide métahy- Ces composés peuvent s'obtenir seulement à partir des esters des acides minéraux poly- |



![PDF] Solubility of Sodium Acetate in Ternary Mixtures of Methanol PDF] Solubility of Sodium Acetate in Ternary Mixtures of Methanol](https://upload.wikimedia.org/wikipedia/commons/f/fe/Chilisalpeter_%28Sodium_nitrate%29.jpg)

![PDF] Solubility of Sodium Acetate in Ternary Mixtures of Methanol PDF] Solubility of Sodium Acetate in Ternary Mixtures of Methanol](https://upload.wikimedia.org/wikipedia/commons/thumb/d/d9/Sodium_chloride_dissolution.jpg/1200px-Sodium_chloride_dissolution.jpg)








![PDF] Solubility of Sodium Acetate in Ternary Mixtures of Methanol PDF] Solubility of Sodium Acetate in Ternary Mixtures of Methanol](https://img.yumpu.com/13059979/1/500x640/pdf-file-facultatea-de-chimie-si-inginerie-chimica.jpg)