Exemple de pile electrochimique 3ème Physique
|
3 3C3D1I12CH14 Notion Composition dune pile électrochimique
Points communs et différences entre la pile saline et la pile alcaline : 3 1 La composition de la borne positive est-elle la même dans les 2 types de pile |
|
3ème 21/02/2013
21 fév 2013 · Laurent veut réaliser une pile électrochimique Parmi les schémas qu C'est cette dernière qui servira de modèle pour les piles à combustibles |
|
MANIPULATION 3EME TP4 : LA PILE ELECTROCHIMIQUE
des réactifs est transférée à l'extérieur sous forme d'énergie II TRANSFORMATION CHIMIQUE ET ENERGIE ELECTRIQUE 4 EXEMPLE DE PILE ELECTROCHIMIQUE a |
|
Sommaire
— © Cned Physique - Chimie 3e 86 La différence entre une pile et un accumulateur • Un exemple de pile à combustible : la « pile H2 – O2 » La pile à |
|
Thème : Piles et électrolyses Fiche 4
Dans la pile les cations circulent de la demi pile à l'aluminium vers la demi pile au nickel et les anions en sens inverse ▻ Exercice n°2 1) Les électrons |
|
TP N°10-PROF : LES PILES ELECTROCHIMIQUES
➢ Dans une troisième expérience (qui peut être collective) simuler l'évolution du comportement électrique d'une pile vers son état d'équilibre (décharge) en |
Comment fabriquer une pile électrochimique ?
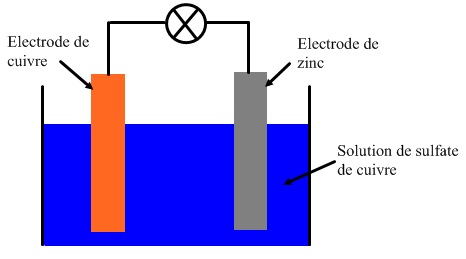
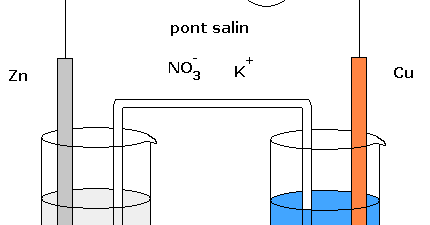
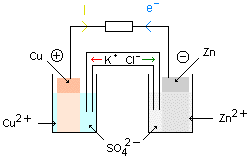
Pour fabriquer une pile électrochimique, il suffit d'immerger deux métaux différents dans des électrolytes contenant leurs propres ions Mn+ , et relier ces deux électrolytes par un pont salin.
C'est quoi une pile électrochimique ?
Une pile électrochimique est le siège d'une réaction d'oxydoréduction spontanée (c'est à dire naturelle) entre deux couples redox.
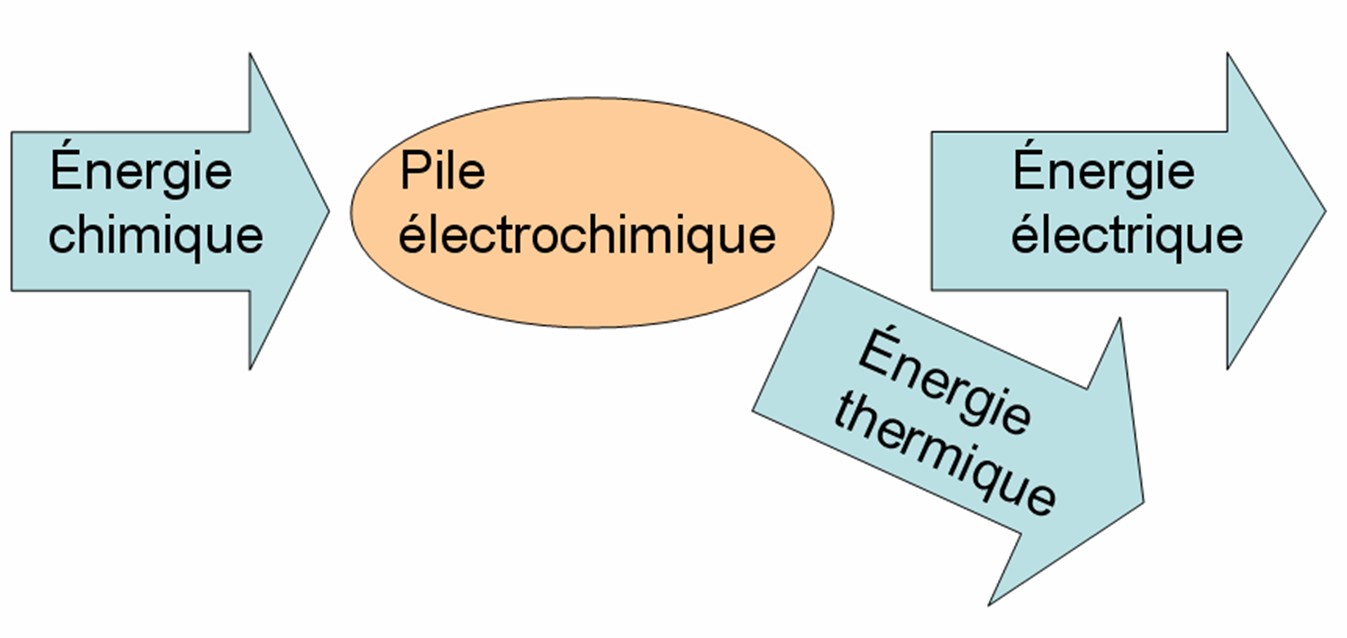
Elle permet la conversion de l'énergie chimique en une autre forme d'énergie.Quelle électrode s'use ?
L'anode (« électrode négative ») s'use jusqu'à sa dégradation totale.
L'anode, complètement usée, stoppe la réaction : Il n'y a plus de circulation d'électrons, il n'y a plus de courant électrique : La réaction étant irréversible.
Cet ensemble constitue alors une « pile ».- Elle s'intéresse aux réactions chimiques, qui dans certaines conditions, créent un mouvement d'électrons et donc un courant électrique.
La pile est un générateur électrochimique.
Ce système permet de fournir de l'électricité à partir de réactions chimiques.
|
Chapitre 2 - Évolution spontanée dun système chimique
en illustrant par l'étude du fonctionnement d'une pile électrochimique. Exemple : N2 + 3H2. 2 NH3. Poisson Florian. Spécialité Physique-Chimie Terminale ... |
|
ANNALES SCIENCES PHYSIQUES 3ème
DES LANGUES NATIONALES. ANNALES. SCIENCES PHYSIQUES. 3ème Chapitre 4 : Un générateur électrochimique : la pile ... L'air est un exemple de gaz. |
|
Chapitre 3 :Oxydoréduction
II Piles électrochimiques œ potentiel redox. A) Pile électrochimique précipitation. Exemple : électrode au Calomel saturé (ECS) ... |
|
Annexe : Principe de fonctionnement et constituants dune batterie
un système électrochimique réversible contrairement aux piles. (par exemple Plomb/Oxyde de plomb |
|
Ressources pour la classe de troisième
A1.5 Pile électrochimique et énergie chimique. A1.5.1 Principe Le présent document est relatif au programme de physique-chimie en vigueur. |
|
Exercice 1 (6 points) La fabrication du verre Exercice 2 (7 points
Une pile électrochimique convertit l'énergie chimique en énergie électrique. exemple le cuivre (Cu) a une plus grande tendance à perdre des électrons ... |
|
Lénergie chimique et ses conversions
Lorsque la pile fonctionne il se produit une transformation chimique. Une partie de l'énergie chimique contenue dans les réactifs est transférée au circuit |
|
Ressource daccompagnement de lancien programme de physique
des programmes de physique-chimie publiés en 2008. A ce titre elle A1.5 Pile électrochimique et énergie chimique. A1.5.1 Principe. |
|
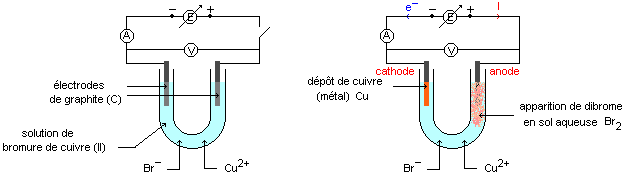
Oxydoréduction (2ème partie)
b- Exemples de piles ou cellules galvaniques . La chaîne électrochimique de l'électrode au calomel est : ... iii- Electrode de troisième espèce. |
|
Etude et réalisation dune pile électrochimique.pdf
1 : Quelques degrés d'oxydation possibles avec des exemples simples pour différents éléments. *degré d'oxydation moyen. II.3. Définition de l'oxydation et de la |
Quel est le principe d'une pile électrochimique ?
. Une pile transforme une partie de l'énergie provenant de cette réaction chimique en énergie électrique.
Comment fonctionne une pile electrolytique ?
. Elles sont reliées au circuit électrique, par lesquelles entre ou sort le courant électrique.
. L'électrolyte est une solution aqueuse conductrice qui permet la circulation des ions.
Pourquoi Parle-t-on de pile électrochimique ?
Comment faire une pile Physique-chimie ?
|
Chap4 Pile électrochimique et énergie chimique
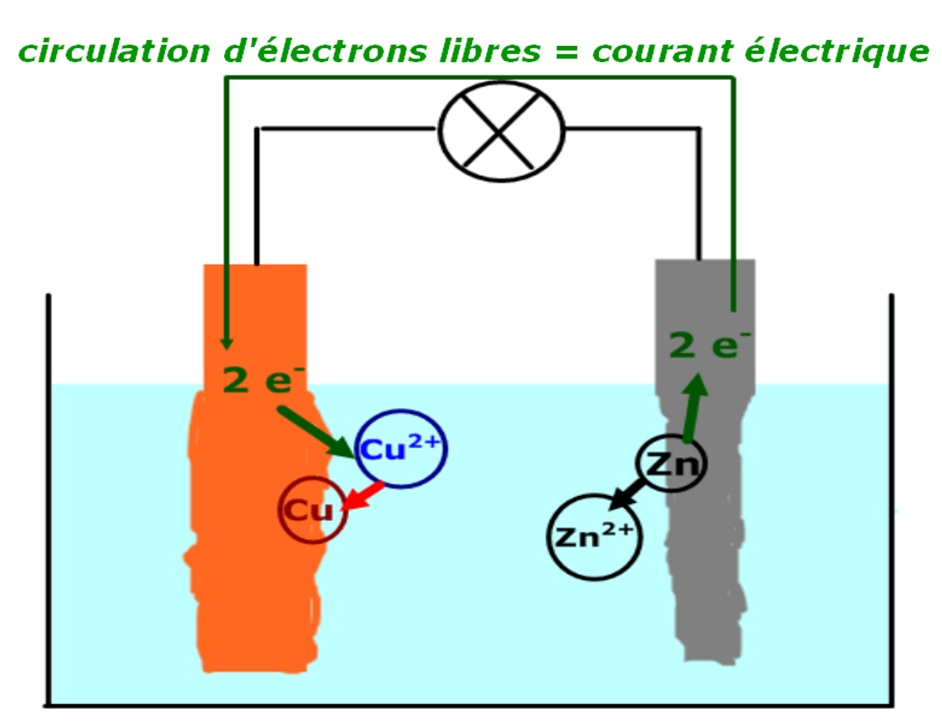
L'énergie mise en jeu dans une pile provient d'une réaction chimique : la consommation de galvanoplastie, par exemple pour argenter du cuivre A B Cu Zn |
|
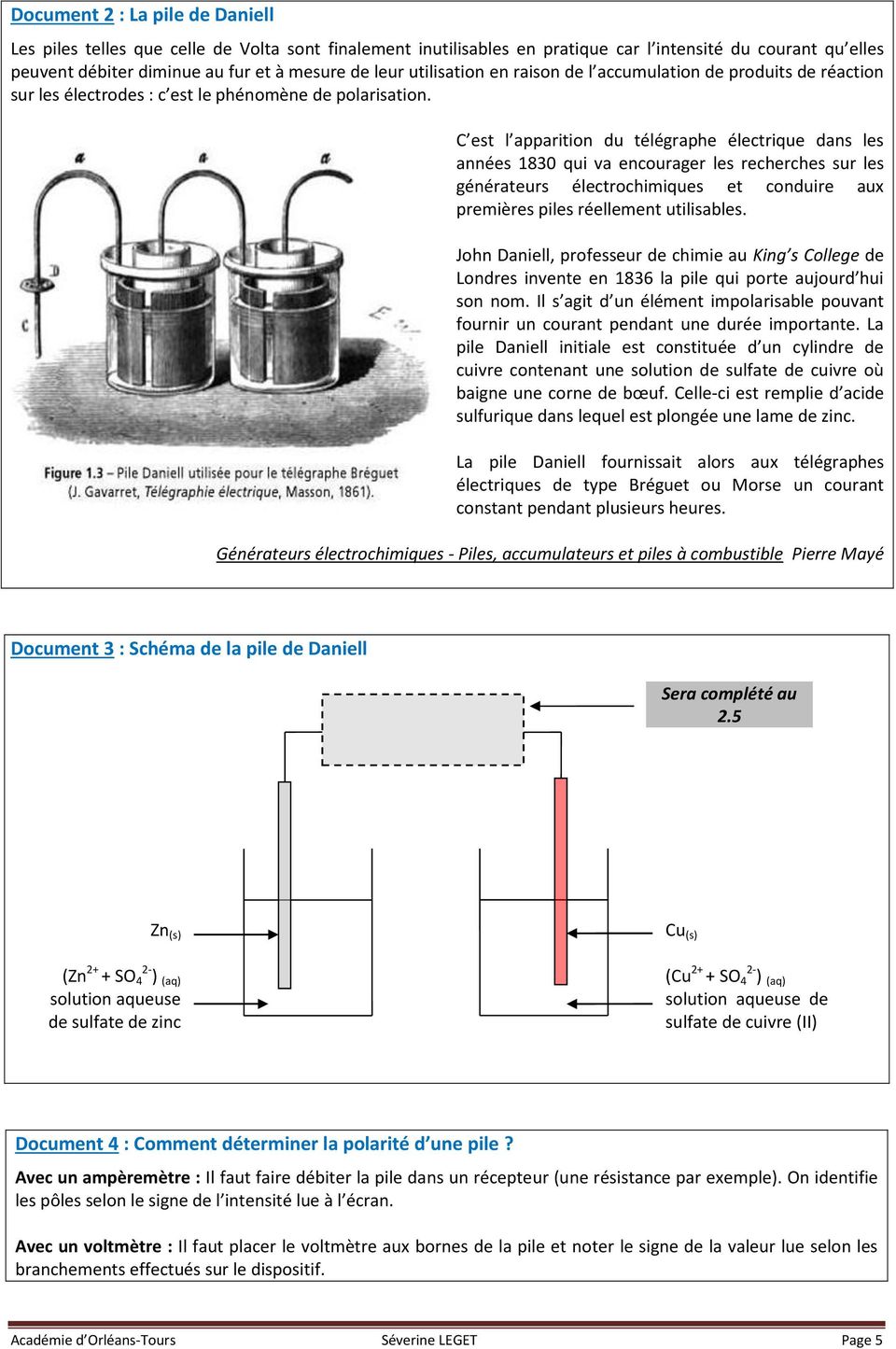
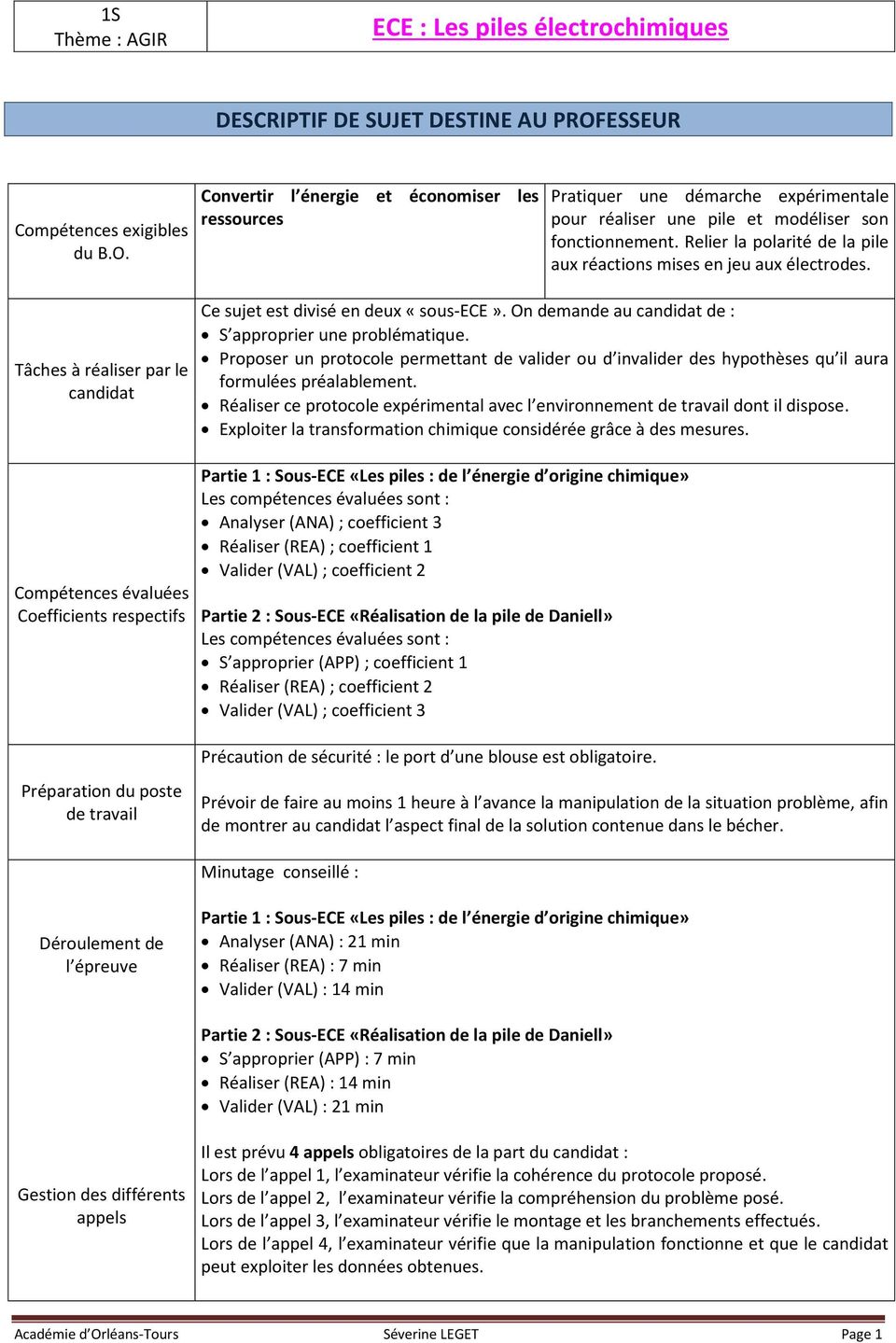
ECE : Les piles électrochimiques - Académie dOrléans-Tours
Royale de Physique à Londres, le 20 mars 1800, Générateurs électrochimiques - Piles, accumulateurs et piles à combustible Pierre Mayé Avec un ampèremètre : Il faut faire débiter la pile dans un récepteur (une résistance par exemple) |
|
TP N°10-PROF : LES PILES ELECTROCHIMIQUES - Physagreg
Montrer qu'une pile délivre un courant en circuit fermé Utiliser le critère Dans une troisième expérience (qui peut être collective), simuler l'évolution du comportement électrique préférable de lui associer une résistance, par exemple 22 Ω |
|
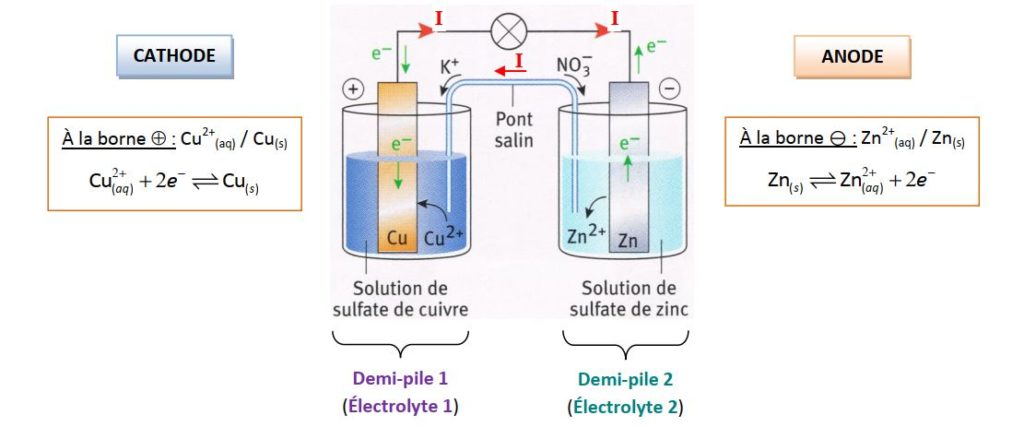
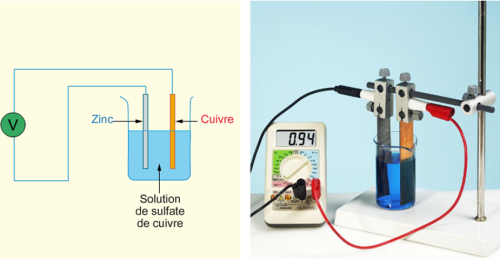
10-Les piles électrochimiques - Physagreg
Chimie 2 2) Exemple : la pile Daniell : Voir TPχn°10 Expérience 2 3) Constitution d'une pile : ➢ Chaque pile électrochimique est constituée de deux demi-piles |
|
Piles électrochimiques et énergie chimique - Chapitre 1 : Le circuit
Eric Fourel, certifié de sciences physiques 2008 Chapitre 5 : Piles électrochimiques et énergie chimique Les métaux ions zinc par exemple) Remarque: Le |
|
Fiche pédagogique enseignant CHIMIE Les piles électrochimiques
Fiche professeur et fiche élève pour l'activité 3 : Quels sont les facteurs qui influencent la fém d'une pile ? TP n°10 « facteurs influençant la fém d'une pile |
|
Epreuves communes de Sciences Epreuves communes de
21 fév 2013 · Sens de déplacement des ions chlorures Sens de déplacement des ions sodium Page 3 3 Exercice n°3 Exercice n°3 : Pile électrochimique : |
|
Les Piles
conversion électrochimique d'énergie dans les deux sens de Londres, devait imposer un modèle de pile d'une tension constante On lui ajoute parfois les termes cathodes liquides ou cathodes solides, insistant sur l'état physique I GILLET, La pile à combustion électrochimique : une ouverture sur le 3ème millénaire |
|
Ressources pour la classe de troisième - Espace pédagogique
A1 5 Pile électrochimique et énergie chimique l'enseignement des sciences physiques et chimiques fondamentales et appliquées (voir ANNEXE par exemple, le zinc est transformé en ions zinc (II) dans la pile ordinaire du commerce On |
|
Filière sciences de la matière Cours délectrochimie SMC Semestre 5
Relation entre potentiel de pile et activités des corps dissous I 3 Variation de Propriétés physiques du mercure I 3 3ème cas : Si les deux formes sont solides b EXEMPLE : Tracé du diagramme tension – pH du cuivre – eau à 25° C à |