chapitre 1 acide fort base forte
|
Les acides et les bases
Les acides forts et les bases fortes • une base forte est un électrolyte fort qui s’ionise complètement dans l’eau • ex ; n’importe quel hydroxyded’un métal alcalin (ex ; NaOH) • une base faible est un électrolyte faible qui ne s’ionise que très peu dans l’eau • ex ; NH 3 (aq) + H 2 O(l) NH 4 +(aq) + OH-(aq) |
|
TITRE ACIDE FORT – BASE FORTE OS 3 Moyens
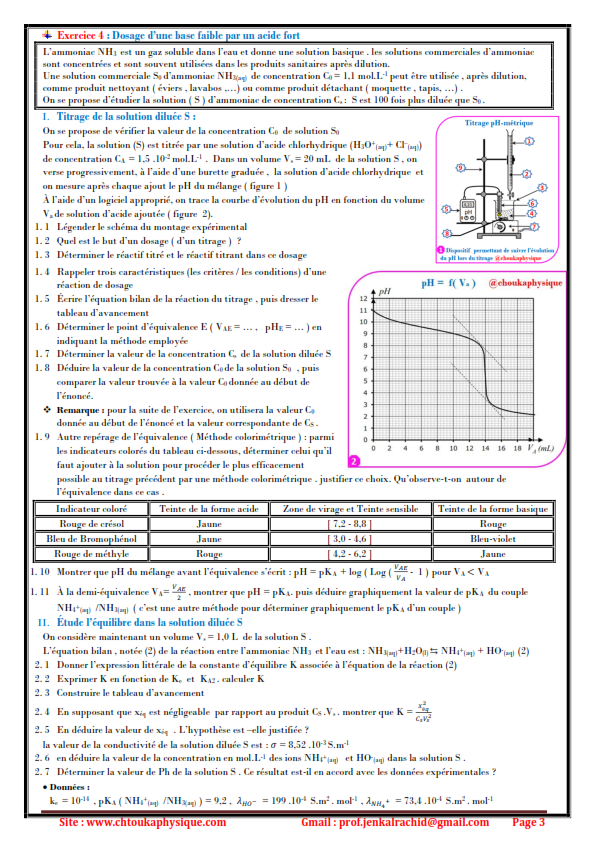
COURS DE REACTIONS ACIDE-BASE TITRE: ACIDE FORT – BASE FORTE Durée: 4 H Objectifs spécifiques: OS 3: Définir les notions d’acide fort et de base forte à partir des solutions aqueuses de chlorure d’hydrogène et d’hydroxyde de sodium OS 7: Interpréter la courbe de variation du pH au cours d’une réaction acide-base Moyens: |
|
Dosage acide fort
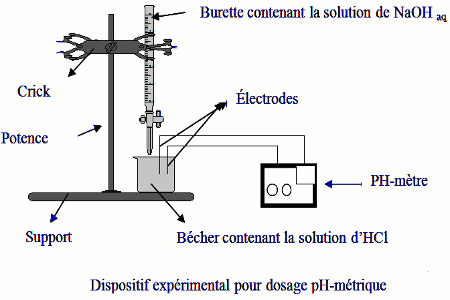
Université du Maine - Faculté des Sciences Acide fort - base forte 1 Dosage acide fort – base forte Acide fort HA : titré concentration (à déterminer) c a volume v a: HA H O →H O ++ A − 2 3 Base forte NaOH titrant concentration c b volume v b (à verser à la burette) : NaOH →Na + +OH − |
Comment calculer la quantité d’acide dans une solution ?
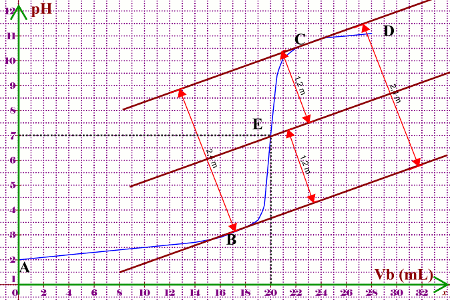
La méthode consiste à déterminer la quantité d’acide dans une solution en y ajoutant une quantité équivalente d’une base, ou vice-versa. un volume V0 connu d’une solution d’acide de concentration inconnue ca on ajoute progressivement une solution de base de concentration connue ctitr .
Quelle est la différence entre acide fort et base forte ?
acide fort / base forte (Ca= Cb; Va= 10 mL) Vb(mL) 0 5 10 15 20 pH 0 2 4 6 8 10 12 14 Ca = 10 -1M Ca = 10 -2M Ca = 10 -3M Ca = 10 -4M pH = pHéquiv= 7 Vb= Vb équiv Title Dosage acide fort - base forte\r Author
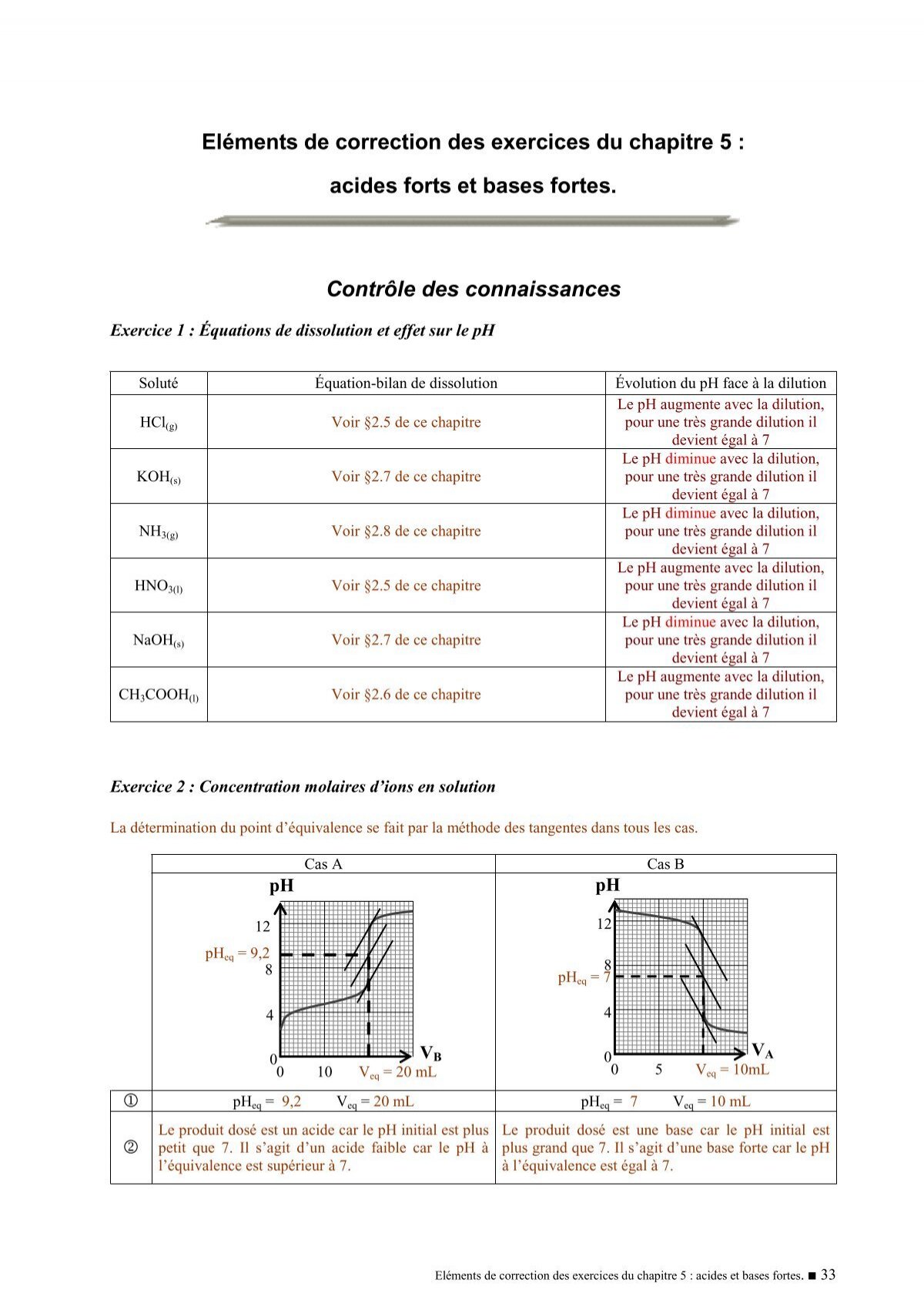
Quel est le point d'équivalence du titrage d'une base forte par un acide fort ?
Dans le cas du titrage d’une base forte par un acide fort, la courbe de neutralisation varie lentement pendant l’addition de l’acide, puis présente une partie quasi-verticale pendant laquelle le pH change brusquement de plusieurs unités. Le pH du point d’équivalence est encore égal à 7.
Quelle est la formule générale des acides aminés ?
Leur formule générale est de la forme: Le groupement R est soit un H soit un alkyle. Ils comportent donc une fonction carboxyle, donc un acide et une fonction amine, donc une base. Au niveau acido-basique les acides aminés sont en général le siège de deux équilibres acido-basiques fondamentaux.

Acides forts bases fortes pH et solutions tampons

Calculer le pH dune base forte & dun acide fort

Calcul de pH : FORMULES & CONDITIONS
|
COURS DE CHIMIE GENERALE Semestre 1 SVI - Université Cadi
Titrages acide-base 1 1 Titrage d'un acide fort par une base forte 1 2 Titrage d' un acide faible par une base forte CHAPITRE III : REACTIONS D'OXYDO- |
|
Chapitre 1 Acides et bases
Un acide est dit : — fort dans l'eau ssi il est totalement dissocié dans l'eau ssi Ka > 1 ssi pKa < 0; — faible ssi la dissociation est une réaction équilibrée ssi pKa > |
|
Révisions sur les acides et les bases - Nicole Cortial
donc la base la plus forte, dans l'eau Les couples acide faible / base faible ont tous des constantes d'acidité comprises entre 1 et 14 10 |
|
Transformations chimiques en solution aqueuse - Chimie en PCSI
Chapitre SA1_PSI : Réactions acide-‐base Cours de LES ACIDES FORTS ET LES BASES FORTES 8 2 formule et nature – faible ou forte – des acides |
|
Force des acides et des bases - Lycée dAdultes
4 3 1 Acide fort ou faible - Base forte ou faible avec le chapitre2 sur le sens d' évolution spontanée d'une réaction chimique Le chapitre se découpe selon le |
|
Acides forts et bases fortes
Chapitre 5 Sciences Physiques - BTS Acides forts et bases fortes 1 Définitions 1 1 Théorie de Bronsted et Lowry ( 1923) Un acide libère des protons H+ pour |
|
VIEtude sommaire des mélanges
Acides et bases Chapitre VI 82 Cette approximation grossière n'est justifiée que si l'apport d'ions hydroxyde par la base faible est négligeable par rapport à |
|
Chap TS acide-base
Comparaison du comportement des acides en solution aqueuse : 1) Forces relatives de deux acides : Un acide faible A1H est plus fort qu'un autre acide faible |
|
Chapitre 1 : Les acides et les bases
Le pH d'une solution aqueuse d'acide fort de concentration en soluté apporté c0 ( en mol L –1) est : pH = – log c0 - Cas d'une base forte : Tout comme l'acide |
|
Le pH 3 Le pH des acides et bases forts - théorie - 2014
A la fin de ce chapitre vous devrez être capable de • Déterminer si une espèce chimique est un acide fort, un acide faible, une base forte ou une base faible |









![corrige-livre-chimie-par-[-wwwheights-bookblogspotcom-]-Flip corrige-livre-chimie-par-[-wwwheights-bookblogspotcom-]-Flip](http://pcracine.free.fr/local/cache-vignettes/L520xH256/Capture02-2-5c271.png)