base forte liste
|
Fiche de révisions sur les acides et les bases
• L’hydroxyde de sodium (ou soude) est une base forte : NaOH( s) Na aq OH aq → + + − • L’hydroxyde de potassium (ou potasse) est une base forte : KOH( s) K aq OH aq → + + − Exemples de réactions de dissolution de bases et d’acides faibles: • L’acide éthanoïque (CH3 COOH) est un acide faible : CH3 COOH(liq) H 2 O H3 O aq |
|
Les acides et les bases
• une base forte est un électrolyte fort qui s’ionise complètement dans l’eau • ex ; n’importe quel hydroxyded’un métal alcalin (ex ; NaOH) • une base faible est un électrolyte faible qui ne s’ionise que très peu dans l’eau • ex ; NH 3 (aq) + H 2 O(l) NH 4 +(aq) + OH-(aq) |
Quelle est la différence entre un acide fort et une base forte ?
• Un acide fort est un acide réagissant totalement avec l’eau. Si sa concentration est c, alors . • Un acide faible AH réagit avec l’eau selon une réaction limitée . • Une base forte réagit avec l’eau selon une réaction totale. Pour une concentration c, on a . • Une base faible A– réagit avec l’eau selon une réaction limitée .
Quels sont les acides forts ?
Un acide fort donne 100 % de H3O+ et de A- lorsque l’acide s’ionise dans l’eau ; la figure 5.3.1 énumère plusieurs acides forts. Si nous commençons avec 0,1 M HCl, à l’équilibre nous obtenons 0,1 M H3O+ et 0,1 M Cl–. Selon la définition de Brønsted-Lowry, en tant qu’acide fort, le HCl est un très bon donneur de protons.
Quelle est la différence entre une base forte et une base faible ?
Base forte - base faible Toujours selon Brønsted, une base est une espèce chimique susceptible de capter un ou plusieurs protons . Dans la pratique, ces protons peuvent être pris à des molécules d’eau, formant alors des ions hydroxydes . On prendra en compte ici uniquement des monobases.
|
Les acides et bases en solution aqueuse.
d'identifier dans une liste donnée |
|
Fiche de révisions sur les acides et les bases
donc la base la plus forte dans l'eau. Les couples acide faible / base faible ont tous des constantes d'acidité comprises entre 1 et. 14. 10. |
|
Acides forts et bases fortes
Un acide libère des protons H+ pour former des ions oxonium ( ou hydronium) H3O+. Une base capte des protons H+. 1.2. Exemples. Dissolution du chlorure d' |
|
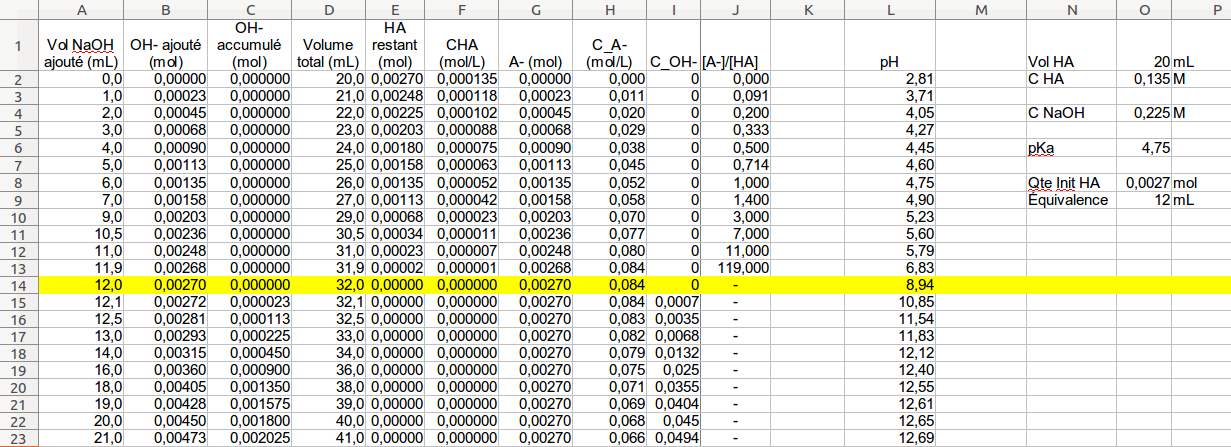
Cours de Chimie - Informatique Titrage acide/base
17 avr. 2013 1.6 Liste des plages nommées. Titrage acide/base. Figure 5 Courbe de titrage d'un acide fort par une base forte. |
|
135.Quel est le mode de calcul? 1) Afin de répartir les sièges entre
2) Répartition du siège restant au plus fort reste : Pour calculer le plus fort reste on soustrait du nombre de voix de chaque liste le total des quotients. |
|
Liste Verbes Irréguliers 4ème Enjoy BV (base verbale) V-ED
Comment apprendre les verbes irréguliers en anglais? Dans la liste ci-dessus surligne les cases des verbes à apprendre dans la colonne de gauche. Révise |
|
Liste Verbes Irréguliers 3ème Enjoy BV (base verbale) V-ED
Comment apprendre les verbes irréguliers en anglais? Dans la liste ci-dessus surligne les cases des verbes à apprendre dans la colonne de gauche. |
|
MANUEL BELGE DE RÉGULATION POMPIER
questionnement de base » l'opérateur peut identifier un « protocole spécifique ». Il en existe 40 qui sont basés sur les sous-catégories de la liste des |
|
COMMISSION EUROPÉENNE Bruxelles le 3.9.2020 COM(2020
3 sept. 2020 matières premières y compris les métaux de base |
|
LISTE DES PRIX DES PRINCIPALES OPERATIONS BANCAIRES
Le taux d'intérêt débiteur est exprimé sur base annuelle et peut être modifié à tout moment par la banque. Les clients CBC sont informés de toute |
|
Acides forts et bases fortes
d'un acide fort par une base forte 4 1 But d'un dosage Le but est de déterminer la concentration |
|
Les acides et bases en solution aqueuse - Groupe Transition
ifier, dans une liste donnée, les acides et les bases selon b) NaOH est une base forte H2O |
|
Révisions sur les acides et les bases - Nicole Cortial
base la plus forte, dans l'eau Les couples acide faible / base faible ont tous des constantes d' |
|
COURS DE CHIMIE GENERALE Semestre 1 SVI - Université
n acide fort 2 2 Cas d'un acide faible 2 3 Cas d'une base forte 2 4 Cas des bases faibles 2 5 |
|
Transformations chimiques en solution aqueuse - Chimie en
LA REACTION ACIDE/BASE 8 1 LES ACIDES FORTS ET LES BASES FORTES 8 2 LES ACIDES |
|
Déterminer si une base est fort ou faible
e est forte si elle se dissocie totalement lors de sa mise en solution On a alors la relation |
|
Chapitre 1 Acides et bases
init le pKa du couple acide/base : pKa = −log (Ka) Un acide est dit : — fort dans l'eau ssi il est |
|
Les acides et les bases
st-ce qu'une base forte ou faible ? ▫ E Calculs de la concentration des acides (Tableau et |
|
PH et pKa - Eli Zysman-Colman
e solution de base forte pH = 14 + log [B] 8 Calcul de pH Formule générale pour le pH de |