 Activité documentaire
Activité documentaire
3 – Quelle est la différence entre l'écriture vue en 4ème (atome et molécules) et les formules des ions ? 4 – A la découverte de la formation des ions : Qu'est-
 Activité documentaire
Activité documentaire
Identifier les ions présents dans une solution de médicaments. La présence d'un ion peut être mise en évidence par la formation d'un précipité provoquée par.
 ACTIVITE 5 comment se forme un ion
ACTIVITE 5 comment se forme un ion
Un ion est un atome ayant gagné ou perdu 1 ou plusieurs électrons. CHIMIE CHAPITRE 3 : Conduction des solutions ACTIVITE 5 : De quoi est constitué un ...
 Activité. Comment reconnaître certains ions ? Ton travail : Diapo 3 (à
Activité. Comment reconnaître certains ions ? Ton travail : Diapo 3 (à
(ici l'espèce chimique à identifier sera un ion). Diapo 2 (à 22 sec) : 1) Comment s'appelle la solution permettant de faire un test ?
 Activité 3-Etude documentaire-Et le principe de neutralité de la
Activité 3-Etude documentaire-Et le principe de neutralité de la
Ex : Le chlorure de sodium composé d'un ion sodium Na+ et d'un ion chlorure Cl –. Ce qui donne la formule chimique NaCl. Avec le puzzle ionique
 Activité 2-Etude documentaire : Comment mettre en évidence la
Activité 2-Etude documentaire : Comment mettre en évidence la
3ème. Activité 2-Etude documentaire : Comment mettre en évidence la présence d'ions ? Etape 1 : Prélever quelques mL de la solution à tester.
 Chapitre 5 : Atomes et ions I –Latome 1. Histoire de latome Activité
Chapitre 5 : Atomes et ions I –Latome 1. Histoire de latome Activité
Histoire de l'atome. Activité documentaire 1 p 136 (à faire via pronote). Depuis toujours les savants se sont intéressés à déterminer la composition de.
 Atomes-et-Ions-Activité-correction-3ème.pdf
Atomes-et-Ions-Activité-correction-3ème.pdf
b) La charge de cet ion est -1. 2. Utiliser un modèle. Correction : La formule chimique de l'ion nitrate est : NO3.
 ACTIVITE N°3 ions -tests caractéristiques
ACTIVITE N°3 ions -tests caractéristiques
Faire de même pour l'ion chlorure. 3°> Les solutions ioniques contiennent des ions (espèces chargées) mais sont électriquement neutre expliquer pourquoi.
 Correction de lactivité 1 page 122 – (énoncé en page 2) 1/ Un ion
Correction de lactivité 1 page 122 – (énoncé en page 2) 1/ Un ion
2/ L'atome et l'ion magnésium ont le même nombre de protons mais n'ont pas le même nombre d'électrons. 3/ La charge électrique de l'ion fluorure vaut. -1 ( 1
 Chapitre : LES IONS - ac-reunionfr
Chapitre : LES IONS - ac-reunionfr
Activité documentaire P122 Définition : Un ion est un atome ou groupe d’atomes qui a perdu ou gagné un ou plusieurs électrons Un ion n’est donc pas neutre il porte une charge électrique On distingue deux types d’ions : Les ions positifs ou cations Lorsqu’un atome ou un groupe d’atome perd un ou plusieurs électrons il devient
Quels sont les différents types d’ions ?
Un ion n’est donc pas neutre, il porte une charge électrique. On distingue deux types d’ions : Les ions positifs ou cations Lorsqu’un atome ou un groupe d’atome perd un ou plusieurs électrons, il devient un ion chargé positivement ou un cation. Exemple : L’ion magnésium
Comment identifier les ions présents dans une solution ?
Identifier les ions présents dans une solution en effectuant les tests nécessaires. Classe concernée CAP Durée d’utilisation 1 heure Ordre dans la séquence ou période La notion d’ion a été traitée au préalable. Type de document Activité cours Evaluation TP Fiche matériel
Quels sont les exemples d’atomes qui donnent des anions en solutions ?
Lorsqu’un atome gagne un ou plusieurs électrons, il se charge négativement et forme un ion négatif appelé anion. Voici d’autres exemples d’atomes qui donnent des anions en solutions : La formule chimique d’un ion nous renseigne sur le nombre d’électrons gagnés ou perdus par l’atome pour le former. L’atome et l’ion ont le même numéro atomique Z.
Pourquoi les ions sont-ils libres de se déplacer sous l’effet de la tension électrique ?
Ces ions sont libres de se déplacer sous l’effet de la tension électrique : c’est ce qui explique la conduction électrique d’une solution ionique. Les cations se dirigent vers la borne négative alors que les anions se dirigent vers la borne positive. Pour visualiser ce déplacement d’ions, on réalise le test de migration des ions.
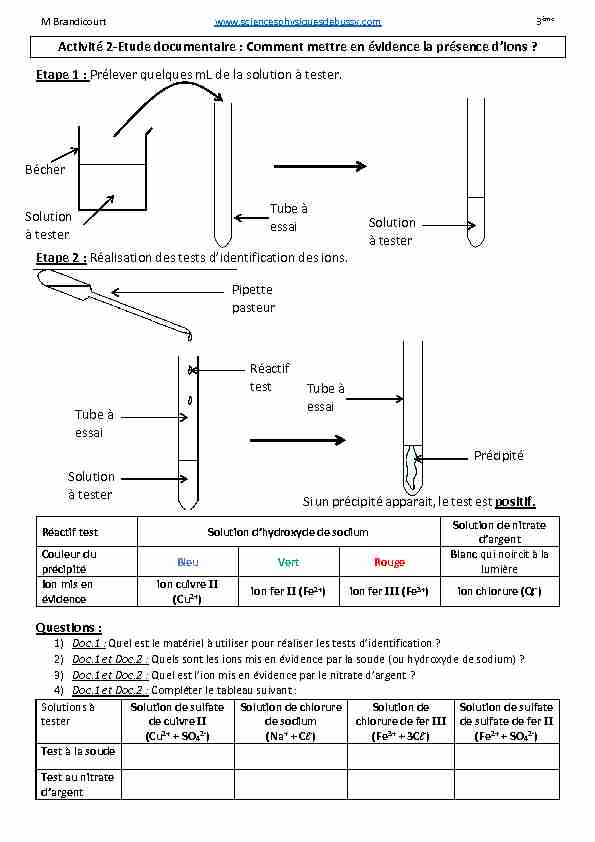 M Brandicourt www.sciencesphysiquesdebussy.com 3ème Activité 2-Etude documentaire ͗ Comment mettre en Ġǀidence la prĠsence d'ions ? Etape 1 : Prélever quelques mL de la solution à tester. Etape 2 : Réalisation des tests d'identification des ions. Réactif test Solution d'hydrodžyde de sodium Solution de nitrate d'argent
M Brandicourt www.sciencesphysiquesdebussy.com 3ème Activité 2-Etude documentaire ͗ Comment mettre en Ġǀidence la prĠsence d'ions ? Etape 1 : Prélever quelques mL de la solution à tester. Etape 2 : Réalisation des tests d'identification des ions. Réactif test Solution d'hydrodžyde de sodium Solution de nitrate d'argent Couleur du
précipité Bleu Vert Rouge Blanc qui noircit à la lumièreIon mis en
évidence
ion cuivre II (Cu2+) ion fer II (Fe2+) ion fer III (Fe3+) ion chlorure (Cl -)Questions :
1) Doc.1 : Quel est le matériel à utiliser pour réaliser les tests d'identification ?
2) Doc.1 et Doc.2 : Quels sont les ions mis en évidence par la soude (ou hydroxyde de sodium) ?
3) Doc.1 et Doc.2 : Yuel est l'ion mis en Ġǀidence par le nitrate d'argent ?
4) Doc.1 et Doc.2 : Compléter le tableau suivant :
Solutions à
testerSolution de sulfate
de cuivre II (Cu2+ + SO42-)Solution de chlorure
de sodium (Na+ + Cl-)Solution de
chlorure de fer III (Fe3+ + 3Cl-)Solution de sulfate
de sulfate de fer II (Fe2+ + SO42-)Test à la soude
Test au nitrate
d'argent Si un précipité apparait, le test est positif.Tube à
essaiSolution
à tester
Pipette
pasteurRéactif
testTube à
essaiPrécipité
Solution
à tester
Solution
à tester
Tube à
essaiBécher
M Brandicourt www.sciencesphysiquesdebussy.com 3ème Activité 2-Etude documentaire ͗ Comment mettre en Ġǀidence la prĠsence d'ions ? Etape 1 : Prélever quelques mL de la solution à tester. Etape 2 : Réalisation des tests d'identification des ions. Réactif test Solution d'hydrodžyde de sodium Solution de nitrate d'argentCouleur du
précipité Bleu Vert Rouge Blanc qui noircit à la lumièreIon mis en
évidence
ion cuivre II (Cu2+) ion fer II (Fe2+) ion fer III (Fe3+) ion chlorure (Cl -)Questions :
1) Doc.1 : Quel est le matériel à utiliser pour réaliser les tests d'identification ?
2) Doc.1 et Doc.2 : Quels sont les ions mis en évidence par la soude (ou hydroxyde de sodium) ?
3) Doc.1 et Doc.2 : Yuel est l'ion mis en Ġǀidence par le nitrate d'argent ?
4) Doc.1 et Doc.2 : Compléter le tableau suivant :
Solutions à
testerSolution de sulfate
de cuivre II (Cu2+ + SO42-)Solution de chlorure
de sodium (Na+ + Cl-)Solution de
chlorure de fer III (Fe3+ + 3Cl-)Solution de sulfate
de sulfate de fer II (Fe2+ + SO42-)Test à la soude
Test au nitrate
d'argent Si un précipité apparait, le test est positif.Tube à
essaiSolution
à tester
Pipette
pasteurRéactif
testTube à
essaiPrécipité
Solution
à tester
Solution
à tester
Tube à
essaiBécher
quotesdbs_dbs30.pdfusesText_36[PDF] differences linux unix
[PDF] exercice corrigé commande linux pdf
[PDF] cours systeme d'exploitation unix pdf
[PDF] tp linux avec correction
[PDF] examen linux avec correction
[PDF] la différence entre linux et unix wikipedia
[PDF] cours unix debutant pdf
[PDF] l expression oral au primaire
[PDF] cours sur les batteries daccumulateurs
[PDF] cours piles et accumulateurs sti2d
[PDF] courbe décharge batterie plomb
[PDF] cours batterie pdf
[PDF] charge et décharge dun accumulateur au plomb
[PDF] j'en prends note signification
