 RÈGLEMENT (UE) No 536/2014 DU PARLEMENT EUROPÉEN ET
RÈGLEMENT (UE) No 536/2014 DU PARLEMENT EUROPÉEN ET
27 мая 2014 г. nues lors de l'essai clinique (ci-après dénommées «bonnes pratiques de fabrication»). ... essai clinique et les procédures de levée de l'insu s' ...
 RÈGLEMENT DEXÉCUTION (UE) 2017/ 556 DE LA COMMISSION
RÈGLEMENT DEXÉCUTION (UE) 2017/ 556 DE LA COMMISSION
25 мар. 2017 г. ... procédures d'inspection en matière de bonnes pratiques cliniques et ... pratiques cliniques relatives aux essais cliniques
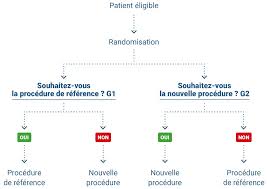 Méthodologie pour le développement clinique des dispositifs
Méthodologie pour le développement clinique des dispositifs
8 июн. 2021 г. Un manque d'expérience peut influencer le résultat de l'essai en pénalisant la nouvelle thérapeutique tes- tée (biais de performance) (39).
 Guide de Bonnes Pratiques en Recherche Clinique
Guide de Bonnes Pratiques en Recherche Clinique
Cliniques et des procédures opératoires standards de l'essai. Il est recruté essai clinique et dont l'investigateur n'a plus de nouvelles. Plus le nombre ...
 Bonnes pratiques de participation - Directives pour les essais de
Bonnes pratiques de participation - Directives pour les essais de
La disponibilité des produits ou des procédures nouvelle- ment identifiés Cycle d'un essai : Ensemble du processus d'essai clinique qui commence par ...
 Le système européen de réglementation des médicaments
Le système européen de réglementation des médicaments
L'EMA et les États membres coopèrent et partagent leur ex- pertise en matière d'évaluation des nouveaux médicaments et de nouvelles données en matière de
 LES ESSAIS CLINIQUES EN 10 QUESTIONS
LES ESSAIS CLINIQUES EN 10 QUESTIONS
5 дек. 2018 г. Les essais cliniques sont la phase "pivot" du développement d'un médicament : après les phases de recherche en laboratoire et sur les ...
 Du laboratoire au patient:
Du laboratoire au patient:
Les nouveaux médicaments potentiels sont d'abord testés en laboratoire puis sur des volontaires humains
 Pratique des essais cliniques en Afrique
Pratique des essais cliniques en Afrique
Cerre supervision du processus de l'essai clinique consisre en une vérification scrupuleuse des procédures. Observance du protocole _ respect des critères
 entrée en vigueur du règlement européen sur les essais cliniques
entrée en vigueur du règlement européen sur les essais cliniques
4 окт. 2022 г. participant à l'essai clinique ; ou c) outre la pratique clinique normale des procédures de diagnostic ou de surveillance s'appliquent aux ...
 RÈGLEMENT (UE) No 536/2014 DU PARLEMENT EUROPÉEN ET
RÈGLEMENT (UE) No 536/2014 DU PARLEMENT EUROPÉEN ET
27 mai 2014 Les nouvelles procédures d'autorisation d'es sais cliniques ... Par rapport à la pratique clinique normale de nombreux essais clini.
 LES ESSAIS CLINIQUES EN 10 QUESTIONS
LES ESSAIS CLINIQUES EN 10 QUESTIONS
5 déc. 2018 explique pourquoi il est nécessaire d'entreprendre cette nouvelle recherche. En pratique il doit : • avoir une légitimité scientifique (se ...
 Guide de Bonnes Pratiques en Recherche Clinique
Guide de Bonnes Pratiques en Recherche Clinique
Dans un essai clinique le moniteur doit veiller au respect des droits des patients
 Module 7 - Utiliser les méthodes damélioration de la qualité pour
Module 7 - Utiliser les méthodes damélioration de la qualité pour
constitue la référence pour la recherche clinique. La profonde des processus de soins des patients ainsi ... l'amélioration car disposer de nouvelles.
 Une nouvelle ère pour la recherche clinique en Europe: le
Une nouvelle ère pour la recherche clinique en Europe: le
15 fév. 2019 Procédure d'autorisation de l'essai clinique (Chapitre II ... médicament en dehors de la pratique clinique courante et en vertu d'un ...
 Essais cliniques production de la preuve et mutations de la
Essais cliniques production de la preuve et mutations de la
impliqué d'adapter les procédures ou d'en inventer de nouvelles
 Bonnes pratiques de participation - Directives pour les essais de
Bonnes pratiques de participation - Directives pour les essais de
3.16 Accès aux produits et procédures de l'essai une fois pratiques cliniques2
 LES ESSAIS CLINIQUES EN 12 QUESTIONS
LES ESSAIS CLINIQUES EN 12 QUESTIONS
27 mai 2014 explique pourquoi il est nécessaire d'entreprendre cette nouvelle recherche. En pratique il doit : ? avoir une légitimité scientifique (se ...
 Méthodologie pour le développement clinique des dispositifs
Méthodologie pour le développement clinique des dispositifs
8 jui. 2021 recherche bibliographique : veille de la recherche effectuée en 2013 et nouvelle re- cherche sur les thématiques complémentaires ...
 loi n° 28-13 relative à la protection des personnes participant aux
loi n° 28-13 relative à la protection des personnes participant aux
Toute recherche ou essai organisé et pratiqué sur l'être soit des essais cliniques portant sur des médicaments expérimentaux ou des investigations ...
 LES ESSAIS CLINIQUES EN 10 QUESTIONS - Leem
LES ESSAIS CLINIQUES EN 10 QUESTIONS - Leem
Les essais cliniques constituent la phase ultime du développement d’un médicament après les essais précliniques Les participants à ces essais permettent ainsi la mise à disposition pour tous des nouveaux traitements et bénéficient quant à eux d’un accès précoce à ces innovations 1
 « Essais cliniques 2030 - Leem
« Essais cliniques 2030 - Leem
Les évolutions des essais cliniques Nouvelles technologies de santé > Médicaments de Thérapie Innovante > Médicaments associés: - à des biomarqueurs - à un dispositif médical + service Nouvelles méthodologies > Nouveaux designs des essais > Intégration de bras virtuels > Combinaison au recueil en vie réelle Nouvelles modalités de
[PDF] Droit de la protection de l adulte
[PDF] BAPAAT - BPJEPS - DEJEPS - DES JEPS BAPAAT BP JEPS DE JEPS DES JEPS
[PDF] TABLE DES MATIÈRES PAGE
[PDF] Propositions d orientations pour la CAI du mandat 2014-2015
[PDF] FICHE DE SYNTHÈSE. Intitulé du projet
[PDF] Cette gestion se trouve compliquée :
[PDF] Comment atteindre ses objectifs de façon certaine
[PDF] GUIDE DE LAPPRENTI PREPARATEUR EN PHARMACIE CFA. de GUILHERAND-GRANGES 07500
[PDF] Les institutions représentatives du personnel
[PDF] Partenariat EFIDIS Emmaüs Défi Présentation du métier de gardien. Dossier de presse
[PDF] Semaine Africaine des TIC (SATIC) Note conceptuelle
[PDF] FAITES AFFAIRES AVEC CONSTRUCTION DE DÉFENSE CANADA. Martine Côté, Gestionnaire régionale services des marchés
[PDF] 1 Les mesures de gestion du budget des prestations sociales et d accompagnement social :...3
[PDF] Journée d actualité. Loi de Finances 2015. 20 janvier 2015. Lille- Arras
