 Chapitre 1 : Extraction et séparation despèces chimiques I. Notion d
Chapitre 1 : Extraction et séparation despèces chimiques I. Notion d
Une substance constituée de plusieurs espèces chimiques est un mélange. Exemples : L'air est un mélange car il est contitué de plusieurs espèces chimique
 Les espèces chimiques
Les espèces chimiques
On appelle mélange une substance constituée de plusieurs espèces chimiques. Exemple : l'eau est une espèce chimique constituée de molécules identiques : la ...
 Corps pur et eau distillée
Corps pur et eau distillée
Un corps pur est une substance constituée d'atomes ou de molécules d'une même espèce.chimique. Une espèce. chimique est un ensemble d'atomes ou de molécules ou
 Chapitre 16 : Extraction identification et synthèse despèces
Chapitre 16 : Extraction identification et synthèse despèces
▫ Une substance constituée d'une seule espèce chimique est un corps pur ;. ▫ Une substance constituée de plusieurs espèces chimiques forme un mélange.
 Les espèces chimiques
Les espèces chimiques
On appelle mélange une substance constituée de plusieurs espèces chimiques. Exemple : l'eau est une espèce chimique constituée de molécules identiques : la ...
 Les minéraux et les roches pour tous
Les minéraux et les roches pour tous
Un minéral est défini par sa composition chimique. Page 26. Composition Une roche peut être constituée d'une ou de plusieurs espèces minérales. Granite ...
 Technique didentification dune espèce chimique
Technique didentification dune espèce chimique
La masse volumique est la masse d'un certain volume de matière. La masse volumique ρ d'une espèce chimique est identifiée par cette lettre de l'alphabet grec
 الكيميائية الأنواع Les espèces chimiques
الكيميائية الأنواع Les espèces chimiques
* Une substance est constituée d'une seule espèce chimique est un ................. . * Une substance constituée de plusieurs espèces chimiques est un ...
 2de_Santé_cours_3 : Caractéristiques dune espèce chimique M
2de_Santé_cours_3 : Caractéristiques dune espèce chimique M
Une substance constituée d'une seule espèce chimique est un corps ........... Une substance constituée de plusieurs espèces chimiques est un ...
 Les idées reçues : « Qui dit produit chimique… dit nocif pour la
Les idées reçues : « Qui dit produit chimique… dit nocif pour la
Un « produit chimique » correspond à un échantillon de matière constitué d'une collection macroscopique d'un nombre élevé d'une ou de plusieurs espèces
 Les mélanges
Les mélanges
Une substance constituée d'une seule espèce chimique est appelée un corps pur. Un Un mélange est une substance composée de plusieurs espèces chimiques.
 Espèces chimiques molécules et atomes
Espèces chimiques molécules et atomes
Une transformation chimique est constituée de phénomènes multiples et complexes qui peuvent le plus souvent
 Chapitre 1
Chapitre 1
Une substance constituée d'une seule espèce chimique est un corps pur. Une substance constituée de plusieurs espèces chimiques est un mélange.
 Chapitre 1 : Extraction et séparation despèces chimiques I. Notion d
Chapitre 1 : Extraction et séparation despèces chimiques I. Notion d
Comment le chimiste procède t'il pour extraire les espèces chimiques qui Une substance constituée de plusieurs espèces chimiques est un mélange.
 Constitution et transformations de la matière
Constitution et transformations de la matière
Un corps pur est une substance constituée d'une seule espèce chimique. Un mélange est une substance constituée de plusieurs espèces chimiques.
 Chapitre 16 : Extraction identification et synthèse despèces
Chapitre 16 : Extraction identification et synthèse despèces
Une substance constituée d'une seule espèce chimique est un corps pur ;. ? Une substance constituée de plusieurs espèces chimiques forme un mélange.
 Série 1
Série 1
Une substance est constituée de plusieurs espèces chimiques est un ………………………… ? Une espèce chimique fabriquée par l'homme est une espèce chimique…
 Les espèces chimiques Cours I. Comment définir le caractère
Les espèces chimiques Cours I. Comment définir le caractère
4. Qu'elle soit naturelle synthétique ou artificielle
 Les mélanges et solutions On va se limiter à lécole primaire à l
Les mélanges et solutions On va se limiter à lécole primaire à l
Un corps pur : C'est une substance constituée d'une seule espèce chimique. Lorsque l'on est en présence de plusieurs espèces chimiques qui coexistent ...
 Exercices : série 2 I Espèces chimiques - AlloSchool
Exercices : série 2 I Espèces chimiques - AlloSchool
a Une substance est constituée d'une seule espèce chimique est un Une substance constituée de plusieurs espèces chimiques est un b Une espèce chimique présente dans la nature est une espèce chimique Une espèce chimique fabriquée par l'homme est une espèce chimique c Une espèce chimique fabriquée
 Qu'est-ce qu'une espèce chimique - MAXICOURS
Qu'est-ce qu'une espèce chimique - MAXICOURS
On appelle mélange une substance constituée de plusieurs espèces chimiques Toute espèce chimique peut être représentée par une formule chimique Exemple : l’eau est une espèe himique onstituée de moléules identiques : la molé ule d’eau : H 2 O 2)- Objets et espèces chimiques
 Chapitre 1 État et évolution d’un système chimique
Chapitre 1 État et évolution d’un système chimique
chimique peut être constitué d’une seule espèce chimique (corps pur) ou de plusieurs espèces chimiques (mélange) Un état de ce système est caractérisé par la donnée de certaines grandeurs physiques pouvant être extensives ou intensives Grandeurs intensives et extensives
 Exercices : série 2 I Espèces chimiques
Exercices : série 2 I Espèces chimiques
a Une substance est constituée d’une seule espèce chimique est un Une substance constituée de plusieurs espèces chimiques est un b Une espèce chimique présente dans la nature est une espèce chimique Une espèce chimique fabriquée par l’homme est une espèce chimique c Une espèce chimique
 Searches related to une substance constituée de plusieurs espèce chimique est un PDF
Searches related to une substance constituée de plusieurs espèce chimique est un PDF
Une substance constituée d’une seule espèce chimique est un corps pur On représente le corps pur par une formule chimique Ex : le dioxygène 0 2 ; l’acide salicylique de formule C 7H6O 3 Chaque espèce chimique est caractérisée par son aspect (état physique couleur) son nom sa formule chimique et
Quels sont les différents types d’espèces chimiques ?
Une espèce chimique est naturelle lorsqu’elle est produite par la nature. Le sucre (glucose, fructose, etc.) peut être produit par les fruits, la betterave ou la canne à sucre. Le sel est une espèce chimique naturelle produite dans la mer. Le colorant rouge E124 est une espèce chimique naturelle produite par un insecte : la cochenille.
Quels sont les entités qui composent une espèce chimique moléculaire ?
Les entités qui composent une espèce chimique moléculaire sont des molécules identiques. Une molécule est un assemblage d’au moins deux atomes. Les espèces moléculaires sont électriquement neutres car les atomes qui constituent chacune des molécules le sont.
Qu'est-ce que le système physico-chimique ?
?Système physico-chimique Une espèce (ou un constituant) physico-chimique est une substance caractérisée par sa formule chimique et son état physico-chimique (solide, liquide, gaz, ou soluté). Un système physico- chimique peut être constitué d’une seule espèce chimique (corps pur) ou de plusieurs espèces chimiques (mélange).
Comment savoir si une espèce chimique a des caractéristiques physiques ?
Savoir qu’une espèce chimique possède des caractéristiques physiques. Une espèce chimique, naturelle ou synthétique, est un ensemble constitué d’un nombre très élevé d’entités identiques. Les entités peuvent être des atomes, des molécules ou des ions.
 1
1 Les mélanges et solutions
La difficulté de ce cours réside dans le vocabulaire.Le voici :
Un corps pur : C'est une substance constituée d'une seule espèce chimique.Le corps pur peut être simple (constitué d'un seul type d'atomes) Ex : He (hélium), O2
(dioxygène) ou composé (constitué d'atomes de différentes natures) Ex : H2O, CO2Lorsque l'on est en présence de plusieurs espèces chimiques qui coexistent, alors on a
affaire à un mélange (ex : de l'eau salée, l'air).1) Les mélanges homogènes
Lorsque les mélanges ne comportent qu'une seule phase (comme justement l'eau salée etl'air), alors le mélange est dit homogène. Il s'agit des mélanges où la substance ajoutée au
solvant est miscible dans le cas d'un liquide (ex : le sirop de menthe) ou soluble dans le cas d'un solide ou d'un gaz (ex : CO2 rajouté dans l'eau pour faire de l'eau gazeuse ; sel dans l'eau). Lorsque l'on disperse une quantité donnée de substance (soluté) dans l'eau (volume le plus important) (solvant), on effectue une dissolution. Il y a conservation de la masse, i.e. que : masse du mélange = masse du soluté + masse du solvantLe mélange obtenu s'appelle une solution.
La masse de substance qui peut se dissoudre dans un volume donné de solvant (la solubilité de la substance) n'est pas infinie : au-delà d'une certaine limite, la substance ne pourra plus se dissoudre. On dit alors que la solution est saturée.0Attention au vocabulaire : Le sel ne fond pas (il ne passe pas de l'état solide à l'état liquide
- cf. cours n°2) mais on dira qu'il se disperse. Les particules constituant le sel se placent en effet entre les molécules d'eau. On pourra demander aux élèves de récupérer le sel (par vaporisation de l'eau salée). 22) Les mélanges hétérogènes
Lorsque les mélanges comportent au moins deux phases (ex : huile et eau) alors le mélangeest dit hétérogène. La substance ajoutée au solvant est alors non miscible ou non soluble
(on dit insoluble). Dans le cas de l'huile et de l'eau, on peut observer des gouttelettes d'huile qui se dispersent dans l'eau. On parle alors d'émulsion. On pourra remarquer aussi que la phase contenant l'huile se " place » au-dessus de celle contenant l'eau : on dira que l'huile est moins dense que l'eau. 33) Séparer les constituants des mélanges
Ces techniques sont basées sur les changements d'état de la matière (ex : distillation,
évaporation - cf. cours n°2) ou les transformations physiques (décantation ou encore filtration). a) Comment séparer les constituants d'un mélange hétérogène ? a.1. La décantation Il est possible de pratiquer une décantation (on laisse reposer le mélange solide/liquide -une suspension) ou liquide/liquide. a.2. La filtrationIl est possible de filtrer une suspension, notamment à l'aide d'un papier filtre (on peut
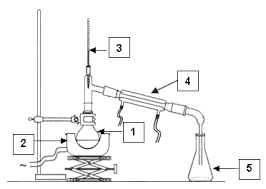
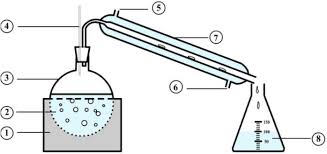
imaginer un filtre dont la trame est plus ou moins fine) un mélange hétérogène pour en séparer les constituants. Le solide est alors récupéré dans le filtre. 4 b) Comment séparer les constituants d'un mélange homogène ? b.1. La distillation Lors d'une distillation d'un mélange homogène, il y a des changements d'états successifsqui se réalisent : vaporisation (ébullition) puis liquéfaction (les vapeurs passent à l'intérieur
d'un tube réfrigéré nommé le réfrigérant). On recueille un distillat. Ceci est possible car l'un
des composés de la phase liquide a une température d'ébullition plus basse que celle de l'autre composé. b.2. L'évaporation Le solvant peut s'évaporer sous l'effet de la chaleur.On peut ici citer l'exemple des marais salants de Saint Leu. Du gros sel est récupéré après
évaporation de l'eau de mer.
Images issues des sites : je-comprends-enfin.fr ; scientic.ca ; intellego.fr ; clgjeanperrinkb.ac-creteil.fr ;
randoreunion.fr, onf.frquotesdbs_dbs28.pdfusesText_34[PDF] controle de la fecondation a la naissance
[PDF] études de physique débouchés
[PDF] que faire après une licence de physique chimie
[PDF] que faire après une licence de physique
[PDF] licence physique débouchés
[PDF] que faire apres un master de physique
[PDF] débouchés après master physique
[PDF] ingénieur physique onisep
[PDF] travailler avec un bac stl
[PDF] david olère oeuvres
[PDF] david olère mouvement artistique
[PDF] david olère portrait
[PDF] tout savoir sur le cycle menstruel de la femme
[PDF] physiologie du cycle menstruel pdf
