 Calculer une quantité de matière
Calculer une quantité de matière
M la masse molaire
 Chapitre 1 La quantité de matière la concentration molaire et le
Chapitre 1 La quantité de matière la concentration molaire et le
L'unité est toujours le gramme par mole notée g.mol–1. Ainsi
 CHIMIE I : Chimie générale
CHIMIE I : Chimie générale
n : nombre de moles ; m : masse du composé en g ;. MM : masse molaire du composé en g/mol. VI-La masse molaire atomique. C'est la masse d'une mole d'atomes .
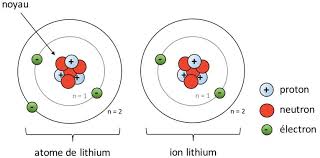 Fiche de synthèse n° 2.a Isotopes et masse molaire
Fiche de synthèse n° 2.a Isotopes et masse molaire
Elle est notée. M et s'exprime en gramme par mole (g·mol–1). Illustration de la notion de masse molaire d'un élément chimique : représente un atome de fluor. Un
 Grandeurs physiques pour caractériser un système initial
Grandeurs physiques pour caractériser un système initial
mol-1. a. Masse molaire atomique. Elle représente la masse d'une mole d'un atome. Elle correspond à la masse atomique.
 Composition initiale dun système chimique Fiche
Composition initiale dun système chimique Fiche
la masse molaire atomique du carbone est 12 g.mol−1. Elle sera notée : . Cela signifie qu'une mole de carbone ( atomes) pèse 120 g.
 Untitled
Untitled
Exercice 2 : 1 mole de CO₂ correspond à une masse molaire de : M(CO2)= M(C) Calcul du nombre de moles initial de CuO initial: la masse molaire de CuO est.
 MOLE MASSE MOLAIRE
MOLE MASSE MOLAIRE
masse molaire d'un composé (M) en additionnant les masses molaires des éléments autant de fois qu'ils apparaissent dans la formule. M H2SO4 = (2 mol H x 1 ...
 Chimie générale et organique Séries de Travaux Dirigés et Solutions
Chimie générale et organique Séries de Travaux Dirigés et Solutions
Quelle est la masse d'un atome de magnésium Mg dont la masse atomique est 24305 g/mol. Masse molaire atomique du magnésium naturel Mg (Z=12) : Soit : M = Σ ...
 Cours de Chimie générale et organique
Cours de Chimie générale et organique
MM : masse molaire du composé en g/mol. 6-La masse molaire atomique (MA) La masse d'une mole de molécules est appelée aussi masse moléculaire on la note MM.
 Chapitre 1 La quantité de matière la concentration molaire et le
Chapitre 1 La quantité de matière la concentration molaire et le
La masse molaire atomique d'un élément chimique est la masse d'une mole d'atomes de cet élément chimique. L'unité est le gramme par mole notée g.mol–1.
 Calculer une quantité de matière
Calculer une quantité de matière
M la masse molaire
 La mole Ce quil faut retenir La mole : Exercices dapplication niveau
La mole Ce quil faut retenir La mole : Exercices dapplication niveau
M : masse molaire* de l'espèce chimique contenue dans l'échantillon en g.mol-1. *Pour déterminer la masse molaire d'une espèce chimique moléculaire
 Fiche de synthèse n° 2.a Isotopes et masse molaire
Fiche de synthèse n° 2.a Isotopes et masse molaire
Elle est notée. M et s'exprime en gramme par mole (g·mol–1). Illustration de la notion de masse molaire d'un élément chimique : représente un atome de fluor. Un
 La mole comme unité de quantité de matière et les grandeurs molaires
La mole comme unité de quantité de matière et les grandeurs molaires
des javelots (élément chimique) ; masse du javelot masse des atomes du La masse molaire atomique M(X) d'unélémentX est la masse d'une mole d'atomes.
 quelques rappels sur les calculs de quantités et de concentrations
quelques rappels sur les calculs de quantités et de concentrations
concentration molaire : M. C masse molaire : MM (en g/mole) nombre de moles : n définitions masse molaire : masse d'un mole de substance ; unité : g.mole-1.
 Grandeurs physiques pour caractériser un système initial
Grandeurs physiques pour caractériser un système initial
mol-1. a. Masse molaire atomique. Elle représente la masse d'une mole d'un atome. Elle correspond à la masse atomique.
 Thème : chimie générale MOLE MASSE MOLAIRE
Thème : chimie générale MOLE MASSE MOLAIRE
MOLE MASSE MOLAIRE
 N N n =
N N n =
La masse molaire atomique est la masse d'une mole d'atomes : Son symbole est M ; elle s'exprime en grammes par mole (g.mol-1). Elle est donnée dans le tableau
 La notion de mole
La notion de mole
La notion de mole. BUT DU LABORATOIRE. Déterminer l'influence de la masse molaire par rapport au volume occupé par une mole de substance.
Page 1 sur 2
quelques rappels sur les calculs de quantités et de concentrations molaires et massiques rappels de définition : NB : symboles et abréviations utilisés dans la suite du texte (pas forcément conventionnels) quantité :Q quantité massique :
mQ quantité molaire : M
Q volume :V (unité internationale : m
3 ; autre unité conventionnelle : L) masse : volume : m (unité internationale : kg ; autre unité conventionnelle : g) concentration massique : m C concentration molaire : M C masse molaire :MM (en g/mole)
nombre de moles : n définitions masse molaire : masse d'un mole de substance ; unité : g.mole -1 (abréviations usuelles : MM, PM, FW...) concentration : c'est la quantité de soluté par volume de solvant (soluté soluté solvant CQV ou par masse de solvant ( soluté soluté solvant CQm concentration massique : concentration exprimée en masse de soluté par volume de solvant (m soluté solvant Cm V ) ou par masse de solvant ( m soluté solvant Cm m ) NB : la concentration massique est parfois exprimée en pourcentage : % de masse de soluté sur la masse de solvant. ex : solution d'albumine à 1% : d'albumine pour de solvant. concentration molaire = molarité : concentration en soluté exprimée en nombre de moles de soluté par volume de solvant (m soluté solvant Cn V ) ; Unité : mole.L -1 symbole : M concentration molale = molalité : concentration exprimée en nombre de moles de soluté par masse de solvant (m soluté solvant Cn m )unité : mole.kg -1 osmolarité : concentration en particules solubles exprimée en nombre de moles de particules par volume de solvant ( m particules solvant Cn V ) ; unité : osmole.litre -1 ; abréviation : osm.L -1 osmolalité : concentration en particules solubles exprimée en nombre de moles de particules par masse de solvant ( m particules solvant Cn m ). unité : osmole.kg -1 UFr SdV - Université Bordeaux Segalen - Etienne RouxPage 2 sur 2
quelques calculs de base1. comment convertir une quantité molaire en quantité massique ?
La quantité en massique est égale à la quantité en mole multipliée par la masse molaire.
mM QQMM2. comment convertir une quantité massique en quantité molaire ?
La quantité en molaire est égale à la quantité en mole multipliée par la masse molaire.
Mm QQMM3. comment calculer une concentration massique à partir d'une concentration
molaire ? La concentration molaire (molarité) est égale à la concentration massique multipliée par la masse molaire. mM CCMM exemple : on veut préparer une solution de NaCl à 10 mM (10 -2M) à partir de NaCl
solide. Le problème rest donc : quelle masse de NACl en solution correspond une concentration de 10 -2 M ? M C=10 -2M MM=58,44
2-110 58,44 0,5844g×L
m C4. comment calculer une concentration molaire à partir d'une concentration
massique ? La concentration massique est égale à la concentration molaire (molarité) divisée par la masse molaire. Mm CCMM exemple : on veut connaître la concentration molaire d'une solution de NaCl à 500 mg.L -1 . (5.10 -1 g.L -1 M C =5.10 -1 g.L -1MM=58,44
13-15 10 58,44 8,556 10 mol×L (M)
M C5. comment calculer un volume de dilution ?
Connaissant la masse de produit et la concentration finale voulue, on veut déterminer le volume dans lequel diluer le produit pour obtenir la concentration voulue. soluté soluté solvantCQV. D'où :
solvant soluté soluté VQC exemple 1 : on veut diluer d'albumine pour faire une solution aqueuse à 3%. On reformule le problème de la manière suivante : dans quel volume diluer d'albumine pour avoir une concentration massique de pour 10 (= 10 -1 L) d'eau ? 1g soluté Q 11 310gLsoluté C 2
130 3,310 L
solvant VIl faut diluer d'albumine dans 33 mL d'eau.
exemple 2 : on veut diluer de glucose pour faire une solution aqueuse 10 mM, sachant que la MM du glucose est de 180,16. Un calcul intermédiaire est nécessaire car la quantité de glucose est exprimée en masse et la concentration voulue en mole. Il faut donc exprimer la concentration molaire en concentration massique, (ou la quantité massique en quantité molaire). On a () ()solvant m soluté m solutéVQC. Si on convertit la concentration massique en
concentration molaire, sachant que mM CCMM , l'équation devient : solvant m MVQCMM,
soit : 21 (1 10 180,16) 0,555L
solvant Vquotesdbs_dbs47.pdfusesText_47[PDF] mole superficie epaisseur sable
[PDF] Molécule
[PDF] molécule (devoir n2 cned physique chimie)
[PDF] molecule achirale
[PDF] molécule apolaire
[PDF] molécule apolaire définition simple
[PDF] Molécule C2H7NO
[PDF] molécule chirale sans carbone asymétrique
[PDF] molécule coudée définition
[PDF] Molécule d'ADN - Rôle et structure
[PDF] Molécule d'ADN structure
[PDF] molécule d'alcool
[PDF] Molécule d'eau : distance des atomes hydrogène
[PDF] molécule d'adhérence définition
