 Étude dune réaction : titrage des ions fer II par les ions permanganate
Étude dune réaction : titrage des ions fer II par les ions permanganate
Étude d'une réaction : titrage des ions fer II par les ions permanganate. I – Généralités sur les titrages. 1) Objectif d'un titrage. Il permet à l
 Dosage du fer ferreux La manganimétrie est une technique
Dosage du fer ferreux La manganimétrie est une technique
D'autre part le potassium ( +) ion spectateur
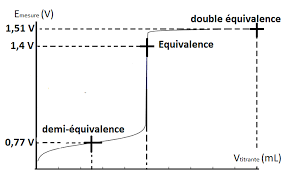 Dosage potentiométrique
Dosage potentiométrique
DOC3 : Courbe théorique du dosage des ions permanganate par les ions fer II ions ferreux Fe2+ en solution mais le sel de Mohr est moins facilement oxydé par ...
 DOSAGE DES IONS FERREUX PAR DES IONS PERMANGANATE
DOSAGE DES IONS FERREUX PAR DES IONS PERMANGANATE
Produit phytosanitaire utilisé contre la chlorose sous forme de poudre à base d'élément fer (ce solide est en cristal ionique contenant l'ion fer II).
 TP- Dosage des ions Fer II dans un produit anti- mousse
TP- Dosage des ions Fer II dans un produit anti- mousse
Alors que l'on ajoute de la solution aqueuse de permanganate de potassium de couleur violette dans le tube la le mélange reste incolore. Q2-2 : Une réaction
 Teneur en fer dun produit sanitaire. La teneur en fer dun produit
Teneur en fer dun produit sanitaire. La teneur en fer dun produit
ions permanganate réagissent en solution aqueuse avec les ions ... solution de permanganate de potassium pour réaliser le titrage des ions ferreux contenus dans ...
 Untitled
Untitled
dosage Fer(II) /. Ce(IV)) car les espèces Fe3+ et Fe2+ sont présentes en ... tion ferreuse à la solution de permanganate. La formation d'ion manganeux en mi ...
 Détermination dune quantité de matière Fiche
Détermination dune quantité de matière Fiche
Quelle est l'évolution du système lors d'un dosage par titrage colorimétrique ? Les ions permanganate sont en excès et les ions fer (II) sont le réactif ...
 Étude dune réaction : titrage des ions fer II par les ions permanganate
Étude dune réaction : titrage des ions fer II par les ions permanganate
Étude d'une réaction : titrage des ions fer II par les ions permanganate. I – Généralités sur les titrages. 1) Objectif d'un titrage.
 TP 13 DOSAGE des IONS FER (II) contenus dans le SEL de MOHR
TP 13 DOSAGE des IONS FER (II) contenus dans le SEL de MOHR
une solution aqueuse de concentration connue en ion fer (II) dosage des ions. 2+. (aq). Fe de S1 par une solution acidifiée de permanganate de potassium.
 Compte rendu du TP de chimie n°9 Les dosages rédox
Compte rendu du TP de chimie n°9 Les dosages rédox
II) Dosages des ions Fe2+ réagir avec un oxydant tel l'ion permanganate MnO4 ... d'hydroxyde de fer (II) en présence d'ions fer (II) Fe2+. (aq) selon.
 TP- Dosage des ions Fer (II) dans un produit anti-mousse
TP- Dosage des ions Fer (II) dans un produit anti-mousse
PROBLÉMATIQUE : Déterminer la concentration molaire en ion fer(II) de la solution la réaction entre les ions fer (II) Fe2+ et les ions permanganate.
 Teneur en fer dun produit sanitaire. La teneur en fer dun produit
Teneur en fer dun produit sanitaire. La teneur en fer dun produit
Pour réaliser le titrage des ions ferreux Fe2+
 Titrage des ions fer II
Titrage des ions fer II
En déduire l'équation chimique de la réaction de titrage. Q3. À l'équivalence quelle relation existe-t-il entre la quantité de matière d'ions permanganate
 TP- Dosage des ions Fer II dans un produit anti- mousse
TP- Dosage des ions Fer II dans un produit anti- mousse
Q2-2 : Une réaction chimique a-t-elle eu lieu ? Si oui quel réactif pouvez-vous déjà identifier ? L'expérience 2 prouve que les ions permanganate
 TP8 - Dosage colorimétrique dions fer II en solution
TP8 - Dosage colorimétrique dions fer II en solution
Déterminer la quantité de matière puis la concentration en ions fer II d'une solution de sel de Mohr en dosant ces ions par une solution de permanganate
 TP n°12 : LA CHLOROSE DES VEGETAUX
TP n°12 : LA CHLOROSE DES VEGETAUX
(aq) + MnO4. -. (aq)) de couleur violette. Lors du dosage les ions permanganate MnO4. - réagissent avec les ions Fer (II) Fe2+
 Les dosages doxydoréduction
Les dosages doxydoréduction
Les dosages d'oxydoréduction appelés également dosages rédox
1STL-SPCL Thème Chimie et développement durable ² Analyses physico-chimiques
(Catherine BOUTON et Gérald FAYOLLE, lycée Paul Langevin de Beauvais)TP- Dosage des ions Fer (II) dans un produit
anti-mousse Capacités théoriques et expérimentales abordées : - 7HVPV G·LGHQPLILŃMPLRQ GHV LRQV. - GpILQLU O·pTXLYMOHQŃH ORUV G·XQ GRVMJHB - Déterminer les concentrations des espèces présentes dans le milieu réactionnel au cours du dosage. - GpPHUPLQHU OM YMOHXU GH OM ŃRQŃHQPUMPLRQ G·XQH VROXPLRQ inconnue. - (VPLPHU OM YMOHXU GX YROXPH j O·pTXLYMOHQŃHB - Réaliser un dosage par changement de couleur. - Repérer une équivalence. M. Martin constate que la pelouse dans son jardin est envahie par une quantité importante dePRXVVHB HO GpŃLGH G·arroser la pelouse MYHŃ XQH VROXPLRQ G·MQPL-mousse de gazon. Il retrouve dans sa
remise un bidon avec étiquette sur laquelle est inscrite " Sulfate de fer » mais il a un doute sur le
contenu : V·MJLP-il G·XQH solution anti-chlorose (solution très concentrée en ion fer (II) utilisée pour
soigner les carences en fer des végétaux) ou G·XQH solution anti-mousse (moins concentrée en ions fer
(II)) ? PROBLÉMATIQUE : Déterminer la concentration molaire en ion fer(II) de la solution retrouvée et en déduire si M. Martin peut en faire un usage pour éliminer la mousse de sa pelouse. Document 3 : Test G·LGHQPLILŃMPLRQ GHV LRQV (rappels)Ion à tester FRXOHXU GH O·LRQ HQ
solutionRéactif Résultat positif
Fer (III) (Fe3+) Rouille Ion hydroxyde (HO-) Précipité rouille Fer (II) (Fe2+) Vert très pâle Ion hydroxyde (HO-) Précipité vertPermanganate (MnO4-) Violette - -
Manganèse (Mn2+) Incolore Ion hydroxyde (HO-) Précipité blanc qui brunit Sulfate (SO42-) Incolore Ion baryum (Ba2+) Précipité blanc Argent (Ag+) Incolore Ion chlorure (Cl-) Précipité blanc qui noircit à la lumièreDocument 1 : Produit anti-mousse
Le sulfate de fer II est employé pour éliminer la mousse qui envahit les gazons, empêchant ainsi le gazon de pousser. Pour ne pas faire trop de dégât cette solution doit avoir une concentration en ion fer (II), CFe2+ inférieure à 50 g.L-1.Document 2 : Formulaires
(rappels) n = C x V m = n x MCm = C x M
Avec n en mole
m en gC en mol.L-1
Cm en g.L-1
M en g.mol-1
I- Etude qualitative
Cette SMUPLH SHUPHP G·étudier la réaction entre les ions fer (II) Fe2+ et les ions permanganate
MnO4-. Cette réaction servira ensuite de réaction support au dosage.Expérience n°1 :
- Dans un tube à essais verser quelques millilitres de la solution aqueuse de sulfate de fer (II) - $ÓRXPHU TXHOTXHV JRXPPHV G·XQH VROXPLRQ aqueuse G·O\GUR[\GH GH VRGLXP - Noter vos observations et compléter le document réponseExpérience n°2 :
- Dans un tube à essais verser quelques millilitres de la solution aqueuse de sulfate de fer (II)- Ajouter quelques gouttes à O·MLGH G·XQH OLTXLSLSHPPH XQH VROXPLRQ aqueuse de permanganate de
potassium - Noter vos observations et compléter le document réponseExpérience n°3 :
3MUPMJHU OM VROXPLRQ RNPHQXH j OM ILQ GH O·H[SpULHQŃH 2 GMQV GHX[ PXNHV à essais.
- GMQV OH SUHPLHU PXNH YHUVHU TXHOTXHV JRXPPHV G·XQH VROXPLRQ G·O\GUR[\GH GH VRGLXPB - Observer et compléter le document réponse - Dans le second tube, continuer à ajouter de la solution de permanganate de potassium. - Noter vos observations et compléter le document réponseII- Etude quantitative
Document 4 : Principe du dosage par titrage
IRUV G·XQ GRVMJH RQ YHXP GpPHUPLQHU OM ŃRQŃHQPUMPLRQ molaire G·XQH HVSqŃH chimique dans une
solution donnée : ici la concentration molaire en ion Fer (II), notée CFe2+, de la solution retrouvée par
M. Martin.
Pour cela on fait réagir un volume connu de la solution de concentration inconnue avec unesolution titrante de concentration connue. On détermine le volume exact de solution titrante
QpŃHVVMLUH SRXU TXH O·HVSèce titrée présente dans le prélèvement ait totalement réagi.
Les ions Fer (II) Fe2+de la solution retrouvée réagissent avec les ions permanganate MnO4- de la solution titrante VHORQ O·pTXMPLRQ :5 Fe2+(aq) + MnO4- (aq) + 8 H+(aq) AE 5 Fe3+(aq) + Mn2+(aq) + 4 H2O(l)
2Q MSSHOOH pTXLYMOHQŃH O·LQVPMQP où les réactifs titrés (Fe2+) et titrant (MnO4-) ont été versés
GMQV OHV SURSRUPLRQV VP±ŃOLRPpPULTXHV Ń·HVP-à-GLUH VHORQ OHV SURSRUPLRQV LQGLTXpHV GMQV O·pTXMPLRQ GH
réaction du dosage.CHOM VLJQLILH TX·j O·pTXLYMOHQŃH RQ M O·pJMOLPp VXLYMQPH HQPUH OHV TXMQPLPpV GH PMPLqUH GHV
réactifs (mole) :1- Manipulation
Légender le schéma sur le compte-rendu
0HPPUH HQ ±XYUH OHV pPMSHV VXLYMQPHV :
Dosage rapide
Remplir la burette graduée avec la solution de permanganate de potassium de concentrationCMnO4- = 1,00.10-2 mol.L-1
À O·MLGH G·XQH SLSHPPH ÓMXJpH, prélever VE = 10,0 mL de solution retrouvée par M. Martin.
Les verser dans un erlenmeyer de 250 mL.
$ÓRXPHU 10 PI G·MŃLGH VXOIXULTXH j 10 % (mettre vos gants et lunettes de protection). Introduire un barreau aimanté GMQV O·HUOHQPH\HU.HQVPMOOHU O·MJLPMPHXU PMJQpPLTXH VRXV OM NXUHPPH graduée et placer O·HUOHQPH\HU VXU O·MJLPMPHXU
magnétique.0HPPUH HQ URXPH O·MJLPMPLRQ magnétique (agitation modérée).
Introduire progressivement la solution titrante mL par mL. Dès que la coloration rose de la solution dans le bécher persiste MUUrPHU O·MÓRXP GH VROXPLRQ PLPUMQPHB1RPHU OH YROXPH 9· LQGLTXp sur la burette graduée.
Dosages précis
Réïtérer les mêmes étapes, mais ajouter au préalable de la solution PLPUMQPH ÓXVTX·MX YROXPH
V·-2 mL.
Introduire ensuite la solution titrante goutte-à-goutte et arrêter les ajouts dès que la solution
GMQV O·HUOHQmeyer se colore en rose (dosage à la goutte près). Noter le volume V1 indiqué sur la burette graduée. Recommencer ce dosage deux fois supplémentaires et noter les volumes V2 et V3 obtenus.2- Interprétation
Compléter le compte-rendu de façon à interpréter les résultats du dosage et répondre à la
problématique du TP. TP- Dosage des ions Fer (II) dans un produit anti- mousseCompte rendu
I- Etude qualitative
Voir les photographies des expériences en annexe Q1 IRUV GH O·H[SpULHQŃH 1 TX·RNVHUYH]-vous ? Q2-1 : Lors GH O·H[SpULHQŃH 2 TX·RNVHUYH]-vous ?Q2-2 : Une réaction chimique a-t-elle eu lieu ? Si oui, quel réactif pouvez-vous déjà identifier ?
Q3 IRUV GH O·H[SpULHQŃH 3 TX·RNVHUYH]-vous ?Q4 : $ O·MLGH GX GRŃXPHQP 3 LGHQPLILHU OHV LRQV SUpVHQPV GMQV OHV PXNH 1 HP 2 GH O·H[SpULHQŃH 3B
Q5 : Interpréter OH UpVXOPMP GH O·H[SpULHQŃH 3.II- Etude quantitative
Q6 : Légender le montage ci-contre.
Q7 : On reporte les volumes équivalents trouvés :9· 12 mL (rapide)
V1 = 11,7 mL
V2 = 11,75 mL
V3 = 11,7 mL
Calculer le volume équivalent moyen VMQV PHQLU ŃRPSPH GH 9· Veq = Q8-1 GRQQHU O·H[SUHVVLRQ OLPPpUMOH GH OM TXMQPLPp GH PMPLqUH nFe2+ Q8-2 GRQQHU O·H[SUHVVLRQ OLPPpUMOH GH OM TXMQPLPp GH PMPLqUH QMnO4-Q9 : Déduire de O·pJMOLPp j O·pTXLYMOHQŃH GRQQpH GMQV OH GRŃXPHQP 4 HP GHV TXHVPLRQV 48 XQH UHOMPLRQ
entre les concentrations des espèces titrée CFe2+ et titrante CMnO4-. Q10 : GRQQHU MORUV O·H[SUHVVLRQ GH OM ŃRQŃHQPUMPLRQ HQ LRQ )H2+ en fonction de ܥVE et du volume équivalent, noté Veq.
Q11 : Calculer alors la concentration molaire en ion Fe2+ de la solution retrouvée par M. Martin.Q12 : En déduire la concentration massique en ion Fe2+ de la solution retrouvée par M. Martin. On donne
M(Fe) = 55,8 g.mol-1
Q13 : Conclure sur la problématique.
TP- Dosage des ions Fer (II) dans un produit anti- mousseAnnexes
Photographie expérience 1
Photographie expérience 2
IH PXNH j JMXŃOH UHSUpVHQPH OH UpVXOPMP GH O·H[SpULHQŃH 2 OH PXNH GH droite donne la couleur initiale de
la solution de permanganate de potassium)Photographie expérience 3
Précipité vert
Précipité orange
orangeorangequotesdbs_dbs50.pdfusesText_50[PDF] dosage des salicylés dans le sang
[PDF] dosage des triglycérides sériques par méthode enzymatique
[PDF] dosage du cholestérol total
[PDF] dosage du mélange naoh et na2co3
[PDF] dosage du mélange naoh na2co3 par hcl
[PDF] dosage dureté de l'eau
[PDF] dosage en point final définition
[PDF] dosage enzymatique de substrat en point final
[PDF] dosage ethanol dans le vin
[PDF] dosage ethanol dichromate
[PDF] dosage fe2+ par cr2o72-
[PDF] dosage fuel fit
[PDF] dosage indirect
[PDF] dosage ion fer ii par permanganate

