 MESURE DE LA PRESSION ATMOSPHÉRIQUE: LE BAROMÈTRE
MESURE DE LA PRESSION ATMOSPHÉRIQUE: LE BAROMÈTRE
On prend une bassine et on la remplit de mercure. On remplit ensuite le tube de Torricelli en utilisant un entonnoir adapté jusqu'à ce que le ménisque du
 Baromètre de Torricelli sans mercure
Baromètre de Torricelli sans mercure
When air pressure fluctuations occur the red fluid level will differ from the last position of your pointer. The difference is the indication of the coming
 Le baromètre
Le baromètre
De Galilée à Blaise Pascal en passant par René Descartes et surtout Torricelli le baromètre est une invention Torricelli constata aussi que la hauteur du ...
 Untitled
Untitled
C'est bien la preuve que l'instrument devait servir à la prévision du temps. Ainsi 22 ans avant Torricelli
 LA MESURE DE LA PRESSION Historique du baromètre
LA MESURE DE LA PRESSION Historique du baromètre
Le premier baromètre a été inventé par Torricelli en 1644. Voulant mesurer les variations du poids de l'air Torricelli remplit de mercure un tube de verre
 Une brève histoire du baromètre
Une brève histoire du baromètre
17 nov. 2021 pour améliorer la précision du tube de Torricelli et les usages qui sont faits du baromètre. Nous en venons ensuite aux enjeux de la ...
 Themodynamique Activités du chapitre 5 TSI 2 la masse volumique
Themodynamique Activités du chapitre 5 TSI 2 la masse volumique
Activité 1 : Baromètre de Torricelli. On réalise un baromètre en remplissant un tube de 1 mètre de long avec du mercure (on note la masse volumique du
 LA MESURE DE LA PRESSION
LA MESURE DE LA PRESSION
Le premier baromètre a été inventé par Torricelli en 1644. Voulant mesurer les variations du poids de l'air Torricelli remplit de mercure un tube de verre
 Borne n° 9 : Le baromètre Qui a inventé le baromètre et lors de quel
Borne n° 9 : Le baromètre Qui a inventé le baromètre et lors de quel
Un peu d'histoire : Le baromètre a été inventé en 1643 par Evangelista. Torricelli (1608-‐1647) un physicien et mathématicien italien. Limitez votre
 Baromètre et pression atmosphérique
Baromètre et pression atmosphérique
7 juin 2022 René Descartes5 améliore le système de Torricelli en ajoutant une graduation en papier il est le premier à formuler l'hypothèse que la pression ...
 LE BAROMÈTRE
LE BAROMÈTRE
L'histoire met en scène Galilée Torricelli et Pascal. Ils cherchent à expliquer pourquoi il est impossible d'élever l'eau
 MESURE DE LA PRESSION ATMOSPHÉRIQUE: LE BAROMÈTRE
MESURE DE LA PRESSION ATMOSPHÉRIQUE: LE BAROMÈTRE
À travers cette expérience on peut mesurer la pression atmosphérique avec le baromètre de Torricelli. On prend une bassine et on la remplit de mercure.
 Untitled
Untitled
Ce baromètre sensible indéréglable est fragile à transporter. Nous employons un système breveté bloquant la colonne de mercure mais permettant d'en
 LA MESURE DE LA PRESSION
LA MESURE DE LA PRESSION
Le premier baromètre a été inventé par Torricelli en 1644. Voulant mesurer les variations du poids de l'air Torricelli remplit de mercure un tube de verre
 Leçon 13 La mesure de la pression atmosphérique Baromètre
Leçon 13 La mesure de la pression atmosphérique Baromètre
Le baromètre à mercure dérive du tube de. Torricelli ; il est fidèle faisant toujours correspondre la même dénivellation H à la même valeur de la pression.
 Une brève histoire du baromètre
Une brève histoire du baromètre
pour améliorer la précision du tube de Torricelli et les usages qui sont faits du baromètre. Nous en venons ensuite aux enjeux de la prédiction du temps et
 Baromètre de Torricelli sans mercure
Baromètre de Torricelli sans mercure
Le baromètre Eco-celli® est un instrument dont la précision peut être comparée avec un baromètre à mercure. Torricelli-barometer.
 Le baromètre
Le baromètre
Le baromètre à mercure : la pression atmosphérique est équilibrée par une colonne de mercure Il a été inventé par Evangelista Torricelli en 1643 ;.
 Cours 2 : La pression et le vide. Variables thermodynamiques
Cours 2 : La pression et le vide. Variables thermodynamiques
Baromètre de Torricelli par Gasparo Berti à Rome mais... avec de l 'eau ! Evangelista Torricelli. 1608-1647. Evangelista Torricelli ou Gasparo Berti ?
 LA MESURE DE LA PRESSION Historique du baromètre
LA MESURE DE LA PRESSION Historique du baromètre
Le premier baromètre a été inventé par Torricelli en 1644. Voulant mesurer les variations du poids de l'air Torricelli remplit de mercure un tube de verre
 [PDF] mesure de la pression atmosphérique: le baromètre de torricelli
[PDF] mesure de la pression atmosphérique: le baromètre de torricelli
À travers cette expérience on peut mesurer la pression atmosphérique avec le baromètre de Torricelli On prend une bassine et on la remplit de mercure
 [PDF] barometre a mercure
[PDF] barometre a mercure
BAROMETRE A MERCURE Modèle breveté SGDG Ref: 251 001 Ce baromètre sensible indéréglable est fragile à transporter Nous employons un système
 [PDF] LE BAROMÈTRE - AC Nancy Metz
[PDF] LE BAROMÈTRE - AC Nancy Metz
L'appareil de Torricelli permet de mesurer la valeur de cette pression: il est baptisé « baromètre » Page 2 DISCIPLINES CLASSES ET PROGRAMMES – Physique-
 [PDF] Le baromètre de Torricelli
[PDF] Le baromètre de Torricelli
Il sert comme tout baromètre à mesurer la c'est-à-dire la Il est constitué d'un tube de verre
 [PDF] LA MESURE DE LA PRESSION Historique du baromètre - Awekas
[PDF] LA MESURE DE LA PRESSION Historique du baromètre - Awekas
Le premier baromètre a été inventé par Torricelli en 1644 Voulant mesurer les variations du poids de l'air Torricelli remplit de mercure un tube de verre
 [PDF] Baromètre et pression atmosphérique - Eduscol
[PDF] Baromètre et pression atmosphérique - Eduscol
7 jui 2022 · Descendant du tube de Torricelli (figure 1) le baromètre à mercure est un tube en U fermé à une extrémité Rempli de mercure il est renversé
 B AROMÈTRES Torricelli - PDF Téléchargement Gratuit - DocPlayerfr
B AROMÈTRES Torricelli - PDF Téléchargement Gratuit - DocPlayerfr
Les baromètres à mercure appareils de précision mesurent la pression atmosphérique Leur sensibilité n est égalée par aucun autre instrument courant
 [PDF] Le baromètre - PATRIMOINE de Cognac la Forêt
[PDF] Le baromètre - PATRIMOINE de Cognac la Forêt
Le baromètre est un instrument de mesure utilisé en physique et en météorologie Il a été inventé par Evangelista Torricelli en 1643 ;
 [PDF] Baromètre à mercure - Ecole Numériquetn
[PDF] Baromètre à mercure - Ecole Numériquetn
L'expérience de Torricelli (1643) a fourni le principe de la mesure de la pression atmosphérique en la ramenant à une mesure de la hauteur H d'une colonne de
 [PDF] Capteur de pression et baromètre de précision
[PDF] Capteur de pression et baromètre de précision
Capteur de pression et baromètre de précision 1ère Année 2007 - 2008 5 II Historique de la pression Torricelli était un physicien et mathématicien
Comment fonctionne le baromètre de Torricelli ?
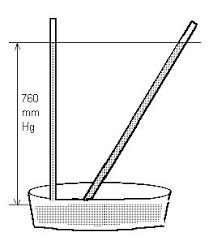
Il est composé d'un long tube en verre, rempli de mercure, et recourbé sur sa partie basse, qui se termine par un réservoir rempli en partie de mercure. La pression atmosphérique 'retient' le mercure, qui se stabilise à pression normale (1013 mbar) à 76 cm de hauteur de mercure dans le tube gradué.Comment régler un baromètre de Torricelli ?
Sur un baromètre de Toricelli, le réglage se fait plus facilement: il suffit de déplacer la petite plaquette amovible (souvent les altitudes sont indiquées pour faciliter le réglage). Toutefois, ne vous inquiétez pas trop si votre baromètre est mal réglé, car même ainsi, il continuera à vous donner la même tendance.Quel est le principe du baromètre à mercure ?
Les baromètres mesurent la pression atmosphérique. Dans le cas du baromètre à mercure, la pression s'exerce sur la surface libre de la cuve à mercure. Une variation de la pression se traduit par une variation de la force exercée sur le mercure de la cuve, et donc par une variation du niveau du liquide dans le tube.- Le principe physique du fonctionnement du baromètre est l'équilibre des forces. La colonne de mercure contenue dans le tube cherche à descendre sous l'effet de son poids. Cependant, l'air environnant pousse sur le mercure dans le bassin.
Thermodynamique Plan du cours 2. Pression d'un fluide à l'équilibre : exemples Le vide et ses conséquences Types de variables thermodynamiques Retour sur le gaz parfait Le gaz réel
- Les TPs démarrent la semaine du 2 octobre- A partir du lundi 25/09 :- Consulter le tableau d'affichage au 1er étage du bat. Oméga pour connaître les jours de passage - Chercher les polycopiés auprès de Mme Defour (porte 125, 1er étage du bat. Oméga) - Il y a 3 TPs : TP1 et TP2 dans la salle 106 et TP3 dans la salle 123, 1er étage du bât Oméga- Pas de report de notes entre l'an passé et cette année- Contrôle stricte de l'assiduité- Voir avec Mme Defour pour les changements de groupe ...INFORMATIONS TPsTransparents du permier Cours : http://lpmcn.univ-lyon1.fr/~sanmigue/puis cliquer " Cours en ligne » (en bas à gauche) puis " Thermodynamique... »
Pression dans un fluide à l'équilibredp=-zgzdzExpresion générale :Qu'on écrit souvent :
dp dz=-zgzExemple : pression au fond des océans H2O=1 gcm-3=103 Kgm-3 g≈10 ms-2z z=0H2Oz=h pp0 ∫P P0 dp=-g∫0 h dzp0 -p=-gh p=p0 gh p=105 10310 10 =2 105 PaPour une profondeur de 10 m : p0 =105 PaBaromètre de TorricellipA=pA'=patm
dp=-gdz∫Pz=0 Pz=h dp=-∫z=0 z=h gdz ∫Patm 0 dp=-∫z=0 z=h gdzz z=0A A'h Hg phph=0.00185torr≈0 pression de vapeur du mercure [P]Patm 0 =-g[z]0 h0 -patm=-ghpatm=gh
Hg=13,59951 gcm-3=13595,1 Kgm-3 g=9,80665 ms-2h=0,760 mpatm=101325 PaL 'expérience deTorricelli (1644) avait déjà étéréalisée par Gasparo Berti à Rome, mais... avec de l 'eau !
Evangelista Torricelli1608-1647Evangelista Torricelli ou Gasparo Berti ?Aristote :" Le espace viden'est qu'une contradictionde termes »Ou l'arrivée du videEt le vide nous entoure !!Auvergne, le baromètre de Torricellisur le haut du puy de DômeMais le vide est bien la ... !
La maîtrise du vide: expérience des " hémisphères de Magdeburg » d 'Otto von Guericke (1657) qui inventá la pompe à vide.Faire le vide ou la naissance de la révolution industrielle
Le vide quantique : la revanche d'AristoteL'Univers ne serait qu'une "écume de vide" :une fluctuation quantique du videLe vide est empli d'énergie
Que peut-on encore faire avec du mercure ?
Une fontaine de Mercure : pourquoi pas?Et nager dans du mercure?Types de variables thermodynamiquesdécrit avec un ensemble de variables.Exemple : n, V, T, p Coupons ce système S en 2 parties S1 et S2 qui restent en équilibreS1S2 Soit un système S homogène et en équilibre thermodynamiqueS
On peut mesurer : n1, V1, T1, p1
n2, V2, T2, p2 Si X est l'une de variables : X est extensive si X = X1 + X2 X est intensive si X = X1 = X2Exemples ?V, n, S(entropie)Exemples ?p, T, η (potentiel chimique)Relation entre variables thermodynamiques Les variables thermodynamiques peuvent être associés par couples(Intensive, Extensive) Le produit de ces couples est une énergie Exemples : p, V : énergie mécanique (travail) T, S : énergie thermique (chaleur) h ,n : énergie chimique
Relation entre variables thermodynamiques On peut décomposer le milieu exterieur au système en un ensemble de " résevoirs ».
Un réservoir est caractérisé par : Une grandeur intensive (" la reserve »... infinie) Une grandeur extensive qui peut-être échangée avec le système si ses parois le permettent. Le produit des 2 grandeurs constitue l'énergie échangée entre le système et le milieu exterieur.
Echanges Système-RéservoirsParticules h
MécaniquepThermiqueT
SystèmenEchimique
SChaleur
VTravail
Principe zéro de la thermodynamiqueT1T3
T3T2T1T2=
ÞSi 2 systèmes sont en équilibre thermique avec un troisièmesystème, ils sont aussi en équilibre entre eux.
Le gaz parfaitSi n=cteSi T= cte Þ pV=cteLoi de Boyle - MariotteSi p= cte Þ VT=cteLoi de Gay-LussacSi V= cte Þ
pT=cteLoi de Charles
V n=ctep=cteT=cteSiÞLoi d'AvogadroDans des conditions normalesp=101325 PaT=273,15 K et pour n=1
V=nRT p=1 ×8,314 ×273,15101325=0,0224 m3 =22,4 l
pV=nRT Pressions partiellesMélange de 2 gaz parfaitsn1n2P,V,TLa pression partielle, pi , du gaz i est
définie par :piV=niRTC'est la pression du gaz i s'il occupait seul le volume total V à temperature T.
p1 V=n1RTOn a donc : p2 V=n2RT p1 p2V=n1n2RT+Et pour le volume total pV=nRT
maisn=n1 n2p1p2V=nRTp=p1 p2Généralisation à un mélange de m gaz parfaits
p=∑i=0 i=m piLoi de DaltonLe gaz réelEquation d'état de van der Waals (prix Nobel 1910)Deux hypothèses supplementaires : H1 : Seul le volume librement accessible est considéré. Le volume des particules est soustrait du volume total :Vréel=Vconteneur-Nb'
Vréel=Vconteneur-nbb: constante de covolumeNb' ou nb: volume incompresssible de N particules.Nb = S
Le gaz réel : équation de van der Waals H2 L'intéraction attractive prédominante entre les particules assure la cohésion du gaz. La pression d'un gaz réel est donc inférieure à celle du gaz parfait.L'intéraction entre particules est par paires. Dans un gaz de N particules :Pour 1 particule : N-1 pairesPour N particules : N(N-1)/2 pairesSi N est très grand : µ N2
On préfére parler de concentration de particules N/V ou encore mieux n/VDonc, l'intéraction entre particules donne lieu à une " pression de cohésion »proportionnelle à n2/V2pvdW=pparfait-an2
V2pparfait=pvdWan2
V2Le gaz réel : équation de van der WaalsL'équation d'état du gaz idéal : pparfaitV=nRTIdée de van der Waals :
Vréel=V-nb'a ) Remplacer V (conteneur) par le volume réel : du gaz pparfait=pvdWan2V2 =pan2
V2b) Remplacer pparfait :
pan2V2V-nb=nRTÉquation d'état de van der Waalsa : constante de pression interneb : constante de covolumeNe dependent que de la nature du gaz
quotesdbs_dbs15.pdfusesText_21[PDF] experience de torricelli pdf
[PDF] torricelli juve
[PDF] blaise pascal pesanteur
[PDF] blâme définition littéraire
[PDF] tsutomu nihei
[PDF] le blâme en littérature
[PDF] chanson de roland texte et traduction
[PDF] la chanson de roland paroles
[PDF] la chanson de roland résumé pdf
[PDF] blancanieves pablo berger analyse
[PDF] blanche neige
[PDF] blanca nieves
[PDF] bled pdf gratuit
[PDF] bled tout en un pdf
