 T.P. n° 1.
T.P. n° 1.
T.P. n° 2. DOSAGE DE DOSAGE DE LA CHLOROPHYLLE a (comparaison des résultats ... fluorimétrie et la spectrophotométrie après extraction des pigments.
 TP No 03. Extraction et dosage des différents pigments
TP No 03. Extraction et dosage des différents pigments
photosynthétiques : Chlorophylle a et b ainsi que les caroténoïdes. but de cette expérience est de quantifier par une méthode spectrophotométrique les.
 TP PV pigments_2009.rtf
TP PV pigments_2009.rtf
Les chlorophylles sont les pigments majeurs impliqués dans la capture des photons. La chlorophylle est synthétisée et dégradée dans l'enveloppe du chloroplaste
 TP N°1 : SPECTROPHOTOMETRIE : DOSAGE PAR ETALONNAGE
TP N°1 : SPECTROPHOTOMETRIE : DOSAGE PAR ETALONNAGE
TP N°1. Chimie. Prof. 1. TP N°1 : SPECTROPHOTOMETRIE : DOSAGE PAR ETALONNAGE. Introduction : 1) Pourquoi une solution est-elle colorée ?
 Mesure de quelques paramètres environnementaux du lagon de
Mesure de quelques paramètres environnementaux du lagon de
Tableau 1 : Comparaison des méthodes spectrophotométrique etfluorimétrique pour le dosage de la chlorophylle dans l'eau lagonaire extraction au méthanol
 Travaux pratiques de physiologie végétale
Travaux pratiques de physiologie végétale
TP ? 04.Extraction et dosage des différents pigments photosynthétiques est de doser par spectrophotomètre d'absorption les chlorophylles a et b.
 TP n°6 Dosage spectrophotométrique des colorants dun sirop de
TP n°6 Dosage spectrophotométrique des colorants dun sirop de
Dosage spectrophotométrique des colorants d'un sirop de menthe. Correction. On souhaite dans ce TP déterminer la concentration des colorants présents dans
 TP SPECTRE DABSORPTION
TP SPECTRE DABSORPTION
5- Tracer le graphe illustrant l'absorbance d'une solution de chlorophylle brute d'épinards en fonction des longueurs d'onde du spectre de la lumière blanche
 Le Soleil notre source dénergie TP4 – Études des pigments
Le Soleil notre source dénergie TP4 – Études des pigments
Ceux que l'on appelle couramment chlorophylle est un mélange de plusieurs pigments On cherche à déterminer par spectrophotométrie
 Méthode danalyse Détermination de la chlorophylle a : méthode par
Méthode danalyse Détermination de la chlorophylle a : méthode par
21 févr. 2003 coup de doser la phéophytine a. La calibration du fluorimètre est préalablement effectuée à l'aide d'un spectrophotomètre et des.
 Extraction et séparation de la chlorophylle - sitesensfeafr
Extraction et séparation de la chlorophylle - sitesensfeafr
Plusieurs gouttes de solution de chlorophylle sont déposées sur la phase fixe à l’aide d’un capillaire pour former une tâche La plaque de silice est mise en contact avec la phase liquide qui va migrer et entrainer les pigments de la chlorophylle par capillarité
 TP BAC : TP : Extraction de la chlorophylle + spectroscope
TP BAC : TP : Extraction de la chlorophylle + spectroscope
TP BAC : TP : Extraction de la chlorophylle + spectroscope Hyp : la chlorophylle absorbe les photons de la lumière et convertit l’énergie lumineuse pour permettre la photolyse de l’eau et les oxydoréductions mises en évidence précédemment 2 La lumière source d’énergie de la photosynthèse est captée par la chlorophylle
 TP CHIMIE N°03 : SPECTROPHOTOMÉTRIE - legtuxorg
TP CHIMIE N°03 : SPECTROPHOTOMÉTRIE - legtuxorg
TP de chimie n°3 SPECTROPHOTOMETRIE dosage par étalonnage et suivi cinétique d’une réaction chimique Terminale MATERIEL AU BUREAU: • Spectrophotomètre + cuves (salle 304) • Grands tubes à essais • 1 pipette graduée de 10 mL + pipeteur • 1 pipette graduée de 2 mL • 3 béchers de 50 mL • 3 bécher de 100 mL • 1 agitateur
 Méthode d’analyse - Détermination de la chlorophylle a
Méthode d’analyse - Détermination de la chlorophylle a
6 4 Solution mère maison de chlorophylle a Préparer une solution mère maison à 2 mg/l dans l’acétone à 90 à partir de chlorophylle a sous forme solide (CAS n° 479-61-8) La concentration de cette solution doit être déterminée précisément par spectrophotométrie (cf 7 1 1)
 Utilisation des spectrophotomètres : Application au dosage du
Utilisation des spectrophotomètres : Application au dosage du
Application au dosage du chlore libre Les spectrophotomètres sont utilisés pour mesurer rapidement et avec une bonne précision différents paramètres de suivi de qualité du traitement des eaux On parle aussi de « micro-méthodes » par opposition aux méthodes de dosages des laboratoires spécialisés 1 Principe de fonctionnement
Comment fonctionne la photosynthèse de la chlorophylle ?
TP BAC : TP : Extraction de la chlorophylle + spectroscope Hyp : la chlorophylle absorbe les photons de la lumière et convertit l’énergie lumineuse pour permettre la photolyse de l’eau et les oxydoréductions mises en évidence précédemment. 2. La lumière, source d’énergie de la photosynthèse est captée par la chlorophylle.
Comment faire l'extraction de la chlorophylle ?
?TP BAC : TP : Extraction de la chlorophylle + spectroscope a) Extraction de la chlorophylle brute. L’extraction des pigments peut se réaliser sur différents types de feuilles de plantes supérieures et aussi sur des thalles d'algues, quelle que soit leur couleur apparente due à des pigments supplémentaires. Protocole : 1 page 196.
Quel est le spectre d’absorption de la chlorophylle ?
La chlorophylle b absorbe fortement à 445 nm (bleu) et 645 nm (rouge) Spectres d'absorption des chlorophylles a et b
Quelle est la longueur d'onde de la chlorophylle ?
Les chlorophylleset les caroténoïdesabsorbent certaines radiations dites actives pour la photosynthèse, dans la gamme de longueurs d'onde visibles comprises entre 400 et 700 nm. L'absorption maximale se réalise - dans le bleu (< 500nm) et - dans le rouge (650-700 nm).
TP n°6
Correction
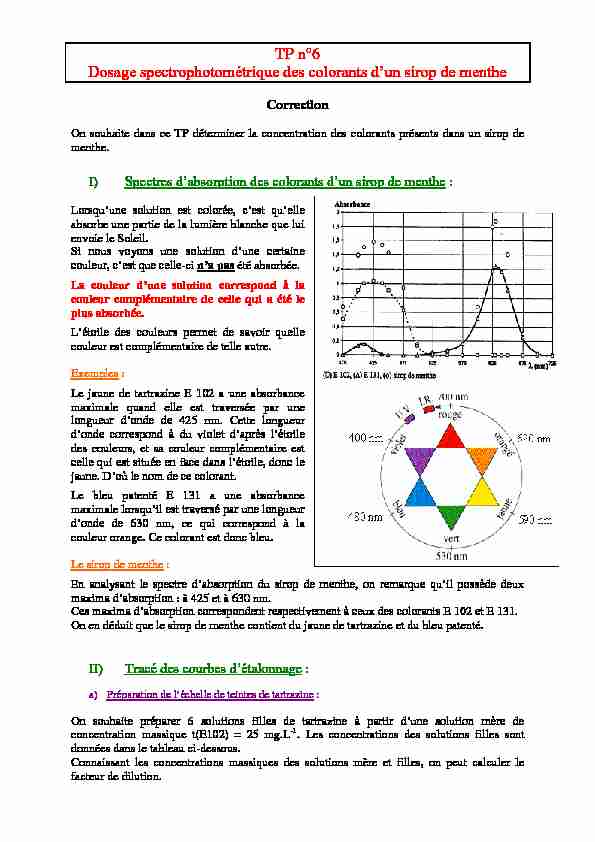
On souhaite dans ce TP déterminer la concentration des colorants présents dans un sirop de menthe. I) : absorbe une partie de la lumière blanche que lui envoie le Soleil. couleur complémentaire de celle qui a été le plus absorbée. couleur est complémentaire de telle autre.Exemples :
Le jaune de tartrazine E 102 a une absorbance
maximale quand elle est traversée par une5 nm. Cette longueur
des couleurs, et sa couleur complémentaire estLe bleu patenté E 131 a une absorbance
maximale lorsq couleur orange. Ce colorant est donc bleu.Le sirop de menthe :
On en déduit que le sirop de menthe contient du jaune de tartrazine et du bleu patenté.II) :
a) e teintes de tartrazine : concentration massique t(E102) = 25 mg.L-1. Les concentrations des solutions filles sont données dans le tableau ci-dessous. Connaissant les concentrations massiques des solutions mère et filles, on peut calculer le facteur de dilution.On sait que :
0VV(fille)
t(fille) t(E102)dilutionfacteur Sachant que V(fille) = V0 + Veau, on a : Veau = V(fille) V0.On peut donc compléter le tableau :
Tube 1 2 3 4 5 6
t(fille) mg/L 5 10 12.5 15 20 25V(fille) en mL 10 10 10 10 10 10
Veau en mL 8 6 5 4 2 0
V0 en mL 2 4 5 6 8 10
Remarque :
rapport des concentrations, et que Cmassique = Cmolaire b) Mesures :Pour cela, il
seule la tartrazine absorbe. seront les plus grandes possibles, de manière à minimiser les incertitudes relatives.440 nm (le bleu patenté absorbe très légèrement à 425
nm si vous regardez bien le spectre).Le réglage du zéro du spectrophotomètre est une étape importante. On peut assimiler ça à la
balance. Si le solvant avec lequel sont préparées les solutions absorbe légèrement à prendre en compte cette éventuelle absorbance (comme la tare que permet de ne pas prendre ne compte la masse de la coupelle lorsque vous pesez un solide).Tube 1 2 3 4 5 6
A 0,26 0,41 0,5 0,61 0,83 1,00
On obtient le graphe A = f(t)
suivant :Rq : t = titre = concentration
massique, ne confondez pas avec le temps, ici !!!! A = f(t) pour quelques solutions de jaune tartrazine y = 0,0382x + 0,0443R2 = 0,995
0 0,2 0,4 0,6 0,8 1 1,2051015202530
t (mg/L) A c) Bleu patenté : On souhaite maintenant réaliser une gamme étalon avec le bleu patenté. On a une solution mère pour laquelle t (E 131) = 10 mg.L-1.Pour préparer les solutions étalons par dilution, les calculs sont les mêmes que pour le jaune
de tartrazine, puisque les facteurs de dilution sont les mêmes. On obtient le tableau :Tube 1 2 3 4 5 6
t(fille) mg/L 2.0 4.0 5.0 6.0 8.0 10.0V(fille) en mL 10 10 10 10 10 10
Veau en mL 8 6 5 4 2 0
V0 en mL 2 4 5 6 8 10
En raisonnant comme précédemment, on règle cette fois le spectrophotomètre sur la longueur
630 nm.
On fait le réglage du zéro.
Tube 1 2 3 4 5 6
A 0,38 0,58 0,74 0,88 1,08 1,41
On trace le graphe A = f(t) :
III) Détermination de la concentration des colorants dans le sirop de menthe : Pour déterminer les concentrations des deux colorants dans le sirop de menthe, il faut faire déterminées précédemment pour que chaque mesure corresponde à un des colorants seul.La manipulation est donc simple
spectrophotomètre et on mesure son absorba A = f(t) pour quelques solutions de jaune tartrazine y = 0,128x + 0,0986R2 = 0,9932
0 0,2 0,4 0,6 0,8 1 1,2 1,4 1,6024681012
t (mg/L) A A = f(t) pour quelques solutions de bleu patentéProblème :
spectrophotomètre, il est donc nécessaire de le diluer au préalable. de - à 440 nm : A = 0,51 - à 630 nm : A = 0,91 On en déduit les concentrations des colorants dans le sirop de menthe dilué par report sur les - jaune : t = 12,5 mg.L-1 - bleu : t = 6,3 mg.L-1Le sirop ayant été dilué 10 fois, les concentrations dans le sirop de menthe commercial sont :
- jaune : t = 125 mg.L-1 - bleu : t = 63 mg.L-1Remarque :
Les deux graphes tracés permettent bien de retrouver la loi de Beer-Lambert : A = kc,
spectrophotométrique permet de déterminer la concentration dquotesdbs_dbs30.pdfusesText_36[PDF] les éléments constitutifs de l'etat évolution ou continuité
[PDF] exercice synthèse despèces chimiques seconde
[PDF] enjeux et objectifs dun projet
[PDF] enjeux sociaux développement durable
[PDF] facteurs économiques: définition
[PDF] facteur économique de la consommation
[PDF] facteur sociologique définition
[PDF] facteur economique wikipedia
[PDF] déterminant économique de la consommation
[PDF] facteurs économiques de la croissance
[PDF] les différents facteurs économiques
[PDF] facteurs économiques de la consommation des ménages
[PDF] devenir hotesse de lair taille minimum
[PDF] hotesse de lair formation
