 Extraction par solvant : étude et modelisation du systeme
Extraction par solvant : étude et modelisation du systeme
organiques et inorganiques en équilibre entre un solvant organique et l'eau. Le potentiel chimique de M dans les deux phases μ et org μ est le même quand le
 TECHNIQUE: Extraction liquide-liquide
TECHNIQUE: Extraction liquide-liquide
S'il s'agit d'un solvant organique la goutte va sécher rapidement. 6 L'extraction est d'autant plus efficace que la substance à extraire est plus soluble ...
 UN PROCEDE PAR SOLVANT POUR LEXTRACTION DU
UN PROCEDE PAR SOLVANT POUR LEXTRACTION DU
extraction sélec- tive des nitrates par solvant organique comprenant une extraction simultanée du plutonium et de l'uranium
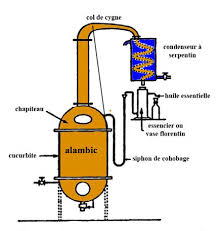 Extraction Sans Solvant Assistée par Micro-ondesConception et
Extraction Sans Solvant Assistée par Micro-ondesConception et
7 déc. 2006 LCSNSA une nouvelle méthode d'extraction sans solvant organique utilisant les micro-ondes comme source de chauffage a été élaborée ...
 Extraction liquide-liquide de larsenic de lantimoine
Extraction liquide-liquide de larsenic de lantimoine
https://inis.iaea.org/collection/NCLCollectionStore/_Public/13/647/13647149.pdf
 these finale
these finale
Vu les temps d'extraction très longs l'extraction aux solvants organiques procédé à une extraction au solvant organique sur les échantillons traités par DIC ...
 Chapitre 2 : Les grandes familles de solvants organiques
Chapitre 2 : Les grandes familles de solvants organiques
D'après Cohr un solvant organique est un composé chimique ou un en alicycliques
 Séparation de composés par extraction acido-basique Extraction
Séparation de composés par extraction acido-basique Extraction
Nous savons que les produits organiques chargés sont plus solubles dans l'eau que dans un solvant organique. En faisant varier le pH de la solution aqueuse il
 Extraction fractionnement et concentration des huiles marines
Extraction fractionnement et concentration des huiles marines
Des fractions plus ou moins purifiées en AGPI sont obtenues par cristallisation à froid en présence de solvants organiques
 Fiche extraction.pdf
Fiche extraction.pdf
Pour l'extraction continue la solution à extraire est alimentée par un solvant pur recyclé en continue par distillation. 5. Lavage d'une phase organique. ▫ Le
 Polycopié du Cours: Techniques dextraction de purification et de
Polycopié du Cours: Techniques dextraction de purification et de
1) Solvants organiques. 2) Types d'extraction (solvant aqueuse
 Techniques conventionelles et innovantes et solvants alternatifs
Techniques conventionelles et innovantes et solvants alternatifs
24 juin 2013 4.1 L'extraction par solvant organique. Les lipides des micro-algues sont stockés au sein des cel- lules qui peuvent être protégées par une ...
 EXTRAIRE DES ESPÈCES CHIMIQUES DUN SOLVANT
EXTRAIRE DES ESPÈCES CHIMIQUES DUN SOLVANT
L'extraction est utilisée en chimie pour séparer des mélanges. On met en contact deux liquides non-miscibles appelés phase organique et phase aqueuse dans une
 TECHNIQUE: Extraction liquide-liquide
TECHNIQUE: Extraction liquide-liquide
un capillaire et la déposer sur une plaque CCM. S'il s'agit d'un solvant organique la goutte va sécher rapidement. 6. Principe
 Extraction liquide-liquide : théorie applications
Extraction liquide-liquide : théorie applications
https://www.ata-journal.org/articles/ata/pdf/2010/02/ata100009.pdf
 UN PROCEDE PAR SOLVANT POUR LEXTRACTION DU
UN PROCEDE PAR SOLVANT POUR LEXTRACTION DU
tive des nitrates par solvant organique comprenant une extraction simultanée du plutonium et de l'uranium
 Coefficient de partage
Coefficient de partage
On considère le partage d'un soluté entre l'eau et un solvant non miscible D'où la concentration du soluté dans la phase organique après extraction :.
 Extraction des sous-produits de la vigne du vin par eau sous-critique
Extraction des sous-produits de la vigne du vin par eau sous-critique
1 sept. 2016 L'hydrodistillation ou l'extraction par solvant est la méthode ... solvants organiques) en augmentant la pression à 5 MPa et la température ...
 Traitements de léchantillon biologique avant lanalyse
Traitements de léchantillon biologique avant lanalyse
d'extraction peut être fonction du mode de détection choisi. C'est ainsi que les extraits (ou le sérum) avec le solvant organique va entraîner une.
 L'extraction liquide-liquide - CultureSciences-Chimie
L'extraction liquide-liquide - CultureSciences-Chimie
Les principales techniques d’extraction de séparation et d’analyse Figure 1 Exemples de techniques de prétraitement des échantillons environnementaux extraction par solvants échangeurs d’ions coprécipitation électrodéposition techniques membranaires extraction - liquide/liquide - par solvants - en phase solide micro-extraction
 Chapitre 2 : l’extraction d’espèces chimiques - Physagreg
Chapitre 2 : l’extraction d’espèces chimiques - Physagreg
Nous avons effectué une extraction par solvant 2) Principe : L’extraction par solvant consiste à faire passer par solubilisation la substance à extraire dans un solvant Celui-ci peut être de l’eau mais généralement il s’agira d’un solvant organique issu de la chimie du pétrole : cyclohexane éther de pétrole toluène
 leay:block;margin-top:24px;margin-bottom:2px; class=tit ph-chmzrhe-monsitecom1 Série d’exercices avec corrections : Extraction séparation
leay:block;margin-top:24px;margin-bottom:2px; class=tit ph-chmzrhe-monsitecom1 Série d’exercices avec corrections : Extraction séparation
Extraction par solvant 1) A l’aide du tableau de données ci-dessous indiquer le solvant d’extraction le plus approprié pour extraire le benzaldéhyde du sirop d’orgeat en justifiant votre réponse Solvant Eau Ether diéthylique Ethanol Solubilité du benzaldéhyde dans ce solvant grande très grande très grande
Comment calculer l'extraction d'un solvant organique ?
À titre d'exemple, considérons l'extraction de n 0 mole de A en solution dans aqueuse de volume V a q par un volume V o r g de solvant organique. La relation K p = [ A o r g] / [ A a q] = ( n o r g / V o r g) / ( n a q / V a q) donne n o r g = ( K p V a q / V o r g) n a q.
Qu'est-ce que la fiche de solvants organiques ?
Cette fiche est la première d'une série consacrée aux différentes familles de solvants organiques et qui se propose de fournir, pour chaque famille, un condensé des connaissances utiles. - bibliographie sélective.
Comment extraire du solvant en plusieurs fois ?
On peut montrer que pour un volume donné de solvant d'extraction, il est plus efficace de procéder en plusieurs extractions avec des fractions de ce volume qu'en une seule fois [1]. À titre d'exemple, considérons l'extraction de n 0 mole de A en solution dans aqueuse de volume V a q par un volume V o r g de solvant organique.
Comment extraire le soluté ?
On peut quand-même extraire le soluté en utilisant un agent de transfert de phase. Un agent de transfert de phase est une substance qui réagit avec le soluté et le transforme en une espèce plus soluble dans le solvant d'extraction. Considérons par exemple les ions permanganate MnO4- en solution aqueuse à extraire par le toluène [2].
TECHNIQUE:
Extraction liquide-liquide
2Extraction liquide-liquide
L'extraction liquide-liquide est une méthode de purification basée sur la différence de solubilitéd'un soluté dans deux phases non miscibles. En chimie organique, on utilise habituellement une phase aqueuseet une phase organique.Matériel utilisé:
• Ampoule à décanter • Bouchon • Support à ampoule • Entonnoir • Cylindre gradué • Erlenmeyers 2 3Tableau de miscibilité des solvants
4Solvants organiques de choix
Notez bien la densitédes différents solvants. Cela vous permettra de savoir si la phase organique se retrouve au- dessusou en-dessousde la phase aqueuse dans l'ampoule à décanter.Tableau en page 49 de votre plan de cours
3 5Solvants organiques
Voici deux trucssi l'on ne sait pas si la phase organique se trouve en-haut ou en-bas dans l'ampoule à décanter: •Ajouter quelques gouttes d'eau et regarder dans quelle phase elles se mélangent. •Prélever un peu de liquide de la phase supérieure avec un capillaire et la déposer sur une plaque CCM. S'il s'agit d'un solvant organique, la goutte va sécher rapidement. 6Principe de l'extraction
L'extraction consiste à faire passer un produit d'un solvant dont il est difficile à séparer (eau) à un autre solvant dont il sera facilement isolable (solvant organique).Phases
org. aq.Agitation
manuellePenser à
laisser sortir la pression par le robinet 4 7Problèmes rencontrés
1) Formation d'une émulsion
Solutions:
ĺ Patienter
ĺ Ajouter du sel (NaCl)
ĺ Filtrer
ĺ Centrifuger
ĺ Ajouter quelques gouttes de solvant polaire (MeOH,EtOH, acétone)
2) Produits d'interface
Solutions:
ĺ Les prélever dans la phase organique (extraction) ĺ Les éliminer dans la phase aqueuse (lavage) 8Extraction d'un produit organique
L'extraction est d'autant plus efficace que la substance à extraire est plus soluble dans le solvant d'extraction que dans son solvant original. ĺ Les produits organiques neutressont beaucoup plus solubles dans les solvants organiques que dans l'eau. Mais ils peuvent être un peu ou beaucoup solubles dans l'eau. ĺ Les sels inorganiques et les composés organiques chargéssont plus solubles dans l'eau que dans les solvants organiques, d'où l'intérêt de connaître le pKa des produits et le pH des solutions. 5 9Coefficient de partage
La solubilité d'un corps pur dans un solvant est fonction de sa polarité. Deux composés de polarité proche sont solubles entre eux, alors qu'un composé non polaire est insoluble dans un solvant polaire (et vice versa). Lors de la mise en présence d'un composé et de deux liquides non miscibles, il s'établit un équilibre caractérisé par le rapport des concentrations du soluté dans chacune des deux phases.Cet équilibre est fixe pour des conditions
thermodynamiques fixes. Soit un produit A qu'on veut extraire d'une phase aqueuse:Coefficient de partage
A OHA org CCK 2 10Coefficient de partage
K=Corg
Caq =m Vorg Vaq m 1 x K= (m 0 -m 1VorgVaq
m 1 m 1 m 0KVorg+VaqVaq
Soit: m
0 la masse initiale du composé A dans l'eau m 1 la masse restante du composé A dans l'eau après une extraction m la masse du composé extraite par le solvantPuisque m
1 = m 0 -m: Si l'on effectue une deuxième extraction avec le même volume de solvant: m 2 m 1KVorg+VaqVaqKVorg+VaqVaq
m 0 2 6 11Coefficient de partage
Il vaut mieux faire 4 extractions avec 50 mL que deux extractions avec 100 mL!On obtient la formule suivante avec nextractions:
Soit d'un composé dans l'eau (50 mL), avec un coefficient de partage de 1. Comparons: • 4 extractions de 50 mL: m 4 = 100 x (50 / 100) 4 = 6.25 g • 2 extractions de 100 mL: m 2 = 100 x (50 / 150) 2 = 11.11 g Il reste plus de produit dans la phase aqueuse après deux extractions avec100 mL de solvant, qu'après quatre extractions avec 50 mL.
m n =m 0KVorg+VaqVaq
n 12Pour améliorer l'extraction
On ne connaît habituellement pas le coefficient de partage de notre produit. On utilise souvent le même volume de solvant que celui de la phase aqueuse. On effectue normalement 2-3 extractions de la phase aqueuse. On peut vérifier par CCM qu'il ne reste plus de produit dans la phase aqueuse. On peut modifier le coefficient de partage du produit en ajoutant un peu de saumure (solution aqueuse saturée en NaCl) dans la phase aqueuse. On appelle ce phénomène le relargage ("salting-out »). 7 13Lavage et séchage
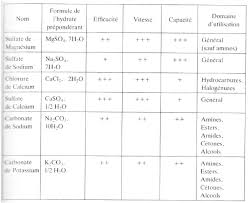
Il peut être nécessaire de laver les phases organiques combinéespour ajuster le pH ou enlever un solvant polaire de haut point d'ébullition (DMF ou DMSO avec de l'eau) ou enlever les traces d'eau (avec une solution aqueuse saturée en NaCl = saumure). Attention, ce n'est pas du relargage !!!! On finit toujours par sécher ces phases organiquespour enlever toute trace d'eau. On utilise pour cela un sel possédant une forte affinité pour l'eau. On en met assez pour que le solide reste sous forme de légère suspension à l'agitation. C'est le moment parfait pour prendre une CCMde notre produit brut. 14Sels asséchants
Tableau en page 49 de votre plan de cours
8 15Filtration et évaporation
Pour enlever le sel dessèchant, la solution est filtrée à travers un entonnoir + papier filtre, directement dans un ballon taré. Le ballon ne doit pas être rempli plus que les 2/3. Pour récupérer notre produit brut, il ne reste plus qu'àévaporer le solvant.
Cela se fait à l'évaporateur rotatif, aussi appelé rotavap. 16Cahier de laboratoire
Indiquez dans votre cahier:
•les solvants d'extraction utilisés, avec les volumes •les solutions de lavage utilisées, avec les volumes •le sel asséchant utilisé •tout changement de couleur que vous avez pu observer •la CCM de votre produit brut.quotesdbs_dbs5.pdfusesText_10[PDF] processus d extraction du cuivre
[PDF] extraction solide liquide pdf
[PDF] extraction solide liquide principe
[PDF] extraction solide liquide soxhlet
[PDF] l environnement et ses problèmes
[PDF] matière organique exemple
[PDF] matière organique du sol
[PDF] degradation de l environnement causes et consequences pdf
[PDF] matière organique composition
[PDF] matière organique et minérale
[PDF] protocole extraction solide liquide
[PDF] matière minérale
[PDF] chromophore definition
[PDF] extraction liquide liquide coefficient de partage
