 Coefficient de partage
Coefficient de partage
Soit V et V / les volumes respectifs de la phase aqueuse et de la phase organique. Soit C0 la concentration du soluté dans la phase aqueuse avant extraction. 1
 TECHNIQUE: Extraction liquide-liquide
TECHNIQUE: Extraction liquide-liquide
On ne connaît habituellement pas le coefficient de partage de notre produit. On utilise souvent le même volume de solvant que celui de la phase aqueuse. On
 Coefficient de partage
Coefficient de partage
En déduire la quantité extraite avec le solvant organique. 3. Dans le cas d'une extraction liquide-liquide le coefficient de partage K est défini comme le
 ÿþC o n c o u r s d I n t e r n a t b l a n c G a l i e n
ÿþC o n c o u r s d I n t e r n a t b l a n c G a l i e n
10 mars 2012 Soit un acide faible aH que l'on souhaite extraire via une extraction liquide/liquide grâce au chloroforme ... coefficient de partage ...
 Simulation du rendement et du coefficient de distribution dans une
Simulation du rendement et du coefficient de distribution dans une
2 juil. 2007 le(s) taux de partage dans une extraction liquide-liquide afin de prévoir dans quelles conditions cette opération est favorable défavorable ...
 EXTRAIRE DES ESPÈCES CHIMIQUES DUN SOLVANT
EXTRAIRE DES ESPÈCES CHIMIQUES DUN SOLVANT
26 mars 2020 du lait) est mesurée par le coefficient de partage vapeur/liquide suivant : Log P = Log (C vap. /C liq. ) où C vap est la concentration d ...
 CPGE Brizeux
CPGE Brizeux
Sélectionner la verrerie adaptée à la précision requise. Réaliser. • Respecter les consignes de sécurité. • Mettre en œuvre une extraction liquide-liquide.
 Extraction liquide-liquide : extraction de lacide benzoïque
Extraction liquide-liquide : extraction de lacide benzoïque
Les objectifs de notre activité sont multiples : • Déterminer un coefficient de partage. • Montrer qu'il est préférable de faire deux extractions successives
 TP n°5 Extraction de lacide benzoïque et mesure dun coefficient de
TP n°5 Extraction de lacide benzoïque et mesure dun coefficient de
Première partie : extraction simple et mesure du coefficient de partage. 1 Conclure. Page 3. FICHE : L'extraction liquide-liquide. 1) Définitions. Soit un ...
 Extraction liquide-liquide : théorie applications
Extraction liquide-liquide : théorie applications
https://www.ata-journal.org/articles/ata/pdf/2010/02/ata100009.pdf
 Extraction liquide-liquide : extraction de lacide benzoïque
Extraction liquide-liquide : extraction de lacide benzoïque
coefficient de partage et efficacité des extractions successives. Présentation générale de la manipulation. Le matériel de l'extraction liquide-?liquide
 TECHNIQUE: Extraction liquide-liquide
TECHNIQUE: Extraction liquide-liquide
On ne connaît habituellement pas le coefficient de partage de notre produit. On utilise souvent le même volume de solvant que celui de la phase aqueuse. On
 ÿþC o n c o u r s d I n t e r n a t b l a n c G a l i e n
ÿþC o n c o u r s d I n t e r n a t b l a n c G a l i e n
10 mars 2012 Le coefficient de partage acétate d'éthyle/ eau injectable est égal à 50. ... Le solvant d'extraction et le liquide d'échantillon ne doivent ...
 Extraction liquide-liquide : théorie applications
Extraction liquide-liquide : théorie applications
https://www.ata-journal.org/articles/ata/pdf/2010/02/ata100009.pdf
 Extraction liquide-liquide.pdf
Extraction liquide-liquide.pdf
L'extraction liquide-liquide est basée sur la distribution d'un soluté entre deux solvants en fonction de sa solubilité dans chacun d'entre eux. Coefficient
 Simulation du rendement et du coefficient de distribution dans une
Simulation du rendement et du coefficient de distribution dans une
2 juil. 2007 Extraction liquide-liquide partage
 Fiche extraction.pdf
Fiche extraction.pdf
L'extraction consiste à traiter un mélange homogène ou non de liquides ou de solides par un solvant pur appelée coefficient de partage.
 Extraction liquide-liquide : extraction de lacide benzoïque
Extraction liquide-liquide : extraction de lacide benzoïque
coefficient de partage et efficacité des extractions successives. Présentation générale de la manipulation. Le matériel de l'extraction liquide-?liquide
 Coefficient de partage
Coefficient de partage
Soit V et V / les volumes respectifs de la phase aqueuse et de la phase organique. Soit C0 la concentration du soluté dans la phase aqueuse avant extraction. 1
 EXTRAIRE DES ESPÈCES CHIMIQUES DUN SOLVANT
EXTRAIRE DES ESPÈCES CHIMIQUES DUN SOLVANT
Objectif Être capable de comprendre la notion d'extraction liquide- traduit scientifiquement par un coefficient de partage solvant/eau en faveur de la.
 Extraction liquide-liquide
Extraction liquide-liquide
L’extraction liquide-liquide est basée sur la distribution d’un soluté entre deux solvants en fonction de sa solubilité dans chacun d’entre eux Coefficient de partage et taux de distribution Le schéma classique de la séparation est l’extraction par un solvant organique B d’un soluté S
 Chapitre 9 Extraction liquide-liquide: Introduction et
Chapitre 9 Extraction liquide-liquide: Introduction et
variable X Coefficient de partage = la pente de la droite Y*=f(X) Exemple: Pour extraire le DMSO (diméthyl sulfoxide) mélangé avec du benzène (le diluant) on utilise comme solvant l'eau Lecoefficientde partage de ce système vaut: /' 2000 / gdeDMSO gd eau m g de DMSO g debenzène Plus le coefficient de partage est élevé plus le soluté
 TECHNIQUE: Extraction liquide-liquide - Zysman-Colman
TECHNIQUE: Extraction liquide-liquide - Zysman-Colman
Coefficient de partage Il vaut mieux faire 4 extractions avec 50 mL que deux extractions avec 100 mL! On obtient la formule suivante avec n extractions: Soit 100 g d’un composé dans l’eau (50 mL) avec un coefficient de partage de 1 Comparons: • 4 extractions de 50 mL: m4 = 100 x (50 / 100) 4 = 6 25 g
 Coe?cient de partage - Université de Limoges
Coe?cient de partage - Université de Limoges
Coe?cient de partage 1 Dé?nition On considère le partage d’un soluté entre l’eau et un solvant non miscible (hexane éther chloroforme octanol ) Le coe?cient de partage P est égal au rapport des concentrations du soluté dans les deux phases : P = C? C C C’ Eau (saturée de solvant) Solvant (saturé d’eau)
 Searches related to extraction liquide liquide coefficient de partage PDF
Searches related to extraction liquide liquide coefficient de partage PDF
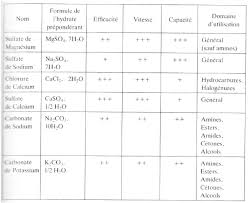
Dc : coefficient de distribution = ? : coefficient de partage n : nombre d’extractions 1 5 Applications de l’extraction liquide-liquide : Application Mode d’extraction Facteurs influant sur l’extraction (coef de partage +++) Extraction de molécules simples Solvant organique • structure de la molécule : longueur de la chaîne
Qu'est-ce que l'extraction liquide-liquide?
L’extraction liquide-liquide met à profit les différences de solubilité d'un composé entre deux phases liquides. Pour séparer le produit cible (le soluté) d'une phase liquide donnée (le diluant), on rajoute au système un solvant
Comment calculer l'extraction d'un solvant organique ?
À titre d'exemple, considérons l'extraction de n 0 mole de A en solution dans aqueuse de volume V a q par un volume V o r g de solvant organique. La relation K p = [ A o r g] / [ A a q] = ( n o r g / V o r g) / ( n a q / V a q) donne n o r g = ( K p V a q / V o r g) n a q.
Comment faire une extraction en continu ?
Extraction en continu Si K p est très inférieur à 1 et que la nature du soluté ne permet pas de mettre en oeuvre le transfert de phase, on peut réaliser une extraction en continu. On utilise pour cela un montage qui permet de recycler le solvant d'extraction (figure 7).
Comment calculer le coefficient de partage ?
Considérons un soluté A en solution dans l'eau à extraire par une phase organique non-miscible à l'eau. Lorsque les deux phases liquides sont en contact il s'établit un équilibre de partage pour A (figure 1). Cet équilibre est caractérisé par une constante thermodynamique K p appelée le coefficient de partage : K p = [ A o r g] / [ A a q] 1.
Exercice n°1 - 1 -
NOM : VILLE : Prénom : Note sur : / 40 INTERNAT PHARMACIE EXERCICE N°1 40 POINTS Date : Samedi 10 mars 2012
Exercice n°1 - 2 -
Partie A : On souhaite doser un médicament X dans une solution injectable à 45mg/L par une extraction liquide/liquide. On extrait 10mL de soluté injectable par 2mL d'acétate d'éthyle. Le coefficient de partage acétate d'éthyle/ eau injectable est égal à 50. Dans cette partie, on sait que X n'est ni dissocié ni dimérisé dans la phase organique. 1/ Quelles sont les conditions nécessaires pour une extraction de bonne qualité ? 2/ Calculer la quantité de X extraite ainsi que la quantité restante dans la phase aqueuse et le rendement de l'extraction. 3/Quelle pourcentage restera-t-il après 5 extractions successives par 1mL d'acétate d'éthyle ? Partie B : Soit un acide faible aH, que l'on souhaite extraire via une extraction liquide/liquide grâce au chloroforme de formule CHCl3. 1/ A quel pH devra-t-on se placer afin d'avoir une extraction optimale ? 2/ Démontrer la formule du coefficient de partage conditionnel ou taux de distribution à partir du pKa, de la concentration en H3O+ et des concentrations de aH dans les phases aqueuse et organique. 3/ On prépare deux échantillons de 100mL de solution aqueuse de concentration égale à 45mg/L. Sachant qu'en tamponnant à : pH=1, la solution étant extraite avec 50mL de CHCl3, la phase aqueuse après extraction contient 5,35 x10-3 mg ; et pH= 4, la solution étant extraite avec 50mL de CHCl3, la phase aqueuse après extraction contient 13,5 x10-3 mg. Calculer le coefficient de partage aH/CHCl3 et le Ka.
Correction Exercice n°1 - 1 -
CORRECTION INTERNAT PHARMACIE EXERCICE N°1 CHIMIE ANALYTIQUE Date : Samedi 10 mars 2012
Correction Exercice n°1 - 2 -
Partie A : 1/ L'extraction correspond au passage partiel d'un soluté d'un liquide d'échantillon vers un solvant d'extraction. Elle repose sur la différence d'affinité du soluté entre deux phases liquides non-miscibles entre elles. • Le solvant d'extraction et le liquide d'échantillon ne doivent pas être miscibles l'un dans l'autre; (0,25) • Si le composé est un acide faible ou une base faible, tenir compte de l'influence du pH; (0,25) • L'extraction nécessite une agitation (0,25) afin d'augmenter l'interface entre les deux phases et d'atteindre l'équilibre plus rapidement (0,25); • Le solvant d'extraction doit présenter une grande solubilité pour le soluté à extraire (0,25) → il faut sélectionner le solvant ayant le P le plus grand. (0,25) 3 2/ Vorg= volume d'acétate d'éthyle= 2mL (0,25) Vaq= volume de soluté injectable= 10mL (0,25) P= coefficient de partage ou D ou λ = 50 (0,25) Co= concentration initiale dans la solution aqueuse= 45mg/L (0,25) Cn= concentration restante dans la solution aqueuse après extraction (0,25) qo = quantité de X initiale (0,25) qn = quantité de X restant dans la phase aqueuse (0,25) qorg = quantité de X dans la phase organique (0,25) Cn= Co x (1/ (1+ P x Vorg/Vaq )) (1) Cn= 4,091mg/L (1) qn = Cn x Vaq (0,5)= 0,041mg (0,5) qo= Co x Vaq (0,5) = 0,45 mg (0,5) qorg= qo - qn (0,5) = 0,409 mg (0,5) Rendement = R= qorg /qo (0,25)= 91% (1) 8 3/ Cn = Co x (1/ (1+ P x Vorg/Vaq ) )n (2) Avec n = nombre d'extractions (0,25) Cn/Co = (1/ (1+ P x Vorg/Vaq ) )5 (0,25) Cn/Co= 0,013% (0,5) 3
Correction Exercice n°1 - 3 -
Correction Exercice n°1 - 4 -
Donc 166 = P x (1/ (1 + Ka / H3O+)) (1) 166 = P x (1/ (1 + Ka / 10-1)) (0,5) Et 64.7 = P x (1/ (1 + Ka / H3O+)) (1) 64.7 = P x (1/ (1 + Ka / 10-4)) (0,5) Alors P = 166 x (1 + Ka / 10-1) = 64.7 x (1 + Ka / 10-4) (2) 166 + 166 x Ka/ 10-1 = 64.7 + 64.7 x Ka / 10-4 166 + 1660 Ka = 64.7 + 647 000 Ka 101.3 = 645 340 Ka Ka = 1.57 x 10-4 (2) pKa = 3.8 (1) P = 166 x (1 + 1.57 x 10-4 / 10-1) P = 166.26 (2) Ou P = 64.7 x (1+ 1.57 x 10-4 / 10-4) P = 166.28 15
quotesdbs_dbs26.pdfusesText_32[PDF] chromophore uv
[PDF] tp extraction liquide liquide
[PDF] les indicateurs de croissance économique pdf
[PDF] distillation protocole
[PDF] indicateur de croissance bébé
[PDF] extraction liquide liquide pdf
[PDF] extraction liquide liquide cours pdf
[PDF] les principaux indicateurs du niveau de développement d'un pays
[PDF] coefficient 1ere es
[PDF] indicateur de croissance definition
[PDF] indicateur de croissance d'une entreprise
[PDF] système scolaire espagnol et français
[PDF] système scolaire espagnol vacances
[PDF] horaire de cours en espagne
