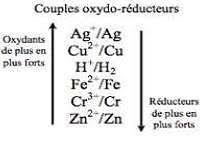
 TD3: Corrosion et moyens de protection (correction)
TD3: Corrosion et moyens de protection (correction)
Exercice 1: Corrosion du fer. Afin de protéger des pièces contre la corrosion il est surface de contact entre ces deux métaux. L'eau joue le role d'un ...
 EXERCICE III Corrosion et protection des métaux
EXERCICE III Corrosion et protection des métaux
PROTECTION DES METAUX correction. 1. Il s'agit de recouvrir la plaque de fer d'une couche de zinc par électrolyse. Sur la plaque de fer se produit donc ...
 Corrigés dexercices doxydoréduction : TD Echi1-1 et TD Echi1-2
Corrigés dexercices doxydoréduction : TD Echi1-1 et TD Echi1-2
Exercice 2 : Accumulateur lithium métal. [oral banque PT
 EXERCICE III Corrosion et protection des métaux
EXERCICE III Corrosion et protection des métaux
Exercice-1 : Corrosion et protection des métaux. La corrosion est un fléau industriel. On estime en effet que 20% de la production mondiale d'acier (mélange
 CORRIGE
CORRIGE
25 mars 2016 05 Pt CORROSION : le métal est oxydé sous une forme ionique soluble. ... TROISIEME EXERCICE Centrale MP Phys-‐Chimie 2 205. ÉTUDE D'UN ALLIAGE Ag ...
 Corrosion et protection des métaux
Corrosion et protection des métaux
8- Calculer la masse de zinc nécessaire à la protection de la carcasse pour une durée de 6 mois. Exercice 3 : (type BTS). La corrosion est un fléau industriel.
 Exercices Comment protéger un véhicule contre la corrosion ? T3
Exercices Comment protéger un véhicule contre la corrosion ? T3
oxydée et réduite du fer. 2) Quel est du cuivre ou du zinc le métal qui assurera une protection efficace du fer ? Pourquoi ? (D
 CORRIGE
CORRIGE
Exercice 3 - Corrosion acide. 35 points. 3.1. E(H+/H2) = - 0
 Série dexercices : Oxydation des métaux dans lair
Série dexercices : Oxydation des métaux dans lair
Exercice 4 : Le fer est un métal utilisé dans plusieurs domaines et il est nécessaire de le protéger contre la corrosion. 1- Décrire le phénomène qui se
 Exercice N°1 : 1)- Compléter les réactions chimiques suivantes : a
Exercice N°1 : 1)- Compléter les réactions chimiques suivantes : a
5)- La corrosion d'un métal par l'air est une oxydation. 6)- Le fer n'est Corriger les réponses fausses : 1)- Un matériau organique contient toujours des ...
 TD3: Corrosion et moyens de protection (correction)
TD3: Corrosion et moyens de protection (correction)
Exercice 1: Corrosion du fer. Afin de protéger des pièces contre la corrosion il est nécessaire 1- Quel est le métal qui se dépose sur le fer ?
 EXERCICE III Corrosion et protection des métaux
EXERCICE III Corrosion et protection des métaux
Sujet 49 : PROTECTION DES METAUX correction. 1. Il s'agit de recouvrir la plaque de fer d'une couche de zinc par électrolyse. Sur la plaque de fer se.
 Corrosion et protection des métaux
Corrosion et protection des métaux
8- Calculer la masse de zinc nécessaire à la protection de la carcasse pour une durée de 6 mois. Exercice 3 : (type BTS). La corrosion est un fléau industriel.
 CORRIGE
CORRIGE
25 mars 2016 PREMIER EXERCICE e2a PC 2015 ... Ce sujet a ... 05 Pt CORROSION : le métal est oxydé sous une forme ionique soluble.
 Soudage et assemblage-soudage Guide dauto-apprentissage
Soudage et assemblage-soudage Guide dauto-apprentissage
Corrigé des exercices . choisir ou de justifier le choix d'un procédé de soudage et d'un métal ... la corrosion ne rouille pas ; c'est le cas des.
 TD 8 : Corrosion
TD 8 : Corrosion
chimie. TD 8 : Corrosion. Exercice 1 : EXTRAIT DE CENTRALE PSI 2003 A.2) La courbe intensité-potentiel du couple H+(aq)/H2 dépend-elle du métal de.
 1re STI2D • Corrosion des métaux et protection
1re STI2D • Corrosion des métaux et protection
Aciers inoxydables métaux nobles. Protection contre la corrosion. Activité expérimentale Mise en évidence expérimentale de la corrosion du fer et de sa
 Rappels atomistiques structure des métaux
Rappels atomistiques structure des métaux
http://campus.cerimes.fr/odontologie/enseignement/chap1/site/html/cours.pdf
 Chapitre 8 – Dégradation des matériaux
Chapitre 8 – Dégradation des matériaux
EXERCICE 8-1. Révision (questions vrai-faux). Corrigé. Énoncé. VRAI. FAUX cathodique apparaissant dans un couple de corrosion auquel ce métal participe.
 CORRIGE
CORRIGE
Exercice 4 - Protection du fer. 325 points. 4.1. Corrosion galvanique. 0
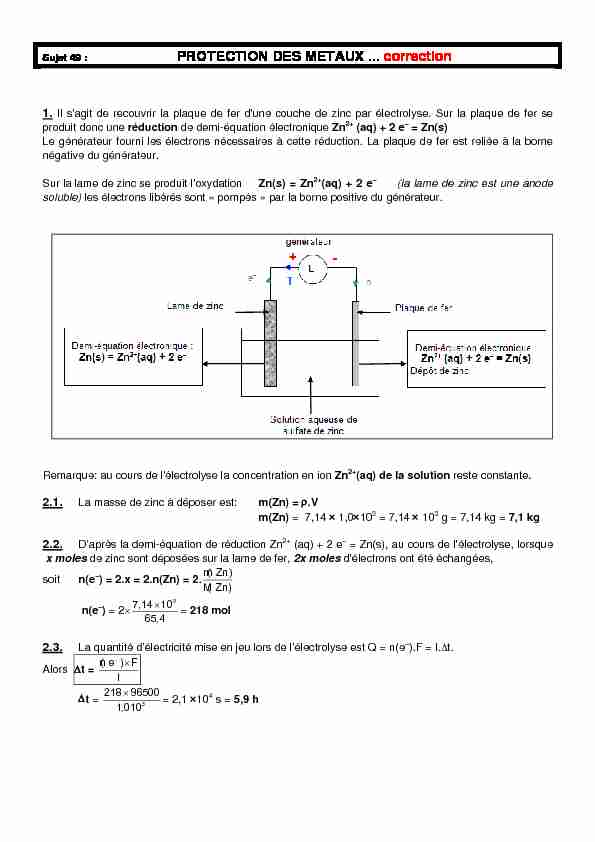 Sujet 49 : PROTECTION DES METAUX ... correction
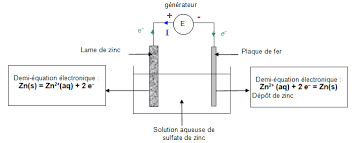
Sujet 49 : PROTECTION DES METAUX ... correction 1. Il s'agit de recouvrir la plaque de fer d'une couche de zinc par électrolyse. Sur la plaque de fer se produit donc une réduction de demi-équation électronique Zn
2+ (aq) + 2 e = Zn(s)Le générateur fourni les électrons nécessaires à cette réduction. La plaque de fer est reliée à la borne
négative du générateur.Sur la lame de zinc se produit l'oxydation
Zn(s) = Zn
2+ (aq) + 2 e- (la lame de zinc est une anodesoluble) les électrons libérés sont " pompés » par la borne positive du générateur.
Remarque: au cours de l'électrolyse la concentration en ion Zn 2+ (aq) de la solution reste constante.2.1. La masse de zinc à déposer est: m(Zn) =
.V m(Zn) = 7,14 1,010 3 = 7,14 10 3 g = 7,14 kg = 7,1 kg2.2. D'après la demi-équation de réduction Zn
2+ (aq) + 2 e- = Zn(s), au cours de l'électrolyse, lorsquex moles de zinc sont déposées sur la lame de fer, 2x moles d'électrons ont été échangées,
soit n(e ) = 2.x = 2.n(Zn) = 2. n(e- ) = 2 = 218 mol2.3. La quantité d'électricité mise en jeu lors de l'électrolyse est Q = n(e
).F = I. t.Alors t =
t = = 2,1 10 4 s = 5,9 hquotesdbs_dbs2.pdfusesText_3[PDF] exercice corrigé cryptographie pdf
[PDF] exercice corrigé cryptographie rsa
[PDF] exercice corrigé cryptographie symétrique
[PDF] exercice corrigé dalgorithme
[PDF] exercice corrigé d'électronique de puissance
[PDF] exercice corrigé de controle interne
[PDF] exercice corrigé de finance publique pdf
[PDF] exercice corrige de genetique pdf
[PDF] exercice corrigé de mecanique analytique
[PDF] exercice corrige de mecanique de lagrange
[PDF] exercice corrige de travaux de fin d'exercice
[PDF] exercice corrigé dosage acido basique
[PDF] exercice corrigé dosage acido basique pdf
[PDF] exercice corrigé dosage conductimétrique
