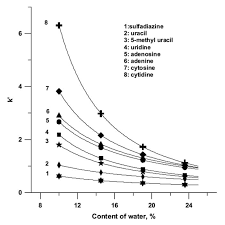
 Exercices CAN 201 Chromatographie liquide 1 Partie I 1. Si pour les
Exercices CAN 201 Chromatographie liquide 1 Partie I 1. Si pour les
en chromatographie liquide en phase inverse (RPLC) pour déterminer le temps mort (t0)?. 4. Déterminez approximativement le volume mort d'une colonne de 5 cm de
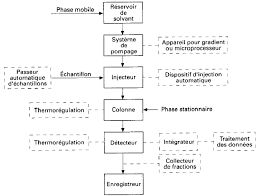 correction exercices 07
correction exercices 07
1 - 4 - Compléter le tableau Avantages et inconvénients des différents types de chromatographie liquide / solide. caractéristiques échange d'ions filtration sur
 Décembre 2015 EXERCICE N° 1 ÉNONCÉ
Décembre 2015 EXERCICE N° 1 ÉNONCÉ
Quel est le type de chromatographie mise en jeu ? Expliquer. Question N°2. Définir l'efficacité d'une colonne chromatographique. Quelle est l'efficacité de la
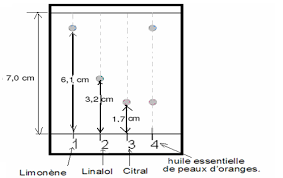 Série dexercices : chromatographie sur couche mince EXERCICE N
Série dexercices : chromatographie sur couche mince EXERCICE N
On réalise la chromatographie de trois corps A. B et C. Le chromatogramme obtenu est le suivant: 1) Faites l'analyse du chromatogramme. 2) Donnez la definition
 Exercices de TD Chromatographie liquide et Gaz H dp * = 3
Exercices de TD Chromatographie liquide et Gaz H dp * = 3
Exercice 1 - Chromatographie en phase liquide. On souhaite réaliser des analyses sur une colonne de 5 cm de long avec un diamètre interne de 46 mm et remplie
 Ex 1 Ex 2 Ex 7 Ex 8 Ex 15 Ex16 Ex 17
Ex 1 Ex 2 Ex 7 Ex 8 Ex 15 Ex16 Ex 17
Exercices corrigés : chromatographie : espèces naturelles et synthétiques p 205. Ex 1. 1. Espèces naturelles : fructose et sorbitol. Espèces synthétiques
 CHROMATOGRAPHIE LIQUIDE - Académie des Sciences et Lettres
CHROMATOGRAPHIE LIQUIDE - Académie des Sciences et Lettres
CHROMATOGRAPHIE GAZ. 79. XI. EXERCICES ET CORRIGES. 80. Page 4. r Jean-Louis CUQ - page 3. I. HISTORIQUE. La chromatographie est une science très ancienne.
 Module LCP3 : Méthodes danalyses Spectroscopiques et
Module LCP3 : Méthodes danalyses Spectroscopiques et
18 déc. 2003 CORRIGÉ. Aucun document n'est autorisé - Les portables doivent être éteints et rangés. On rappelle qu'en chromatographie pour une phase mobile ...
 EXERCICES INTERNAT 2007-2004
EXERCICES INTERNAT 2007-2004
Le coefficient de partage corrigé alpha α = P VBenzène /Veau => α = 3 On sépare 2 composés A et B par chromatographie en phase gazeuse sur une colonne de 20.
 Fiche TD 1 « Chromatographie » - CCM – Exclusion - CPG
Fiche TD 1 « Chromatographie » - CCM – Exclusion - CPG
Exercice 1 : Chromatographie sur couche mince. Sur une plaque CCM en silice nous effectuons les dépôts de quatre solutions dans le dichlorométhane
 ÉPREUVE DEXERCICES DAPPLICATION – Décembre 2015
ÉPREUVE DEXERCICES DAPPLICATION – Décembre 2015
Quel est le type de chromatographie mise en jeu ? Expliquer. Question N°2. Définir l'efficacité d'une colonne chromatographique. Quelle est l'efficacité de la
 univ-oeb
univ-oeb
Exercice 01 : 1. La technique de chromatographie permet de séparer les différentes espèces chimiques présentes dans un mélange et de les identifier par
 Exercices CAN 201 Chromatographie liquide 1 Partie I 1. Si pour les
Exercices CAN 201 Chromatographie liquide 1 Partie I 1. Si pour les
en chromatographie liquide en phase inverse (RPLC) pour déterminer le temps mort (t0)?. 4. Déterminez approximativement le volume mort d'une colonne de 5 cm de
 correction exercices 07
correction exercices 07
La chromatographie est une technique d'analyse pour séparer les constituants d'un mélange ;. • les molécules à séparer sont entraînées par un fluide qui
 chromatographie sur couche mince EXERCICE N 1
chromatographie sur couche mince EXERCICE N 1
EXERCICE N o. 2. On réalise la chromatographie de trois corps A. B et C. Le chromatogramme obtenu est le suivant: 1) Faites l'analyse du chromatogramme.
 Exercices sur la chromatographie
Exercices sur la chromatographie
EXERCICES CHIMIE SPECIALITE TS Exercice 1 Sirop de grenadine ... On extrait ces colorants et l'on effectue la chromatographie sur couche mince des ...
 SERIES DEXERCICES CORRIGES DE BIOCHIMIE STRUCTURALE
SERIES DEXERCICES CORRIGES DE BIOCHIMIE STRUCTURALE
Quel type de chromatographie échangeuse d'ion utilisé ? 2- Indiquer l'ordre de sortie des trois peptides. 3. Peut-on séparer ces peptides lorsqu'on les dépose
 Module LCP3 : Méthodes danalyses Spectroscopiques et
Module LCP3 : Méthodes danalyses Spectroscopiques et
18 déc. 2003 Chromatographiques. Examen de Chromatographie. CORRIGÉ ... dans le cas d'une chromatographie sur colonne de silice la vitesse moyenne u de ...
 EXERCICES INTERNAT 2007-2004
EXERCICES INTERNAT 2007-2004
Le coefficient de partage corrigé alpha ? = P VBenzène /Veau => ? = 3. On sépare 2 composés A et B par chromatographie en phase gazeuse sur une colonne ...
PREUVE D'EXERCICES D'APPLICATION 2005 NORD
[E1-2005N] EXERCICE N¡ 1 (40 points)NONC
1 mg d'un compos X est dissous dans 100 ml d'eau. On effectue une extraction l'aide de 50
- pour la phase aqueuse 240 nm : A 240= 0,26 - pour la phase benznique 235 nm: A 235
= 1,30 Simultanment, on dtermine les absorbances des solutions: aqueuse 1 0 -4 M ou benznique 10 -4
M de X. Les absorbances sont respectivement A
240= 0,72 pour la solution aqueuse et A 235
= 1,20 pour la solution benznique.
RPONSE QUESTION N¡ 1 :
Concentration en X de la phase aqueuse: 10
-4 . ( 0,26/0,72) = 3,61 10 -5 M Concentration en X de la phase benznique: 10-4 . (1,30/1,20) = 1,08 10 -4 M coefficient de partage : P = (1,08 10 -4 )/( 3,61 10 -5 ) = 3 QUESTION N¡ 2 : Quelle est la masse molaire de X?RPONSE QUESTION N¡ 2 :
100 mL de solution aqueuse contient 3,61 10
-5 x 100 mmol = 3,61 micromol50 mL de solution benznique contient 1,08 10
-4 x 50 mmol = 5,40 micromol1 mg = 3,61 + 5,40 = 9,01 micromol
Masse molaire : MM = 1000/9,01 = 111,0 g.mol
-1 QUESTION N¡ 3 : Quel est le rendement de l'extraction?RPONSE QUESTION N¡ 3 :
Ou bien C
= 3 C eau1 mg = 50 C
+ 100 C eau = 250 C eau => C eau = 1/250 = 4.10 -3 mg.mL -1 C = 12 .10 -3 mg.mL -1 -3 mg = 0,6 mg.Rendement = 0.6/1= 60 %
extraire au moins 90 % de X partir de 100 ml de la solution aqueuse?RPONSE QUESTION N¡ 4 :
Le coefficient de partage corrig alpha = P V /V eau => = 3.(50/100) = 1,5 la fin de la 1
extraction, la Qt dans l'eau q e1 = q 0 / (1+ ) = 0,4 mgA la fin de la n
extraction , q en = q 0 / (1+ ) n = 1/(2,5) n => R = (q 0 - q en )/ q 0Le rendement [1-(1/2,5)
n ] " 0,90 => 1/2,5 n # 0,10 => 1 # n log 2,5 => n " 2,5 => n=3 [E2-2005N] EXERCICE N¡ 2 (40 points) Cet exercice se compose de 2 parties A et B indpendantesPARTIE A
NONC
Dans le trai tement d' une maladie, l'un des effets secondaires non attendu pour rait tre lamodification de la concentration d'une protine dans le sang. Pour tudier cette ventualit, on
utilise un chantillon alatoire de 10 patients numrots de 1 10 et, pour chacun d'eux, on
(concentrations exprimes en g.L -lNumro i
du patientConcentration Xi
Avant le traitement
Concentration Yi
1 0,95 0,98
2 0,72 0,72
3 0,82 0,78
4 0,75 0,90
5 0,81 0,98
6 0,88 0,86
7 0,83 0,92
8 0,79 0,74
9 0,70 0,70
10 0,75 0,92
On d signe ci-dessous par P
l la population des patients avant traitement et par P 2 la QUESTION N¡ 1 : Donner les estimations de la concentration moyenne de la protine dans P l et P 2RPONSE QUESTION N¡ 1 :
Moyenne des x
i : x= 0,80 g.L -1 ; Moye nne des y i : y = 0,85 g. L -1Estimations de la moyenne des concentrations:
- avant traitement: 0,80 g.L -1 -1 QUESTION N¡ 2 : Peut-on dire, au risque 0,05, que la concentration de la protine est modifie par le traitement? La rponse devra inclure les lments suivants: - condition(s) de validit du test.RPONSE QUESTION N¡ 2 :
Il s'agit d'chantillons apparis dont les diffrences d i sont:0,03; 0; - 0,04; + 0,15; + 0,17; - 0,02; + 0,09; - 0,05; 0; + 0,17
Le test utiliser est la comparaison de la diffrence moyenne d la valeur 0. Ho: la moyenne de la population des diffrences est gale 0. H1: la moyenne de la population des diffrences est diffrente de 0. Condition de validit du test: la distribution des diffrences d i dans la population doit tre normale.0874,0
1 1 2 n dd s n i i d s md : cart type des moyennes des diffrences => s md = s d /n = 0,0874/10 = 0,0276 t calc = /)0(d s md = 0,05 /0,0276 = 1.81 Lecture de la table de t : ddl = 10 - 1 = 9 ; alpha " = 0,05 t thor = 2,26 t calcul < t thorique : Pas de diffrence significative au risque alpha " = 0,05 Conclusion : Le traitement ne modifie pas la concentration de la protine de faon significative.PARTIE B
NONC
Un instrument de mesure doit donner des rsultats aussi rptables et exacts que possible malgr d'invitables erreurs de mesure.QUESTION N¡ 1 : Lors d'une mesure, les erreurs peuvent tre alatoires et/ou systmatiques;
donner les caractristiques gnrales de ces deux types d'erreur en prcisant ce qui les distingue.RPONSE QUESTION N¡ 1 :
Les erreurs sont dites alatoires si elles se rpartissent au hasard de part et d'autre d'unevaleur moyenne. Elles se traduisent donc lors des rptitions de la mesure par une variabilit
valeurs obtenues.LÕimportance de ces erreurs est val ue globa lement par l'cart type et le coefficient de
variation. En revanche, si les rsultats suivent une tendance, l'erreur peut tre systmatique. Les erreurs systmatiques ne sont pas lies au hasard mais se produisent toujours dans le d'oprations de validation appropries. Dans le cas d'une technique analytique, il est aussi possible de les dtecter par comparaison dursultat obtenu celui o btenu par une techniq ue de rfrence (quand une telle technique
existe).Leur importance est value par l'erreur absolue (delta x : #x = valeur mesure moins valeur
vraie) et l'erreur relative, quotient de l'erreur absolue par la valeur vraie. aqueuse la valeur 4,10. A quelle concentration en ions H 3 O exprime en moI.L -1 , cette valeur correspond-elle?RPONSE QUESTION N¡ 2 :
pH = - log 10 [H3O+] soit [H3O+] = 10 -pH [H3O+] = 10 -4,10 = 7,943.10 -5 M. La valeur de la concentration est: [H3O+] = 7,94.10 -5 mol.L-1 pH dans tout le domaine de mesure de pH. a) Quelle est en % l'erreur relative commise sur la dtermination du pH? b) Quelle est l'erreur systmatique commise dans la dtermination de la concentration en ions H 3 O de la solution, exprime en mol.L -1 et en pourcentage ?RPONSE QUESTION N¡ 3 :
est pH v = 4,00.LÕerreur relative s'crit: pH/pH
v = 0,10/4,00 = 2,5 % b) La concentration "vraie" a pour valeur: [H3O+]v = 10 -4.00 = 1,00.10 -4 mol.L -1 LÕerreur absolue en concentration s'crit: [H3O+] = (7,94 -10,00)10 -5 = - 2,06.10 -5 mol.L -1 LÕerreur systmatique s'crit: [H30+] / [H30+]v = - (2,06.10 -5 )/(1,00.10 -4 ) = - 20,6 %QUESTION N¡ 4 : Quelle(s) opration(s) faut-il faire pralablement l'utilisation et lors de
RPONSE QUESTION N¡ 4 :
est ncessaire de calibrer l'instrument, c'est--dire d'tablir la correspondance numrique entre
l'indication de pH et la diffrence de potentiel au moyen de solutions tampons dont le pH est exactement connu.Par ailleurs, la d.d.p entre les lectrodes tant fonction de la temprature de la solution,
temprature de la solution. [E3-2005N] EXERCICE N¡ 3 (40 points)NONC
Un mdi cament est administr un patie nt par perfu sion intrave ineuse la vitesse de 6
mg.min -1 durant 1 heure.Le tableau des concentrations plasmatiques (mg.L
-1 ) en fonction du temps est le suivant:Temps (min) 10 20 30 40 50 60
Concentrations plasmatiques mg.L
-14,6 7,0 8,4 9,2 10,4 10, 4
d'limination k.RPONSE QUESTION N¡ 1 :
Deux calculs sont possibles:
- Au cours d'une perfusion intraveineuse, les concentrations plasmatiques (C) voluent selon l'quation suivante:C = Css. (1 - e
-kt ) o Css est la concentration l'quilibre Ln (1 - C/Css) = - kt. On calcule donc (1 - C/Css) pour chaque temps (ainsi que le point correspondant au temps =0, pour lequel C = 0 mg/L que l'on reprsente sur le papier semi-logarithmique ( l'exception
des temps 50 et 60 min).Temps (min) 0 10 20 30 40 50 60
1 - C/Css 1 0,558 0,327 0,192 0,115 0 0
On observe (voir figure jointe) que tous les points (non nuls) sont aligns (ce qui justifie leLa pente de la droite est gale -k.
-k = (Ln 1 - Ln 0,1)/(0 - 43) k = 0,054 min -1 - Possibilit galement de dterminer graphiquement le temps de demi-vie : T 1/2 = 12,5 min soit k = Ln2/ T 1/2 = 0,055 min -1 QUESTION N¡ 2 : Calcul er la clairance d'limination pl asmatique et le volume de distribution plasmatique.RPONSE QUESTION N¡ 2 :
Css = Ro/CL o Ro est la vitesse de perfusion
Clairance d'limination plasmatique: CL = 6 mg/min /10,4 mg/L = 0,58 L/min k = CL/Vd Volume de distribution plasmatique: Vd = 0,58 L/min/0,055 min -1 = 10,6 L QUESTION N¡ 3 : Quelle est la dose de charge qui aurait permis, chez ce patient, d'obtenir immdiatement une concentration plasmatique de 20 mg.L-1 ?RPONSE QUESTION N¡ 3 :
Dose de charge: D = C x Vd avec C = 20 mg/L ==> D=212mg QUESTION N¡ 4 : Quell e sera it la vitesse de per fusion permettant de mainte nir cette concentration plasmatique de 20 mg.L -1RPONSE QUESTION N¡ 4 :
Vitesse de perfusion R
0 = Css x CL avec Css = 20 mg/L R 0 = 11,6 mg/minRo = 6 mg/min:
Ro = 6 mg/min => Css = 10,4 mg/L
Ro' =========> Css' = 20 mg/L
Ro' = (20/10,4) x 6 mg/min.
[E4-2005N] EXERCICE N¡ 4 (40 points)NONC
Pour l'tude d'une poudre A possdant une activit enzymatique, on en dissout 0,1 g dans une
Les mesures d'activit enzymatique s'effectuent dans les conditions conventionnelles fixes pour la dfinition de l'unit internationale (UI) sur une prise d'essai de 1 mL de solution B dilue dans 9 ml de solution de substrat (S). Ces conditions conventionnelles prcisent notamment que la concentration en substrat du milieu d'incubation est de 10 K m et le temps d'incubation est fix 10 min. Le graphique ci-dessous montre qu' la fin de cette incubation, la concentration en produit form dans le milieu est [P] = 10.10 -6 mol.L -1On donne le K
m de l'enzyme pour le substrat = 1.10 -3 mol.L -1QUESTION N¡ 1 : Calculer v
0 = activit enzymatique du milieu d'incubation dans des conditions de vitesse initiale.RPONSE QUESTION N¡ 1 :
V 0 = 10.10 -6 moI.L -1 /10 min = 1.10 -6 mol.min -1 .L -1 QUESTION N¡ 2 : En dduire la concentration catalytique de la poudre A.RPONSE QUESTION N¡ 2 :
Activit enzymatique de la poudre A = 500.10
-6 mol.min -1 .kg -1 dans les conditions conventionnelles.Concentration catalytique = 500 UI.kg
-1 ou 0,5 UI.g -1 QUESTION N¡ 3 : Calculer le pourcentage de substrat consomm la fin de l'incubation dcrite dans l'nonc.RPONSE QUESTION N¡ 3 :
d[P] = 10.10 -6 mol.L -1 = - d[S] -d[S]/ [S] = (10.10 -6 ) / (10.10 -3 ) = 1.10 -3 soit 0,1% QUESTION N¡ 4 : On prpare une solution C en dissolvant 0,3 g de poudre A dans une activit enzymatique du milieu d'incubation dans les conditions de vitesse initiale.RPONSE QUESTION N¡ 4 :
Vo x 3 => 3.10
-6 mol.min -1 .L -1Vo = f[E]
Si les conditions de Vo sont respectes, la Vo est fonction de [E]. [E5-2005N] EXERCICE N¡ 5 (40 points)NONC
On spare 2 composs A et B par chromatographie en phase gazeuse sur une colonne de 2,0 QUESTION N¡ 1 : Calculer la rsolution sachant que t RA = 300 secondes, t RB = 318 secondeset que les largeurs la base des pics, extrapoles par les tangentes aux points d'inflexion sont
respectivement de 20 secondes pour A et 21,2 secondes pour B. Qu'en pensez-vous? Justifier votre rponse.RPONSE QUESTION N¡ 1 :
Les largeurs des pics, extrapols par les tangentes aux points d'inflexion omgas: A =20s ; B =21,2s la rsolution R= 22BA RARB tt => R = (318-300)/(10+10,6) = 0,87 Les deux composs ne sont pas correctement spars. QUESTION N¡ 2 : Les coefficients de l'quation de Van Deemter sont dtermins :
A = 10
-3 cm B= 0,144 cm 2 .s -lC = 10
-3 S a) Quelle est la vitesse linaire moyenne de la phase mobile qui minimise la hauteur d'un plateau thorique? Dmontrer. b) Quel serait alors le nombre de plateaux thoriques de la colonne? c) En supposant que l'on donne la colonne son efficacit maximale, sans toucher aux temps de rtention, peut-on sparer correctement A de B?RPONSE QUESTION N¡ 2 :
H=A+B/"+C"
a) Pour tudier la valeur optimale de " (mu) pour laquelle H est minimal, il faut tudier la drive:H'= - B/"
2 +C pour "0 = #(B/C) la drive sÕannule, pour " < "0 , la drive est ngative, pour " > "0 , la drive est positive.H est minimal lorsque " = #(B/C) = #(0,144/10
-3 " optimale = 12 cm.s -1 b) H minimal = A + 2 #(BC) = 10 -3 + 2 # (1,44.10 -4H mini = 0,025 cm
Nombre de plateaux thoriques : N = L/H = 8000
c) t RBquotesdbs_dbs8.pdfusesText_14[PDF] exercices corriges sur electronique numerique
[PDF] exercices corriges sur electronique numerique pdf
[PDF] exercices corriges sur energie mecanique
[PDF] exercices corrigés sur excel 2010
[PDF] exercices corrigés sur l'amplificateur opérationnel pdf
[PDF] exercices corrigés sur lentropie et le second principe
[PDF] exercices corrigés sur l'inference statistique
[PDF] exercices corrigés sur l'oeil pdf
[PDF] exercices corrigés sur l'optique physique
[PDF] exercices corrigés sur la chromatographie pdf
[PDF] exercices corrigés sur la commande des machines électriques
[PDF] exercices corrigés sur la commande optimale
[PDF] exercices corrigés sur la configuration electronique
[PDF] exercices corrigés sur la diffraction
