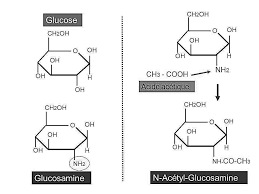
 Les glucides
Les glucides
Parmi les cétoses on retient : Le fructose : C6H12O6 : même formule brute que le glucose mais c'est un hexocétose et non pas un hexoaldose. C'est le sucre
 glucides.pdf
glucides.pdf
le fructose). Formules linéaires du glucose du galactose et du fructose. Page 3. 3. 1.2.1. Le glucose. De formule brute C6H12O6
 La consommation du fructose vers le syndrome métabolique
La consommation du fructose vers le syndrome métabolique
1 juin 2017 Le fructose ou sucre de fruit
 BACCALAURÉAT TECHNOLOGIQUE SCIENCES ET
BACCALAURÉAT TECHNOLOGIQUE SCIENCES ET
14 mars 2023 La concentration en masse totale de sucre dans ce jus est de 107 g·L–1. Les molécules de glucose et de fructose. Leur formule brute est ...
 Chapitre Chimie N° 3 Les glucides
Chapitre Chimie N° 3 Les glucides
Q3/Quelle est la formule brute de ces 3 molécules? Conclure. Ces 3 glucides Fructose... Aretenir ܀ •Les oses sont tous constitues de plusieurs fonctions ...
 Le 25-diméthylfurane : un carburant davenir ? (10 points)
Le 25-diméthylfurane : un carburant davenir ? (10 points)
fructose et du glucose tous deux de formule brute C6H12O6 s'écrit : 6 CO2 + 6 H2O → C6H12O6 + 6 O2. Cet exercice s'intéresse à une espèce chimique ...
 Sucroseglucose
Sucroseglucose
https://www.revmed.ch/view/495441/4091852/RMS_idPAS_D_ISBN_pu2012-09s_sa05_art05.pdf
 Correction Ex 1) Le sucre est un solide moléculaire constitué de
Correction Ex 1) Le sucre est un solide moléculaire constitué de
La formule brute du cholestérol est C27H46O. A quelle masse correspond 790 fructose
 BACCALAURÉAT TECHNOLOGIQUE SCIENCES ET
BACCALAURÉAT TECHNOLOGIQUE SCIENCES ET
20 juin 2017 Le glucose et le fructose ont les formules semi-développées suivantes : Glucose. Fructose. 1.1 Déterminer la formule brute de ces deux molécules ...
 glucides.pdf
glucides.pdf
Formules linéaires du glucose du galactose et du fructose De formule brute C6H12O6
 État des lieux
État des lieux
La consommation de fructose fait l'objet d'une controverse quant à ses effets sur la santé. Cette isomère du glucose (même formule brute mais structure.
 État des lieux
État des lieux
La consommation de fructose fait l'objet d'une controverse quant à ses effets sur la santé. Cette isomère du glucose (même formule brute mais structure.
 État des lieux
État des lieux
Formule brute : C6H12O6. - Famille des sucres ou glucides simples qui regroupe les monosaccharides (glucose
 LES GLUCIDES
LES GLUCIDES
On appelle isomères des composés qui ont la même formule brute mais des formules développées différentes. Formes pyraniques et furaniques du D-fructose.
 Untitled
Untitled
Un glucide a par formule brute: Cn Hy Oz. Un glucide possède. II. Chapitre Chimie N° 3. Les glucides. Exemples de glucides: Glucose Fructose
 La consommation du fructose vers le syndrome métabolique
La consommation du fructose vers le syndrome métabolique
1 juin 2017 Le fructose ou sucre de fruit
 1. BIOCHIMIE STRUCTURALE 1.3- LES GLUCIDES 1. Composition
1. BIOCHIMIE STRUCTURALE 1.3- LES GLUCIDES 1. Composition
Cette formule brute explique le terme utilisé en anglais d'hydrate de carbone. formé de ?-glucose et de ?-fructose liés en ? 1?2.
 CHAPITRE I : LES GLUCIDES
CHAPITRE I : LES GLUCIDES
La formule brute du Glucose fructose
 Correction Ex 1) Le sucre est un solide moléculaire constitué de
Correction Ex 1) Le sucre est un solide moléculaire constitué de
La formule brute du cholestérol est C27H46O. Ex 3) On veut préparer un sirop très léger de fructose (C6H12O6) qui est un sucre.
1. BIOCHIMIE STRUCTURALE
1.3- LES GLUCIDES
Groupe de composés aux fonctions très importantes :• Rôle énergétique : glucose (forme d'énergie di rectement utilisa ble par les cellules), amidon
(forme de stockage du glucose chez les végétaux), glycogène (forme de stockage du glucose chez les
animaux)...• Rôle structural : cellulose (constituant principal de la paroi des cellules végétales, polymère de
glucose), chitine (polymère de N-acétylglucosamine, carapace des arthropodes et paroi des mycètes)...
• Signau x de reconnaissanc e et de commu nication entre les cellules : glycoproté ines membranaires (exemple des antigènes des groupes sanguins A, B, O).1. Composition élémentaire
C, H, O
2. Fonctions chimiques
Groupe carbonyle : fonctions aldéhyde ou cétoneGroupe hydroxyle : fonction alcool
3. Classification des glucides
Également appelés monosaccharides ou sucres simplesNon hydrolysables
Molécules comportant de 3 à 7 atomes de carboneFormule brute : C
n H 2n O n : C n (H 2 O) n Cette formule brute explique le terme utilisé en anglais d'hydrate de carbone.Polyol qui porte au moins 2 fonctions alcools dont l'une au moins est une fonction alcool primaire, et une
groupement carbonyle réductrice, soit : • aldéhyde (-CHO) dans ce cas l'ose est un aldose. • cétone (>C=O) dans ce cas l'ose est un cétose. L'ose le plus répandu est un aldohexose en C6 : le glucose.Formule brute : C
6 H 12 O 6Glucides Non hydrolysables = oses = molécules de base Hydrolysables = osides Condensation d'un ou de plusieurs oses = holosides Condensation d'oses et de consti tuants non glucidiques = hétérosides
Cours biochimie BTS_ABM1 2019-2020 C. Larcher 1.3.1- Oses - Page 2 / 18 -1.3.1- LES OSES
1. Formule développée et isomérie ............................................................................................................... 3
1.1. Isomères de constitution (de fonction) ......................................................................................... 3
1.2. Stéréoisomères ............................................................................................................................. 3
1.2.1. Nombre de stéréoisomères ............................................................................................... 3
1.2.2. Représentation de Fischer ................................................................................................ 3
1.2.3. Diversité des stéréoisomères ............................................................................................ 4
1.2.4. Pouvoir rotatoire .............................................................................................................. 5
2. Structures cyclisées ................................................................................................................................... 6
2.1. Mise en évidence de l'existence de la structure cyclisée du glucose ........................................... 6
2.1.1. Réaction au réactif de Schiff ............................................................................................ 6
2.1.2. Réaction d'hémiacétalisation en présence d'un alcool .................................................... 6
2.1.3. Explication possible aux deux premières expériences ..................................................... 6
2.1.4. Phénomène de mutarotation ............................................................................................. 6
2.1.5. Conclusion ....................................................................................................................... 7
2.2. Représentation de Tollens ............................................................................................................ 7
2.3. Représentation de Haworth .......................................................................................................... 8
3. Propriétés des oses et du glucose .............................................................................................................. 9
3.1. Propriétés physiques ..................................................................................................................... 9
3.1.1. Propriétés optiques ........................................................................................................... 9
3.1.2. Propriétés polaires ............................................................................................................ 9
3.1.3. Thermodégradable ........................................................................................................... 9
3.1.4. Goût sucré ........................................................................................................................ 9
3.2. Propriétés chimiques .................................................................................................................. 10
3.2.1. Stabilité .......................................................................................................................... 10
3.2.2. Réactions d'oxydation des oses ..................................................................................... 10
3.2.3. Réaction de réduction des oses ...................................................................................... 12
3.2.4. Estérification .................................................................................................................. 13
3.2.5. Déshydratation à chaud .................................................................................................. 13
3.2.6. Épimérisation ................................................................................................................. 14
3.2.7. Interconversion des oses ................................................................................................ 14
4. Diversité des oses ................................................................................................................................... 14
4.1. Classification des oses ................................................................................................................ 14
4.1.1. En fonction du nombre de carbones .............................................................................. 14
4.1.2. En fonction de la nature de la fonction réductrice ......................................................... 14
4.1.3. Convention de numérotation .......................................................................................... 14
4.2. Principaux oses ........................................................................................................................... 15
4.2.1. D-ribose ......................................................................................................................... 15
4.2.2. Hexoses .......................................................................................................................... 15
4.3. Dérivés d'oses ............................................................................................................................ 16
4.3.1. Désoxyoses .................................................................................................................... 16
4.3.2. Acides (glyc)uroniques .................................................................................................. 16
4.3.3. (Glyc)osamines ou (hex)osamines : dérivés aminés d'oses ........................................... 16
4.3.4. Polyols ou glycitols : glycérol, sorbitol, xylitol ............................................................. 16
4.3.5. Dérivés autres : acide ascorbique ................................................................................... 16
Cours biochimie BTS_ABM1 2019-2020 C. Larcher 1.3.1- Oses - Page 3 / 18 -1. Formule développée et isomérie
1.1. Isomères de constitution (de fonction)
Des isomères de consti tution sont des molé cules de même formule brute ma is de formulesdéveloppées différentes. On distingue les isomères de chaîne, de position et de fonction.
Les isomères de fonction possèdent des groupes fonctionnels différents, donc des propriétés
physiques et chimiques différentes. Les oses les plus simples ont trois atomes de carbone : glycéraldéhyde et dihydroxyacétone • Aldose : glucide avec fonction aldéhydique en bout de chaîne (C1) • Cétose : glucide avec fonction cétone à l'intérieur de la chaîne (C2). D(+)-glycéraldéhyde L(-)-glycéraldéhyde Dihydroxyacétone Figure 1 : distinction entre un aldose et un cétose (exemple avec C3)On remarque que le C
2 du glyc éraldéhyde porte 4 substituants différent s Þ C as ymétrique Þpropriétés optiques (pouvoir rotatoire) : existence de 2 isomères optiques images l'un de l'autre dans un
miroir : on parle d'énantiomères (D-glycéraldéhyde et L-glycéraldéhyde).1.2. Stéréoisomères
1.2.1. Nombre de stéréoisomères
Le glucose a pour formule développée :
HOH 2 C - CHOH - C
HOH - C
HOH - C
HOH - CH = O
Il possède 4 carbones asymétriques (C
). Il existe donc 2 4 = 16 stéréoisomères différents.Les stéréoisomè res sont des isomères de configuration, c'est-à-dire des molé cules de
constitution identique mais dont l'organisation spatiale des atomes est différente.Pour visualiser les stéréoisomères, on utilise la représentation ou projection de Fischer.
Rappel : représentation de Cram
• C dans le plan de la feuille. • Liaison en pointillés : liaison dirigée vers l'arrière. • Liaison en trait épais : liaison dirigée vers l'avant.1.2.2. Représentation de Fischer
La projection de Fischer est surtout utilisée pour représenter les sucres et les acides aminés. Elle fut inventée par Emil Fischer. Passage de la représentation de Cram à la représentation de Fischer : • la chaîne carbonée est orientée avec son groupement le plus oxydé dirigé vers le haut • les traits verticaux symbolisent des liaisons dirigées vers l'arrière • les traits horizontaux symbolisent des liaisons dirigées vers l'avant C OH CHOH CH 2 OH CH 2 OH C CH 2 OH O C OH CH 2 OH OHH C OH CH 2 OH HHOEmil Fischer
1852-1919
Prix Nobel de
Chimie 1902
Cours biochimie BTS_ABM1 2019-2020 C. Larcher 1.3.1- Oses - Page 4 / 18 - On ne représente pas les atomes de carbone, ils sont situés à l'intersection des segmentshorizontaux et du trait vertical. La représentation de Fischer est souvent allégée en ne marquant la
position des groupements OH que par des tirets.Par convention, le D-glycéraldéhyde est l'énantiomère qui a le groupement OH positionné à
droite dans la représentation de Fischer. Cette représentation permet de différencier facilement les énantiomères chiraux 1L ou D.
Figure 2 : représentations de Cram et de Fischer du D-glucose On clas se les isomères de configurat ion en trois grands groupes : les énantiomères, les diastéréoisomères et les épimères.1.2.3. Diversité des stéréoisomères
a. Énantiomères Un énantiomère est un isomère de configuration non superposable à son homologue après symétrie dans un miroir.Tous les ose s possèdent un pouvoir rotatoire
2 du fai t de la présence d'un carbone asymétrique, les oses sont dits chiraux.Deux énantiomè res ont les mêmes propriétés physiques et chi miques à l'except ion
d'une seule : leur pouvoir rotatoire opposé. Dans la forme D, le groupement alcool (-OH) porté par le carbone n - 1 est à droite (en représentation de Fischer) comme le (+)-glycéraldéhyde. Dans la forme L, le groupement alcool (-OH) porté par le carbone n - 1 est à gauche (en représentation de Fischer) comme le (-)-glycéraldéhyde. Figure 3 : énantiomères du glucose ; forme D-glucose = forme naturelle.Les oses de la série D sont naturels.
Un méla nge équimolaire de 2 énanti omères est appelé mélange racém ique. Il se
caractérise par l'absence d'un pouvoir rotatoire car les effets d'un des énantiomères sur la
déviation du plan de la lumière polarisée sont annulés par ceux du second. 1 Molécule chirale : molécule qui ne peut pas se superposer à son image dans un miroir 2Pouvoir rotatoire : se dit du pouvoir qu'ont les substances asymétriques de faire tourner le plan de polarisation de la lumière.
Cours biochimie BTS_ABM1 2019-2020 C. Larcher 1.3.1- Oses - Page 5 / 18 - b. DiastéréoisomèresLes diastéréoisomères sont les stéréoisomères qui ne sont pas des énantiomères.
c. Epimères Deux épimères ne diffèrent entre eux que par la configuration absolue d'un seul carbone asymétrique, comme par exemple entre le D-mannose et le D-glucose ou encore entre leD-glucose et le D-galactose.
1.2.4. Pouvoir rotatoire
En soluti on, les formes énantiom ères d'une molécule portant un c arbone asymétriqueprésentent des propriétés optiques différentes. Chaque énantiomère dévie le plan de polarisation
d'une onde monochromatique polarisée (angle égal en valeur absolue mais de signe opposé).Cette propriété est caractérisée par le pouvoir rotatoire spécifique qui répond à la loi de Biot :
��� : angle de rotation observée en degré (°). : pouvoir rotatoire spécifique de la substance, constant pour une température et une longueur d'onde données (en °·g -1·dm
2 ℓ : longueur de la cellule contenant la substance, traversée par la lumière (en dm) ��� : concentration massique de la substance (en g·mL -1D-glucose L-glucose
ENANTIOMÈRES
Épimère (en C2) du D-glucose Épimère (en C4) du D-glucoseD-mannose D-galactose
DIASTEREOISOMERES
Figure 4 : illustration de la notion d'énantiomères, d'épimères et de diastéréoisomères
Voir planche filiation des oses
Remarque : en général, le suffixe des aldoses est " -ose » alors que celui des cétoses est " -ulose » (sauf exceptions : fructose,
sorbose,...). OH CH 2 OH OH CH 2 OH OH CH 2 OH OH CH 2 OH Cours biochimie BTS_ABM1 2019-2020 C. Larcher 1.3.1- Oses - Page 6 / 18 -2. Structures cyclisées
2.1. Mise en évidence de l'existence de la structure cyclisée du glucose
2.1.1. Réaction au réactif de Schiff
Le glucose possède une fonction aldéhydique. En présence du réactif de Schiff, on devrait
obtenir une coloration rouge que l'on n'obtient pas !2.1.2. Réaction d'hémiacétalisation en présence d'un alcool
Une molécule avec une fonction aldéhyde ou cétone est capable de réagir successivement avec deux molécules d'alcool (ici le méthanol) suivant les réactions suivantes :En présence d'HCl anhydre :
Aldéhyde + méthanol ® hémiacétal Hémiacétal + méthanol ® acétal + eau
R-CHO + CH
3OH ®
Aldéhyde + méthanol Hémiacétal
+ CH 3OH ®
+ H 2 OHémiacétal méthanol Acétal
Figure 5 : réaction d'hémiacétalisation entre un aldéhyde et un alcool Dans les mêmes conditions, le glucose ne réagit qu'avec une seule molécule de méthanol !2.1.3. Explication possible aux deux premières expériences
Dans le glucose, il s'est produit une réaction entre la fonction a ldéhydique et un desgroupements OH (= réaction d'hémiacétalisation intramoléculaire). Ceci expliquerait pourquoi le
glucose n'est pas capable de colorer le réactif de Schiff et pourquoi il ne peut réagir qu'avec une
seule molécule de méthanol (puisqu'il aurait déjà réagi avec une fonction alcool pour se retrouver
sous la forme d'un hémiacétal).2.1.4. Phénomène de mutarotation
La cristallisation du D-glucose dans des solvants différents (éthanol, pyrimidine) conduit nonpas à un seul produit mais à 2 produits dont les pouvoirs rotatoires sont différents. Ces 2 formes ont
été qualifiées de forme á (+ 112°), cristallisation dans l'éthanol (conditions !), et de forme â
(+ 19°), cristallisation dans la pyrimidine (conditions "). Ces deux formes sont dites anomères.
On observe pour chacune des formes mises en solution aqueuse, en fonction du temps, uneévolution du pouvoir rotatoire qui atteint pour chacune des formes la même valeur + 52,5°. Cette
valeur correspond à une proportion d'environ 1/3 de l'anomère a et 2/3 de l'anomère b. RC OH H OCH 3 RCquotesdbs_dbs1.pdfusesText_1[PDF] formule calcul mensualité emprunt excel
[PDF] formule calcul rapport de boite
[PDF] formule chimique du miel
[PDF] formule chute libre avec vitesse initiale
[PDF] formule dactualisation des prix
[PDF] formule d'actualisation des prix marchés publics
[PDF] formule d'ito exercices corrigés
[PDF] formule d'une force
[PDF] formule de calcul prescurtat clasa a 7
[PDF] formule de fabrication d'aliment de betail
[PDF] formule de la moyenne intégrale exercice
[PDF] formule de math 3eme
[PDF] formule de math 3eme pdf
[PDF] formule de peinture ? l'eau
