 THEME : REACTIONS CHIMIQUES TITRE DE LA LEÇON : LES
THEME : REACTIONS CHIMIQUES TITRE DE LA LEÇON : LES
2 Les alcanes. 2.1 Définition et Formule générale des alcanes. Un alcane est un hydrocarbure de formule générale CnH2n+2 où n désigne le nombre d'atomes de.
 T.P. cours Alcanes Alcools
T.P. cours Alcanes Alcools
- Reconnaître une chaîne carbonée linéaire ramifiée ou cyclique. - Nommer un alcane
 THEME: CHIMIE ORGANIQUE TITRE DE LA LEÇON
THEME: CHIMIE ORGANIQUE TITRE DE LA LEÇON
8 oct. 2022 Écris l'équation-bilan de la combustion complète des alcanes. 2. Déduis la formule brute de l'alcane A. 3. Donne les formules semi-développées ...
 ALCANES ET ALCOOLS
ALCANES ET ALCOOLS
➢ Sa formule brute devient CnH2n s'il est cyclique. n est le nombre d'atomes de carbone présents dans la molécule. Q8. Qu'appelle-t-
 Fiche pédagogique Domaine : Sciences Chimiques et Industries
Fiche pédagogique Domaine : Sciences Chimiques et Industries
La formule d'un alcane à n atomes de carbone est CnH2n+2. Par exemple le butane est un alcane avec la formule C4H10. Le schéma ci-dessous est celui du
 Les alcanes et les alcools
Les alcanes et les alcools
➔ animations : « 1S nomenclature alcane méthode » et « 1S nomenclature alcane animation ». ➔ pour s'entraîner en classe : formule semi- développée.
 Détermination des formules
Détermination des formules
On détermine la masse molaire et la formule générale ou la formule brute avec une 2) 25 l d'un simple alcane ont une masse de 6
 COURS DE CHIMIE ORGANIQUE Semestre 2 SVI
COURS DE CHIMIE ORGANIQUE Semestre 2 SVI
Les alcanes sont des hydrocarbures saturés de formule brute CnH2n+2. Le nom des alcanes se termine par le suffixe "ane". I-1- Alcanes à chaîne linéaire. Les
 Structure des identités chimiques Fiche
Structure des identités chimiques Fiche
Il n'y a pas de ramifications. • La formule brute d'un alcane non cyclique peut s'écrire C H . • Les six premiers alcanes portent des noms
 LES ALCANES
LES ALCANES
Les alcanes sont des hydrocarbures de formule brute CnH2n+2. Tous leurs atomes de carbone sont tétragonaux. Le méthane CH4 est le plus simple des alcanes.
 T.P. cours Alcanes Alcools
T.P. cours Alcanes Alcools
Les alcanes sont des hydrocarbures (constitués uniquement d'atomes de carbone et Cette molécule est un alcane car elle respecte la formule CnH2n+2.
 COURS DE CHIMIE ORGANIQUE Semestre 2 SVI
COURS DE CHIMIE ORGANIQUE Semestre 2 SVI
En chimie organique Il y a 4 façons de l'écriture des formules : - Formule brute
 INFO ALCANE UNE NOUVELLE FORMULE POUR UNE
INFO ALCANE UNE NOUVELLE FORMULE POUR UNE
en laboratoire. ALCANE. UNE NOUVELLE FORMULE. POUR UNE PERFORMANCE. ACCRUE. Dégraissant polyvalent surpuissant destiné à éliminer les salissures organiques.
 Fiche pédagogique Domaine : Sciences Chimiques et Industries
Fiche pédagogique Domaine : Sciences Chimiques et Industries
Une fiche de synthèse sur la formation des « alcanes » Par exemple le butane est un alcane avec la formule C4H10. Le.
 Questions à choix multiple (s) 1. Un alcane dont la formule brute est
Questions à choix multiple (s) 1. Un alcane dont la formule brute est
Un alcane dont la formule brute est C5H12 ayant la formule semi-développée suivante : a. La formule du radical R est : CH3.
 Détermination des formules
Détermination des formules
On détermine la masse molaire et la formule générale ou la formule brute avec une 2) 25 l d'un simple alcane ont une masse de 6
 LES ALCANES Exercice 1 (Monochloration du 2-méthylbutane) 1
LES ALCANES Exercice 1 (Monochloration du 2-méthylbutane) 1
Exercice 2 (Monochloration d'alcanes). 1. Détermination de la formule brute de ces trois alcanes. La formule générale d'un alcane est : CnH2n+2.
 ALCANES ET ALCOOLS
ALCANES ET ALCOOLS
Donner les formules brute et topologique du pentane. Chaîne ramifiée : Pour nommer l'alcane dont la formule semi-développée est : consulter le fichier 1S-
 NOMENCLATURE EN CHIMIE ORGANIQUE 1. Hydrocarbures (HC
NOMENCLATURE EN CHIMIE ORGANIQUE 1. Hydrocarbures (HC
Hydrocarbures (HC) saturés acycliques : les alcanes. Les hydrocarbures saturés ne sont Formule*. Préfixe : groupe secondaire. Suffixe : groupe principal.
 [PDF] TP cours Alcanes Alcools - Physique - Chimie
[PDF] TP cours Alcanes Alcools - Physique - Chimie
Alcanes Alcools Objectifs du TP: - Reconnaître une chaîne carbonée linéaire ramifiée ou cyclique - Nommer un alcane un alcool Ecrire leurs formules
 [PDF] Nomenclature en chimie organique - UniNE
[PDF] Nomenclature en chimie organique - UniNE
Hydrocarbures (HC) saturés acycliques : les alcanes Les hydrocarbures saturés ne sont Formule* Préfixe : groupe secondaire Suffixe : groupe principal
 [PDF] COURS DE CHIMIE ORGANIQUE Semestre 2 SVI
[PDF] COURS DE CHIMIE ORGANIQUE Semestre 2 SVI
Les alcanes sont des hydrocarbures saturés de formule brute CnH2n+2 Le nom des alcanes se termine par le suffixe "ane" I-1- Alcanes à chaîne linéaire Les
 [PDF] Chapitre 13 : De la structure aux propriétés des alcanes et des alcools
[PDF] Chapitre 13 : De la structure aux propriétés des alcanes et des alcools
II 1 Formule générale des alcanes Définition : Les alcanes sont des hydrocarbures saturés (donc formés à partir d'atomes de carbone et d'hydrogène
 [PDF] quelques proprietes des alcanes
[PDF] quelques proprietes des alcanes
1) Ouvrir le fichier Excel « alcanes xls » 2) Compléter les cases vides : noms nombres d'atomes de carbone formules état physique à 20°C masses
 [PDF] Chimie organique 1 (cours) Nomenclature des alcanes alcènes et
[PDF] Chimie organique 1 (cours) Nomenclature des alcanes alcènes et
La formule brute générale d'un alcane est de la forme CnH2n+2 Le nom des alcanes linéaires dépend de la longueur de la chaine carbonée :
 Chap 2 Les Alcanes PDF - Scribd
Chap 2 Les Alcanes PDF - Scribd
LES HYDROCARBURES SATURES · I- La chaîne carbonée des alcanes · 3- Les alcanes possédant quatre atomes de carbone : notion d'isomérie · Alcane Formule Formule
 [PDF] Propriétés physiques des alcanes et des alcools - Fiche professeur
[PDF] Propriétés physiques des alcanes et des alcools - Fiche professeur
Le décane est un alcane linéaire de formule brute C10H22 http://www olympiades-chimie fr/Concours 202010/Caen/XXVI-TPmarsCaen 202010 pdf
Quelle est la formule des alcane ?
Dénommés également paraffines, les alcanes sont des hydrocarbures acycliques saturés de formule générale CnH2n+2.Quels sont les 4 premiers alcanes ?
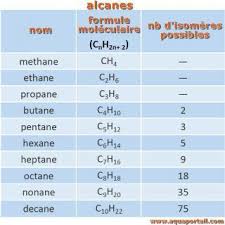
Les premiers alcanes sont le méthane (n = 1), l'éthane (n = 2), le propane (n = 3), le butane (n = 4), le pentane (n = 5) et l'hexane (n = 6).Quels sont les 12 premiers alcanes ?
Combustion: Halogénation: Pyrolyse et isomération:.Meth Eth Prop But Pent HexMethane. Ethane. Propane. Butane. Pentane. Hexane.
1EIE/TEIE
PASCAL ASMUSSEN LES ALCANES 1/5
LES ALCANES
1. Tétravalence du carbone
1.1. Rappel
L'atome de carbone a 6 électronsC12
6Modèle de Lewis : C
L'atome de carbone peut avoir 4 liaisons covalentes simplesLes atomes voisins forment alors un tétraèdre autour de l'atome de carbone qui est dit tétragonal.
1.2. Représentation perspective conventionnelle
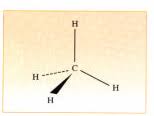
Dans la molécule de méthane CH
4, l'atome de
carbone est situé au centre d'un tétraèdre régulier.Pour représenter sur un plan une structure
tridimensionnelle, il faut utiliser des notations conventionnelles ayant une signification spatiale telles celles de la représentation perspective. C H PrivH Priv H PrivH PrivPar convention, on représente :
• par un trait plein (-) , les liaisons situées dans le plan de figure, la valeur de l'angle entre ces liaisons
étant respectée ;
• par un trait pointillé (----) ou par un triangle allongé hachuré ( ), une liaison dirigée vers
l'arrière du plan de figure ; • par un triangle allongé plein ( ), une liaison dirigée vers l'avant du plan de figure.1.3. Les hydrocarbures
Les hydrocarbures sont des composés organiques ne contenant que les éléments hydrogène et carbone.
Leur formule brute est C
xHy.2. Les alcanes
2.1. Définition
Les alcanes sont des hydrocarbures de formule brute C nH2n+2. Tous leurs atomes de carbone sont tétragonaux. Le méthane CH4 est le plus simple des alcanes.
2.2. L'éthane : la liaison simple C - C
L'éthane, de formule brute C
2H6, est un alcane. La structure de la molécule d'éthane fait apparaître
• une liaison covalente simple entre les atomes de carbone tétragonaux ; • des liaisons covalences simples entre les atomes de carbone et les atomes d'hydrogène.Formule semi-développée :
H3C¾CH3 ou CH3 ¾ CH3
Formule développée :
C H PrivH Priv HPrivC H
Priv H PrivH Priv1EIE/TEIE
PASCAL ASMUSSEN LES ALCANES 2/5 Le groupe- CH3 s'appelle un groupe méthyle.Les deux groupes méthyle - CH3 peuvent tourner l'un par rapport à l'autre, l'axe de rotation étant l'axe
de la liaison C - C. Nous obtenons ainsi une infinité de dispositions spatiales de la molécule d'éthane.
Le phénomène vu sur le modèle moléculaire correspond à la réalité : à température ordinaire, la molécule
d'éthane passe continuellement d'une disposition, ou conformation, à une autre. Ce résultat est général
Dans les hydrocarbures, il y a libre rotation autour des liaisons simples C - C.2.3. La chaîne carbonée des alcanes
Remplaçons l'un des atomes d'hydrogène du modèle moléculaire de l'éthane par un groupe méthyle - CH3 ;
nous obtenons ainsi celui de la molécule de propane C3H8. En répétant celte opération, nous construisons
une série de composés : les alcanes.Les alcanes sont des hydrocarbures à chaîne carbonée dite saturée : toutes les liaisons C - C sont simples.
Pour la formule brute C4H10 , deux possibilités apparaissent :• un alcane à chaîne carbonée non ramifiée, dite aussi chaîne linéaire : le butane
H3C ¾ CH2 ¾ CH2 ¾ CH3
• un alcane à chaîne carbonée ramifiée : le méthylpropaneCH3CH CH3
CH 3Ces deux alcanes ont même formule brute C4H10 , mais leurs structures sont différentes : ce sont des
isomères de constitution. Comme ils ne diffèrent que par l'enchaînement de leurs atomes de carbone,
cette isomérie de constitution est appelée isomérie de chaîne.Des isomères de constitution ont même formule brute, mais des formules développées différentes. Ils ont
des propriétés physiques et chimiques différentes. Voir ci-dessous. Formule brute noms des isomères température d'ébullition butane -0,5 C 4H10 méthylpropane -10 pentane 36 méthylbutane 25 C 5H12 diméthylpropane 92.4. Formules développées et semi-développées
La formule brute étant insuffisante pour représenter deux isomères de constitution, on est amené à
utiliser des formules plus précises.• Dans une formule développée, toutes les liaisons sont représentées par des tirets. Notons que cette
formule, dite plane, ne représente pas la disposition spatiale des atomes : elle indique simplement quels
sont les atomes directement liés les uns aux autres. Pour préciser la disposition spatiale des atomes, il faut
utiliser la représentation en perspective.1EIE/TEIE
PASCAL ASMUSSEN LES ALCANES 3/5 • Dans une formule semi-développée, seules les liaisons carbone-carbone sont représentées par un tiret,
simple ou double selon la nature de la liaison. Les liaisons carbone-hydrogène ne sont pas représentées,
mais les atomes d'hydrogène sont, dans la formule, directement accolés aux atomes auxquels ils sont liés
2.5. Nomenclature des alcanes
La nomenclature des composés chimiques obéit à des règles définies par l'Union Internationale de Chimie
Pure et Appliquée (U.IC.P.A.).
· Alcanes à chaîne carbonée non ramifiéeLes quatre premiers alcanes (1 < n < 4) portent des noms consacrés par l'usage : méthane, éthane, propane,
butane. Les noms des alcanes linéaires suivants (n > 5) sont constitués d'un préfixe qui indique le nombre
d'atomes de carbone de la chaîne (gent-, hex-, hept-, oct-...) suivi de la terminaison -ane caractéristique
des alcanes.· groupes alkyles non ramifiés :
En retirant un atome d'hydrogène à un atome de carbone terminal d'un alcane linéaire, on obtient un
groupe alkyle dont le nom s'obtient en remplaçant la terminaison -ane de l'alcane par la terminaison -yle.
Exemple : méthyle - CH3 ; éthyle - CH2 - CH3 ou - C2H5. en généralisant CnH2n+2 peut s'écrire CnH2n+1 - HGroupe alkyle symbolisé par R -
Exemple : Groupe méthyle - CH
3 ; Groupe éthyle - CH2 - CH3 ou - C2H5. Groupe propyle : - C3H7
Un alcane peut donc s'écrire R - H
· alcane à chaîne carbonée ramifiéeLa chaîne carbonée la plus longue est appelée chaîne principale. Son nombre d'atomes de carbone
détermine le nom de l'alcane. Afin de pouvoir situer les ramifications, on numérote la chaîne principale de
façon à ce que le numéro du premier atome de carbone portant une ramification soit le plus petit possible.
Le nom complet de l'alcane est constitué des noms des ramifications alkyles précédés de leur indice de
position et suivis du nom de l'alcane linéaire de même chaîne principale.Dans les noms composés, on élide le -e final des ramifications et, si plusieurs d'entre elles sont identiques,
leur nombre est indiqué à l'aide d'un préfixe di, tri, tétra...CH3CH2CHCH2CH3
CH2 CH CH3CH3654
3 2 16 atomes de carbone : hexane
2 ramifications : 1 groupe méthyle en 2ème position
1 groupe éthyle en 4ème position
Nom de l'alcane : 4-éthyl-2-méthylhexane
Autres exemples :
CH3CCHCH3
CH31432CH3
CH3CH3CH2CHCH2CH3
CH2CH3 CH3654321
CHCH2CH
CH3871EIE/TEIE
PASCAL ASMUSSEN LES ALCANES 4/5 3. Les réactions de combustions Lors d'une réaction de combustion, il y a destruction des liaisons C- H et C- C.3.1. Combustion complète
La combustion est complète lorsqu'on est en excès d'oxygène.Expérience : Combustion du méthane
Le trou à la base de la cheminée est entrouvert, la flamme comporte un cône bleu surmonté d'une zone pâle.Écrivons l'équation-bilan de réaction.
CH4 + 2 O2 ¾® CO2 + 2 H20
Conclusion : en présence d'un excès de dioxygène, la combustion du méthane est complète et donne de l'eau et du dioxyde de carbone. Alcane + dioxygène ¾® dioxyde de carbone + eau
La réaction est exothermique. On définit le pouvoir calorifique comme étant la quantité de chaleur dégagée
par la combustion de 1 m3 de gaz mesuré dans les conditions normales de température et de pression.
La quantité de chaleur dégagée est de l'ordre de 37 000 kJ/m3.Combustion explosive
Si l'on place exactement un volume de méthane et deux volumes de dioxygène, la réaction est explosive.
Ceci peut se produire dans les mines où il y a des poches de méthane, une étincelle suffit pour provoquer la
réaction : c'est le coup de grisou souvent meurtrier.Généralisation
Lors d'une réaction complète, nous pouvons écrire l'équation-bilan suivante C nH2n+2 + (3n + 1) 2 O2 ¾® n CO2 + (n + 1) H2O
Application : écrire la réaction de combustion complète du propane et du butane. H2O et CO2
1EIE/TEIE
PASCAL ASMUSSEN LES ALCANES 5/5 3.2. Combustion incomplèteExpérience :
Le trou à la base de la cheminée est bouché par la virole, la flamme est jaune et éclairante.Conclusion : en présence d'un défaut de dioxygène, la combustion du méthane est incomplète et donne de l'eau et du carbone. CH
4 + O2 ¾® C + 2 H20
Alcane + dioxygène ¾® carbone + eau
Equation générale :
C nH2n+2 + n+1 2 O2 ¾® n C + (n + 1) H2O
4. Les réactions de substitution
Elles consistent à remplacer un atome d'hydrogène dans la molécule 'un alcane par un autre atome ou par
un groupe d'atomes. Il y a rupture des liaisons C -H et remplacement progressif des atomes d'hydrogène par des atomes d'éléments halogènes : Chlore, Brome...Les dérivés halogènes des alcanes sont des produits de base de nombreuses synthèses, ce sont aussi de
bons solvants.Exemples :
(1) : CH4 + Cl2 ¾® CH3Cl + HCl chlorométhane (gaz)
(2) : CH3Cl + Cl2 ¾® CH2Cl2 + HCl dichlorométhane (gaz)
(3) : CH3Cl2 + Cl2 ¾® CHCl3 + HCl trichlorométhane ou chloroforme (liquide)
(4) : CHCl3 + Cl2 ¾® CCl4 + HCl tétrachlorométhane (liquide) tétrachlorure de carbone
(1) : Synthèse des caoutchoucs, résines..(3) et (4) : solvants, préparation des dérivés fluorés (les fréons), gaz propulseur, fluide caloporteur.
H2O et C
quotesdbs_dbs23.pdfusesText_29[PDF] alcane ramifié
[PDF] oxydation des alcools exercices corrigés
[PDF] taux de sulfate dans l'eau
[PDF] teneur en sulfate dans les sols
[PDF] écrouissage isotrope et cinématique
[PDF] écrouissage isotrope linéaire
[PDF] comportement non linéaire des matériaux
[PDF] la chine et l'afrique un nouveau partenariat pour le développement
[PDF] relation chine afrique
[PDF] la chine en afrique : enjeux et perspectives
[PDF] la chine populaire et l afrique
[PDF] la chine en afrique menace ou opportunité pour le développement
[PDF] présence chinoise en afrique
[PDF] commerce chine afrique