 LES ALCANES
LES ALCANES
Les hydrocarbures sont des composés organiques ne contenant que les éléments hydrogène et carbone. Leur formule brute est CxHy. 2. Les alcanes. 2.1. Définition.
 THEME : REACTIONS CHIMIQUES TITRE DE LA LEÇON : LES
THEME : REACTIONS CHIMIQUES TITRE DE LA LEÇON : LES
2 Les alcanes. 2.1 Définition et Formule générale des alcanes. Un alcane est un hydrocarbure de formule générale CnH2n+2 où n désigne le nombre d'atomes de.
 T.P. cours Alcanes Alcools
T.P. cours Alcanes Alcools
- Reconnaître une chaîne carbonée linéaire ramifiée ou cyclique. - Nommer un alcane
 THEME: CHIMIE ORGANIQUE TITRE DE LA LEÇON
THEME: CHIMIE ORGANIQUE TITRE DE LA LEÇON
8 oct. 2022 Écris l'équation-bilan de la combustion complète des alcanes. 2. Déduis la formule brute de l'alcane A. 3. Donne les formules semi-développées ...
 Fiche pédagogique Domaine : Sciences Chimiques et Industries
Fiche pédagogique Domaine : Sciences Chimiques et Industries
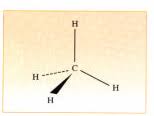
La formule d'un alcane à n atomes de carbone est CnH2n+2. Par exemple le butane est un alcane avec la formule C4H10. Le schéma ci-dessous est celui du
 Les alcanes et les alcools
Les alcanes et les alcools
➔ animations : « 1S nomenclature alcane méthode » et « 1S nomenclature alcane animation ». ➔ pour s'entraîner en classe : formule semi- développée.
 Détermination des formules
Détermination des formules
On détermine la masse molaire et la formule générale ou la formule brute avec une 2) 25 l d'un simple alcane ont une masse de 6
 COURS DE CHIMIE ORGANIQUE Semestre 2 SVI
COURS DE CHIMIE ORGANIQUE Semestre 2 SVI
Les alcanes sont des hydrocarbures saturés de formule brute CnH2n+2. Le nom des alcanes se termine par le suffixe "ane". I-1- Alcanes à chaîne linéaire. Les
 Structure des identités chimiques Fiche
Structure des identités chimiques Fiche
Il n'y a pas de ramifications. • La formule brute d'un alcane non cyclique peut s'écrire C H . • Les six premiers alcanes portent des noms
 LES ALCANES
LES ALCANES
Les alcanes sont des hydrocarbures de formule brute CnH2n+2. Tous leurs atomes de carbone sont tétragonaux. Le méthane CH4 est le plus simple des alcanes.
 T.P. cours Alcanes Alcools
T.P. cours Alcanes Alcools
Les alcanes sont des hydrocarbures (constitués uniquement d'atomes de carbone et Cette molécule est un alcane car elle respecte la formule CnH2n+2.
 COURS DE CHIMIE ORGANIQUE Semestre 2 SVI
COURS DE CHIMIE ORGANIQUE Semestre 2 SVI
En chimie organique Il y a 4 façons de l'écriture des formules : - Formule brute
 INFO ALCANE UNE NOUVELLE FORMULE POUR UNE
INFO ALCANE UNE NOUVELLE FORMULE POUR UNE
en laboratoire. ALCANE. UNE NOUVELLE FORMULE. POUR UNE PERFORMANCE. ACCRUE. Dégraissant polyvalent surpuissant destiné à éliminer les salissures organiques.
 Fiche pédagogique Domaine : Sciences Chimiques et Industries
Fiche pédagogique Domaine : Sciences Chimiques et Industries
Une fiche de synthèse sur la formation des « alcanes » Par exemple le butane est un alcane avec la formule C4H10. Le.
 Questions à choix multiple (s) 1. Un alcane dont la formule brute est
Questions à choix multiple (s) 1. Un alcane dont la formule brute est
Un alcane dont la formule brute est C5H12 ayant la formule semi-développée suivante : a. La formule du radical R est : CH3.
 Détermination des formules
Détermination des formules
On détermine la masse molaire et la formule générale ou la formule brute avec une 2) 25 l d'un simple alcane ont une masse de 6
 LES ALCANES Exercice 1 (Monochloration du 2-méthylbutane) 1
LES ALCANES Exercice 1 (Monochloration du 2-méthylbutane) 1
Exercice 2 (Monochloration d'alcanes). 1. Détermination de la formule brute de ces trois alcanes. La formule générale d'un alcane est : CnH2n+2.
 ALCANES ET ALCOOLS
ALCANES ET ALCOOLS
Donner les formules brute et topologique du pentane. Chaîne ramifiée : Pour nommer l'alcane dont la formule semi-développée est : consulter le fichier 1S-
 NOMENCLATURE EN CHIMIE ORGANIQUE 1. Hydrocarbures (HC
NOMENCLATURE EN CHIMIE ORGANIQUE 1. Hydrocarbures (HC
Hydrocarbures (HC) saturés acycliques : les alcanes. Les hydrocarbures saturés ne sont Formule*. Préfixe : groupe secondaire. Suffixe : groupe principal.
 [PDF] TP cours Alcanes Alcools - Physique - Chimie
[PDF] TP cours Alcanes Alcools - Physique - Chimie
Alcanes Alcools Objectifs du TP: - Reconnaître une chaîne carbonée linéaire ramifiée ou cyclique - Nommer un alcane un alcool Ecrire leurs formules
 [PDF] Nomenclature en chimie organique - UniNE
[PDF] Nomenclature en chimie organique - UniNE
Hydrocarbures (HC) saturés acycliques : les alcanes Les hydrocarbures saturés ne sont Formule* Préfixe : groupe secondaire Suffixe : groupe principal
 [PDF] COURS DE CHIMIE ORGANIQUE Semestre 2 SVI
[PDF] COURS DE CHIMIE ORGANIQUE Semestre 2 SVI
Les alcanes sont des hydrocarbures saturés de formule brute CnH2n+2 Le nom des alcanes se termine par le suffixe "ane" I-1- Alcanes à chaîne linéaire Les
 [PDF] Chapitre 13 : De la structure aux propriétés des alcanes et des alcools
[PDF] Chapitre 13 : De la structure aux propriétés des alcanes et des alcools
II 1 Formule générale des alcanes Définition : Les alcanes sont des hydrocarbures saturés (donc formés à partir d'atomes de carbone et d'hydrogène
 [PDF] quelques proprietes des alcanes
[PDF] quelques proprietes des alcanes
1) Ouvrir le fichier Excel « alcanes xls » 2) Compléter les cases vides : noms nombres d'atomes de carbone formules état physique à 20°C masses
 [PDF] Chimie organique 1 (cours) Nomenclature des alcanes alcènes et
[PDF] Chimie organique 1 (cours) Nomenclature des alcanes alcènes et
La formule brute générale d'un alcane est de la forme CnH2n+2 Le nom des alcanes linéaires dépend de la longueur de la chaine carbonée :
 Chap 2 Les Alcanes PDF - Scribd
Chap 2 Les Alcanes PDF - Scribd
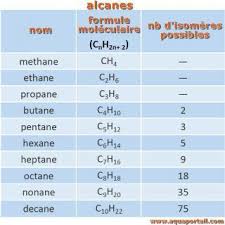
LES HYDROCARBURES SATURES · I- La chaîne carbonée des alcanes · 3- Les alcanes possédant quatre atomes de carbone : notion d'isomérie · Alcane Formule Formule
 [PDF] Propriétés physiques des alcanes et des alcools - Fiche professeur
[PDF] Propriétés physiques des alcanes et des alcools - Fiche professeur
Le décane est un alcane linéaire de formule brute C10H22 http://www olympiades-chimie fr/Concours 202010/Caen/XXVI-TPmarsCaen 202010 pdf
Quelle est la formule des alcane ?
Dénommés également paraffines, les alcanes sont des hydrocarbures acycliques saturés de formule générale CnH2n+2.Quels sont les 4 premiers alcanes ?
Les premiers alcanes sont le méthane (n = 1), l'éthane (n = 2), le propane (n = 3), le butane (n = 4), le pentane (n = 5) et l'hexane (n = 6).Quels sont les 12 premiers alcanes ?
Combustion: Halogénation: Pyrolyse et isomération:.Meth Eth Prop But Pent HexMethane. Ethane. Propane. Butane. Pentane. Hexane.

TPC8 p1
TPC8 1S
ALCANES ET ALCOOLS
Chapitre 14 page 236Les alcanes et les alcools sont des familles de molécules très utilisées dans la vie quotidienne.
I. Distillations :
1°) Exemple de distillation simple : La distillation du vin :
Introduire 50 mL de vin dans le ballon et quelques grains de pierre-ponce. Réaliser le montage ci-contre. Fixer la colonne de distillation avec son thermomètre. Mettre la température du chauffe-ballonà mi-course.
SAUTER UNE DEMI-PAGE pour répondre ultérieurement aux questions Q1. à Q6.Commencer le II, tout en surveillant l"évolution de la température et l"apparition des premières
gouttes de distillat.Q1. Après l"apparition des premières gouttes de distillat, noter la température lorsqu"elle est
stabilisée. Q2. Que peut-on dire de la température en tête de colonne pendant le changement d"état ? Q3. Décrire le distillat obtenu en le comparant au mélange initial : couleur, odeur. Q4. Comparer le degré alcoolique du vin et du distillat obtenu. - Pour le vin : regarder les indications fournies sur la bouteille. - Pour le distillat : Utiliser l"alcoomètre. Q5. Quel est l"intérêt de la distillation du vin ?Q6. Quel est le rôle de la pierre ponce ?
2°) Exemple de distillation fractionnée : La distillation du pétrole.
Voir feuille annexe à faire à la maison.
II. Les alcanes :
La structure des molécules respecte les règles de l"octet et du duet.Q7. Combien d"électrons célibataires possède un atome de carbone ? Combien de doublets
liants forme-t-il avec les atomes voisins ? (Rappel : numéro atomique du carbone Z =6.) Un alcane non-cyclique est un hydrocarbure de formule brute CnH2n+2. Sa formule brute devient CnH2n s"il est cyclique. n est le nombre d"atomes de carbone présents dans la molécule.Q8. Qu"appelle-t-on hydrocarbure ?
TPC8 p2
Le nom d"un alcane se forme à partir d"un préfixe, indiquant le nombre d"atomes de
carbone, et d"une terminaison -ane.Chaîne linéaire :
Nombre d"atomes
de carbone 1 2 3 4 5 6 7 8 Préfixe Méth- Éth- Prop- But- Pent- Hex- Hept- Oct- Q9. Donner les formules brute et développée du méthane. Q10. Donner les formules brute et semi-développée du propane. Q11. Donner les formules brute et topologique du pentane.Chaîne ramifiée :
Pour nommer l"alcane dont la formule semi-développée est : consulter le fichier 1S-Alcanes.swf. Q12. Nommer les alcanes suivants (virgule entre les nombres, tiret entre un nombre et un nom). CH 3 CH3 - CH2 - CH - CH2 - CH2 - CH3 CH3 - CH - CH - CH3
CH2 CH2
CH3 CH3
Q13. Représenter la formule semi-développée du 3-éthyl-3,4-diméthylhexane.Chaîne cyclique :
Le nom d"un alcane cyclique est déduit de l"alcane linéaire correspondant et précédé du préfixe
cyclo. Q14. Donner la formule topologique du cyclobutane.III. Les alcools :
Les formules des alcools dérivent de celles des alcanes en remplaçant un atome d"hydrogène H
par le groupe caractéristique hydroxyle -OH. Il existe donc des alcools linéaires, ramifiés ou
cycliques.Règles de nomenclature :
- Le suffixe devient anol (exemple : éthanol) - La chaîne la plus longue doit contenir le carbone sur lequel est fixé le groupe -OH- La position du groupe -OH est précisée par un nombre qui précède ol dans le suffixe. Il
doit être le plus petit possible.Exemple :
La chaîne carbonée possède 5 carbone, Le carbone fonctionnel est en position 2, La molécule est le pentan-2-ol.Q15. Nommer les alcools suivants :
CH3 - CH2 - CH - CH2 - CH2 - CH3 CH3 OH
OH CH
3 - CH - CH - CH3
Q16. Donner la formule semi-développée du 3,3-diméthylbutan-2-ol.CH3 - CH2 - CH2 - CH - CH3
OHCH3 - CH - CH2 -CH2 - CH3
CH2 - CH3
TPC8 p3
IV. Structure moléculaire et température de changement d"état :1°) Températures de changement d"état des alcanes :
Q17. Compléter les colonnes du tableau.
Alcane
linéaireFormule
brute qqqqéb (°C) qqqqfus (°C) État physique à25°C
Méthane - 161,7 - 182,5
Éthane - 88,6 - 183,3
Propane - 42,1 - 187,7
Butane - 0,5 - 138,3
Pentane 36,1 - 129,3
Hexane 68,7 - 94,0
Heptane 98,5 - 90
Octane 126 - 56,5
Nonane 150,5 - 54
Décane 173 - 30
Q18. À l"aide du logiciel Régressi, imprimer sur un même graphique les courbes donnant latempérature d"ébullition et la température de fusion en fonction du nombre d"atomes n de
carbone contenus dans la molécule. Aide : -Lettre grecque qqqq obtenue en appuyant simultanément sur CTRL + G puis taper q. -Identifier les courbes par un clic droit sur le graphique. Q19. Comment évoluent ces températures quand le nombre d"atomes de carbone augmente ?2°) Comparaison avec les alcools :
Alcools linéaires qqqqéb (°C) qqqqfus (°C) État physique à 25°CMéthanol 64,7 - 98
Ethanol 78,4 - 112
Propan-1-ol 97 - 126
Butan-1-ol 117 - 80
Pentan-1-ol 138 - 78
Hexan-1-ol 156 - 51,5
Heptan-1-ol 174 - 34,5
Octan-1-ol 194 - 16,5
Nonan-1-ol 213,5 - 5
Décan-1-ol 231 7
Q20. Comparer les températures de changement d"état des alcanes et des alcools ayant le
même nombre d"atomes de carbone. Q21. Comment expliquer cette différence en termes de liaisons intermoléculaires ?Q22. Quel est l"état physique de ces alcools à température ordinaire ? Compléter le tableau.
TPC8 p4
V. Miscibilité des alcools dans l"eau :
Des molécules miscibles forment un mélange homogène. Les molécules organiques qui contiennent des liaisons chimiques assez polarisées (H-O- ; H-N-ou H-F-) vont se lier entre elles et aux molécules d"eau grâce aux liaisons hydrogène : elles sont
hydrophiles. Les molécules organiques contenant de longues chaînes carbonées et des liaisons H-C- peupolarisées ne peuvent pas créer de liaisons hydrogène avec les molécules d"eau et les
molécules hydrophiles. Elles sont dites hydrophobes. Les molécules hydrophiles et les molécules hydrophobes ne sont pas miscibles entre elles. Plus la chaîne carbonée d"un alcool est courte et plus sa miscibilité avec l"eau augmente. Q23. Classer ces molécules par miscibilité dans l"eau croissante.Éthanol Butan-1-ol Propan-2-ol
TPC8TPC8 1S
ALCANES ET ALCOOLS
à faire à la maison
I. Distillations :
2°) Exemple de distillation fractionnée : La distillation du pétrole.
Document : La distillation fractionnée, première étape de la pétrochimie !" La pétrochimie est la chimie des dérivés du pétrole. Elle transforme les pétroles bruts
(mélanges complexes d"hydrocarbures, pour l"essentiel d"alcanes) en produits adaptés à la
demande des consommateurs. L"ensemble de toutes ces opérations industrielles constitue le raffinage du pétrole.La première opération de raffinage consiste à séparer ces hydrocarbures par une distillation
fractionnée.La séparation et la purification s"effectue dans une tour de distillation : les composés les plus
volatils étant recueillis en haut de la colonne. »Q24. De quoi est constitué le pétrole brut ? Est-il utilisable directement après son extraction ?
Q25. Le texte parle " de produits adaptés à la demande des consommateurs ». Citer quelques exemples de ces " produits » évoqués par le texte.Q26. Quelle est la première étape du raffinage du pétrole ? Quel est le rôle de cette étape ?
Q27. À partir du schéma ci-après, expliquer comment fonctionne une tour de distillation. TPC8TPC8 1S
ALCANES ET ALCOOLS
à faire à la maison
I. Distillations :
2°) Exemple de distillation fractionnée : La distillation du pétrole.
Document : La distillation fractionnée, première étape de la pétrochimie !" La pétrochimie est la chimie des dérivés du pétrole. Elle transforme les pétroles bruts
(mélanges complexes d"hydrocarbures, pour l"essentiel d"alcanes) en produits adaptés à la
demande des consommateurs. L"ensemble de toutes ces opérations industrielles constitue le raffinage du pétrole.La première opération de raffinage consiste à séparer ces hydrocarbures par une distillation
fractionnée.La séparation et la purification s"effectue dans une tour de distillation : les composés les plus
volatils étant recueillis en haut de la colonne. »Q24. De quoi est constitué le pétrole brut ? Est-il utilisable directement après son extraction ?
Q25. Le texte parle " de produits adaptés à la demande des consommateurs ». Citer quelques exemples de ces " produits » évoqués par le texte.Q26. Quelle est la première étape du raffinage du pétrole ? Quel est le rôle de cette étape ?
Q27. À partir du schéma ci-après, expliquer comment fonctionne une tour de distillation.quotesdbs_dbs30.pdfusesText_36[PDF] alcane ramifié
[PDF] oxydation des alcools exercices corrigés
[PDF] taux de sulfate dans l'eau
[PDF] teneur en sulfate dans les sols
[PDF] écrouissage isotrope et cinématique
[PDF] écrouissage isotrope linéaire
[PDF] comportement non linéaire des matériaux
[PDF] la chine et l'afrique un nouveau partenariat pour le développement
[PDF] relation chine afrique
[PDF] la chine en afrique : enjeux et perspectives
[PDF] la chine populaire et l afrique
[PDF] la chine en afrique menace ou opportunité pour le développement
[PDF] présence chinoise en afrique
[PDF] commerce chine afrique
