 EXERCICES INTERNAT 2007-2004
EXERCICES INTERNAT 2007-2004
Le coefficient de partage corrigé alpha α = P VBenzène /Veau => α = 3 On sépare 2 composés A et B par chromatographie en phase gazeuse sur une colonne de 20.
 Exercices de TD Chromatographie liquide et Gaz H dp * = 3
Exercices de TD Chromatographie liquide et Gaz H dp * = 3
Exercice 12- Chromatographie en phase gazeuse (CPG) - L'analyse de 2 composés 1 et 2 donne les résultats suivants sur une colonne A : t0 = 4
 Question 4: En chromatographie en phase gazeuse la phase
Question 4: En chromatographie en phase gazeuse la phase
termine en présence/absence de sel dans la phase mobile. Partie III: Exercices. Exercice 1: En chromatographie en phase gazeuse deux composes A et B ont des
 Module LCP3 : Méthodes danalyses Spectroscopiques et
Module LCP3 : Méthodes danalyses Spectroscopiques et
18 déc. 2003 On préfère avoir une valeur de k faible pour ne pas allonger les durées d'analyse. B - Chromatographie en phase gazeuse (CPG). 3 - Quels sont ...
 Untitled
Untitled
Justifier votre réponse. EXERCICE N° 4 (30 points). ÉNONCÉ. On soumet à la chromatographie en phase gazeuse les mélanges des tubes suivants : Tube. 1. 2. 3. 4.
 Exercices de cinétique chimique
Exercices de cinétique chimique
La chromatographie en phase gazeuse (CPV) permet de connaître à tout instant les concentrations en cyclohexène A et en chlorocyclohexane C et par
 Fiche TD 1 « Chromatographie » - CCM – Exclusion - CPG
Fiche TD 1 « Chromatographie » - CCM – Exclusion - CPG
4- Calculez les facteurs de sélectivité et de résolution. Exercice 2. L'analyse par chromatographie en phase gazeuse de deux composants A et B conduit à la.
 Untitled
Untitled
b) Calculer le K; de l'inhibiteur pour l'enzyme. EXERCICE N° 3 (30 points). ÉNONCÉ. On procède par chromatographie en phase gazeuse
 Exercices : corrigé
Exercices : corrigé
Exercices : corrigé. Exercice 8 : ordre d'une réaction. Par chromatographie en phase vapeur on étudie l'évolution du système siège de la réaction entre le
 CHROMATOGRAPHIE LIQUIDE - Académie des Sciences et Lettres
CHROMATOGRAPHIE LIQUIDE - Académie des Sciences et Lettres
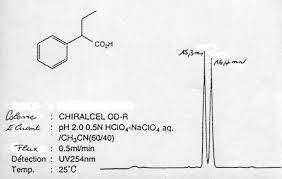
COMPARAISON AVEC LA CHROMATOGRAPHIE EN PHASE GAZEUSE. 20 % environ des Discuter. Corrigé n° 2. 1 ) La phase stationnaire est une phase chirale (par la ...
 Module LCP3 : Méthodes danalyses Spectroscopiques et
Module LCP3 : Méthodes danalyses Spectroscopiques et
18 déc. 2003 Chromatographiques. Examen de Chromatographie. CORRIGÉ. Aucun document n'est autorisé - Les ... A - Chromatographie en phase gazeuse (CPG).
 EXERCICES INTERNAT 2007-2004
EXERCICES INTERNAT 2007-2004
Le coefficient de partage corrigé alpha ? = P VBenzène /Veau => ? = 3. On sépare 2 composés A et B par chromatographie en phase gazeuse sur une colonne ...
 Question 4: En chromatographie en phase gazeuse la phase
Question 4: En chromatographie en phase gazeuse la phase
termine en présence/absence de sel dans la phase mobile. Partie III: Exercices. Exercice 1: En chromatographie en phase gazeuse deux composes A et B ont des
 Chromatographie en phase gaz
Chromatographie en phase gaz
séparer les solutés
 SENEPIXEL
SENEPIXEL
Cours et exercices corrigés graphique fera-t-on appel à la chromatographie en phase gazeuse ou à la chromatographie en phase liquide ?
 Untitled
Untitled
ÉPREUVE D'EXERCICES D'APPLICATION 1999. EXERCICE Nº 1 (20 points) On soumet à la chromatographie en phase gazeuse les mélanges des tubes suivants :.
 Untitled
Untitled
b) Calculer le K de l'inhibiteur pour l'enzyme. EXERCICE Nº 3 (30 points). ÉNONCÉ. On procède
 Techniques danalyses biologiques Travaux dirigés avec corrigés
Techniques danalyses biologiques Travaux dirigés avec corrigés
Justifier. Exercice 4. Deux espèces chimiques A et B sont séparées par chromatographie gazeuse isotherme
 Interpretation des spectres de masse en couplage GC-MS - cours et
Interpretation des spectres de masse en couplage GC-MS - cours et
Cours et exercices corrigés de masse en couplage avec la chromatographie en phase gazeuse ... gas chromatography : chromatographie en phase gazeuse.
 Untitled
Untitled
EXERCICE N° 5 (40 points). ÉNONCÉ. On sépare 2 composés A et B par chromatographie en phase gazeuse sur une colonne de 20 mètres.
 [DOC] TD Chromatographie en phase gazeuse L3 Chimie Physique
[DOC] TD Chromatographie en phase gazeuse L3 Chimie Physique
TD Chromatographie en phase gazeuse Exercice 1 Deux espèces chimiques A et B sont séparées par chromatographie gazeuse isotherme à l'aide d'une
 20 Exercices corrigés en Chromatographie - Bio faculté
20 Exercices corrigés en Chromatographie - Bio faculté
Vous trouverez des exercices en : La chromatographie en phase gazeuse; La chromatographie liquide; La chromatographie ionique; La chromatographie hplc
 [PDF] Question 4: En chromatographie en phase gazeuse la - helptudiant
[PDF] Question 4: En chromatographie en phase gazeuse la - helptudiant
Exercice 1: En chromatographie en phase gazeuse deux composes A et B ont des temps de rétention de 5 4 et 13 3 mn respectivement La largeur des pics
 Chromatographie - coursexercicesexamens - Univdocs
Chromatographie - coursexercicesexamens - Univdocs
cours et examens corrigesexercices corrigestravaux dirigés pdf resumedes Chromatographie en phase gazeuse autre cours Chromatographie en phase
 [PDF] EXERCICES INTERNAT 2007-2004 - Remedeorg
[PDF] EXERCICES INTERNAT 2007-2004 - Remedeorg
On sépare 2 composés A et B par chromatographie en phase gazeuse sur une colonne de 20 mètres QUESTION N° 1 : Calculer la résolution sachant que tRA = 300
 Examen corrige Chromatographie en phase gazeuse de la nicotine
Examen corrige Chromatographie en phase gazeuse de la nicotine
Exercice 1 : Chromatographie en phase gazeuse de la nicotine ( 195 points) Avec des QCM et des exercices corrigés issus pour la plupart d'
 Examen corrige Examen corrigé Chromatographie en HPLC pdf
Examen corrige Examen corrigé Chromatographie en HPLC pdf
Exercice 1 : a) Vous essayez de séparer une mélange inconnu par chromatographie en phase inverse avec un éluant 50 acetonitrile/ 50
 (PDF) Méthodes Séparatives LC HPLC CPG et EC Notes de Cours
(PDF) Méthodes Séparatives LC HPLC CPG et EC Notes de Cours
Chapitre II : chromatographie en phase gazeuse (CPG) Chapitre III : traite l?ectrophorèse capillaire (EC) Chaque chapitre est suivi d?un recueil d?exercices
 TD Chromatographie en phase gazeuse - Clicours
TD Chromatographie en phase gazeuse - Clicours
TD Chromatographie en phase gazeuse Exercice 1 Deux espèces chimiques A et B sont séparées par chromatographie gazeuse isotherme à l'aide d'une colonne
Cours et exercices corrigés
Stéphane Bouchonnet
Ingénieur de Recherche
École Polytechnique
Enseignant en chimie11, rue Lavoisier
75008 Paris
Du même auteur
La spectrométrie de masse en couplage avec la chromatographie en phase gazeuseS. Bouchonnet, Éditions Lavoisier, 2009
Chez le même éditeur
Cinétique et catalyse
Génie des procédés de l'École de Nancy G. Sacchi, M. Bouchy, J.-F. Foucaut, O. Zahraa, R. Fournet, 2 eédition, 2011
Chimie analytique et équilibres ioniques
J.-L. Burgot, 2
eédition, 2011
Méthodes instrumentales d'analyse chimique et applications : méthodes chromatographiques, électrophorèses, méthodes spectrales et thermiquesG. Burgot, J.-L. Burgot, 3
eédition, 2011
Labo-Stat - Guide de validation des méthodes d'analysesM. Feinberg, 2009
Cinétique hétérogène
M. Soustelle
Volume 1
: Modélisation des mécanismes, 2006Volume 2
: Mécanismes et lois cinétiques, 2006Volume 3
: Mécanismes et réactivité, 2006Volume 4
: Exercices et problèmes résolus, 2007Chimie analytique en solution - Principes et applications J.-L. Brisset, A. Addou, M. Draoui, D. Moussa, F. Abdelmalek, 2005
Toute reproduction ou représentation intégrale ou partielle, par quelque procédé que ce soit, des pages publiées
dans le présent ouvrage, faite sans autorisation de l'éditeur ou du Centre français d'exploitation du droit de copie
(20, rue des Grands Augustins - 75006 Paris), est illicite et constitue une contrefaçon. Seules sont autorisées, d'une
part, les reproductions réservées à l'usage privé du copiste et non destinées à une utilisation collective, d'autre part
les analyses et courtes citations justifiées dans le caractère scientifique ou d'information de l'oeuvre dans laquelle
elles sont incorporées (Loi du 1 er juillet 1992 - art. L. 122-4 et L. 122-5 et Code pénal art. 425).© 2012, Lavoisier SAS
ISBN : 978-2-7430-1452-0Direction éditoriale : Emmanuel Leclerc
Édition
: Céline PoiteauxFabrication
: Estelle PerezCouverture
: Isabelle GodenècheMise en pages
: Atelier SMB À ma famille, qui s'organise patiemment autour d'un papa qui consacre beaucoup de son temps à écrire et à dessiner des " ruches * Cycles aromatiques vus par les enfants.Abréviations
AE af finité électronique
AP a ffinité protonique CI c hemical ionization : ionisation chimique CID c ollision induced dissociation : dissociation induite par collision EA nergie d'activation ou electron affinity : affinité électronique EI e lectron ionization : ionisation électronique ou énergie d'ionisation ET tat de transition GC g as chromatography : chromatographie en phase gazeuse GC-MS g as chromatography - mass spectrometry : c hromatographie en phase gazeuse couplée à la spectrométrie de masse I e ffet inductif I : effet inductif donneur I : effet inductif attracteur ICR i onic cyclotronic resonance : résonance cyclotronique ionique LC-MS l iquid chromatography - mass spectrometry chromatographie en phase liquide couplée à la spectrométrie de masse M e ffet mésomère M : e ffet mésomère donneur M : e ffet mésomère attracteur McL réarrangement de McLafferty
MS ma ss spectrometry : spectrométrie de masse MS/MS s pectrométrie de masse en tandem PBDE polybromodiphényléther PCB p olychlorobenzène PI p otentiel d'ionisation PM p oids moléculaire RDA réaction de rétro Diels-Alder
RMN résonance magnétique nucléaire
TQ t riple quadripôle u.m.a. u nité de masse atomiqueTable des matières
Abréviations . .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. . V
Introduction . .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. . 1
Première partie
Mécanismes de formation et de fragmentation des ions en couplage GC-MSChapitre 1
Notions de chimie organique nécessaires à l'interprétation des spectres de masse1. . Généralités. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. . 7
2Électronégativité
7 2 1Définition. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .
7 2 2Électronégativité et liaisons chimiques
8 3 Ef fet inductif 9 3 1Définition. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .
9 3 2 Ef fets inductifs et spectrométrie de masse 10 4 Ef fet mésomère 11 4 1Exemples du benzène et du butadiène. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .
11 4 2Mésomérie et cations
12 4 3Mésomérie et anions. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .
14 4 4Mésomérie et radicaux. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .
14 5Potentiel d'ionisation
15 5 1Définition. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .
15 5 2Sites d'ionisation. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .
16 6Acidité, basicité, af
finité protonique et affinité électronique 17 6 1Acidité et basicité
17 VIII Interprétation des spectres de masse en couplage GC-MS6. .2. . Affinité protonique . .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. . 18
6 3 Af finité électronique 19 7Autres notions de thermochimie
20 7 1Thermochimie d'une fragmentation. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .
20 7 2Énergie interne
217 3
Règle d'Audier
-Stevenson 227 4
Stabilité des radicaux
247 5
Modélisation de spectres de masse
24Chapitre 2
Mécanismes de formation et de fragmentation des ions en spectrométrie de masse1. . Formation et fragmentation des ions en ionisation électronique. .. .. .. .. .. .. . 27
1 1 Formation des ions en ionisation électronique. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. . 271 2
Ruptures simples. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .
281 2 1
Rupture
Į . .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. . 28
1 2 2Rupture allylique
301 2 3
Rupture
ı . .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. . 32
quotesdbs_dbs13.pdfusesText_19[PDF] exercices corrigés chromatographie liquide
[PDF] sujet examen chromatographie
[PDF] exercice d application chromatographie
[PDF] compte rendu tp chromatographie sur couche mince
[PDF] tp chromatographie sur couche mince pdf
[PDF] tp n°4 chromatographie et identification corrigé
[PDF] tp chimie chromatographie corrigé
[PDF] tp chromatographie sur papier
[PDF] chromatographie sur papier tp corrigé
[PDF] chromatographie paprika et carotte
[PDF] comparer les colorants de la carotte et ceux du paprika
[PDF] peut on savoir si tous les colorants du paprika ont ete extraits
[PDF] espece colorée carotte
[PDF] exercice sur la chromatographie seconde
