 Examen Méthodes spectroscopiques 2
Examen Méthodes spectroscopiques 2
16 déc. 2010 Exercice 1 (3 pts – 10min). Il est possible de doser simultanément par spectroscopie UV-‐Visible le cobalt et le nickel dans une.
 Correction exercices sur UV-visible Exercices 7- 8- 9*- 25 -26* - 35 p
Correction exercices sur UV-visible Exercices 7- 8- 9*- 25 -26* - 35 p
Séquence III-3: UV-visible. Correction exercices sur UV-visible. Exercices 7- 8- 9*- 25 -26* - 35 p 104-115. Exercice 7-8 p140-105. Exercice 25 p105. Page 2
 EXERCICES DE REVISION : SPECTROMETRIE DABSORPTION
EXERCICES DE REVISION : SPECTROMETRIE DABSORPTION
EXERCICES DE REVISION : SPECTROMETRIE D'ABSORPTION UV VISIBLE
 République Algérienne Démocratique et Populaire Polycopié de
République Algérienne Démocratique et Populaire Polycopié de
Exercices. 37. Résumé des Transitions électroniques et données d'absorption. 42 Spectroscopie UV-Visible. Un schéma de principe d'un spectromètre typique est ...
 Corrigé EVAL1 2014-2015
Corrigé EVAL1 2014-2015
I- Quelles sont les trois règles de sélection en spectroscopie de vibration dans l'infrarouge ? Le spectre UV-visible de cette solution montre une bande à la ...
 Polycopies-En: Spectroscopie Optique et RMN
Polycopies-En: Spectroscopie Optique et RMN
Une série d'exercices corrigés est donnée à la fin de chaque chapitre. Le polycopié est composé de quatre chapitres : • Chapitre I : Rappel sur la structure de
 Chimie et développement durable Partie 1
Chimie et développement durable Partie 1
EXERCICES. Partie 2/ Synthèses chimiques. Fiche 10 : Spectroscopie UV-visible. Exercice 1. Doc 1 : courbe d'absorbance du diiode. Doc 2 : Dosage d'une solution
 EXERCICES ÉPREUVE CHIMIE 1
EXERCICES ÉPREUVE CHIMIE 1
Exercice n°2. L'étude spectroscopique UV-visible d'une solution contenant la molécule A conduit au spectre de la figure 1. La concentration molaire est c = 2
 3. Spectroscopie UV-Visible
3. Spectroscopie UV-Visible
Spectroscopie UV-Visible : Spectroscopie Justifier votre réponse en expliquant le déplacement vers les grandes longueurs d'onde des spectres. 3.4. Exercices ...
 Examen Méthodes spectroscopiques 2
Examen Méthodes spectroscopiques 2
16 déc. 2010 Exercice 2 (toutes les questions sont indépendantes) (5 pts – 30 min) ... En spectroscopie UV-?visible pour mesurer l'absorbance à 500 nm ...
 EXERCICES ÉPREUVE CHIMIE 1
EXERCICES ÉPREUVE CHIMIE 1
Exercice n°2. L'étude spectroscopique UV-visible d'une solution contenant la molécule A conduit au spectre de la figure 1. La concentration molaire est c
 République Algérienne Démocratique et Populaire Polycopié de
République Algérienne Démocratique et Populaire Polycopié de
Spectroscopie UV-Visible. 9. Spectre d'absorption UV-Visible. 11. 4.Transitions électroniques. 13. 4.1 Groupements chromophores. 14. 4.2 La conjugaison.
 EXERCICES DE REVISION : SPECTROMETRIE DABSORPTION
EXERCICES DE REVISION : SPECTROMETRIE DABSORPTION
Spectroscopie UV visible. • Spectroscopie IR. Exercice 1 (Spectre d'absorption du rouge Ponceau). Le rouge Ponceau 4R
 Méthodes danalyses Spectroscopiques
Méthodes danalyses Spectroscopiques
CHAPITRE I : Spectroscopie UV-Visible Corrigé des exercices . ... Une série d'exercices d'application plus un corrigé sont donnés à la fin de.
 TD Ultra-Violet et IR EST (SEMESTRE 2) Filière Génie Biologique
TD Ultra-Violet et IR EST (SEMESTRE 2) Filière Génie Biologique
EXERCICE 5 : On remplit une cuve de 2 mm avec une solution de benzène de concentration 10-5 mol. L-1 ; le spectre UV-Visible de cette solution montre une
 Chimie Analytique- 3ème Année -Département de Pharmacie
Chimie Analytique- 3ème Année -Département de Pharmacie
TD N° 7: Spectroscopie UV-Visible. EXERCICE 1 : Quelles sont toutes les transitions électroniques possibles pour les molécules suivantes :.
 chimie organique
chimie organique
QCM et exercices. 104. Corrigés. 107. Chapitre 6. Spectroscopies IR UV et RMN. 113. ? 1. Notions de spectroscopie. 113. ? 2. Spectroscopies UV-visible et
 Fiche professeur Lanalyse spectrale : spectroscopies IR et RMN
Fiche professeur Lanalyse spectrale : spectroscopies IR et RMN
La spectroscopie infrarouge : un moyen de déterminer les groupes caractéristiques d'une molécule Exploiter des spectres UV-visible. Spectres IR.
 EXERCICE RÉSOLU 2
EXERCICE RÉSOLU 2
Énoncé. On s'intéresse à la réaction des ions cuivrique Cu2+ en solution aqueuse basique (de pH contrôlé) avec une espèce anionique appelée EDTA et
 CHAP 04-ACT EXP Spectro UV-Visible CORRIGE - legtuxorg
CHAP 04-ACT EXP Spectro UV-Visible CORRIGE - legtuxorg
Vérifier par spectroscopie UV-Visible la nature des colorants présents dans un sirop de menthe Estimer la quantité de colorant bleu dans le sirop Matériel et solutions disponibles : Spectrophotomètre Visible (entre 450 et 750 nm) Béchers fioles et pipettes jaugées 2 fioles jaugées de 100 mL 2 fioles jaugées de 50 mL
 Chimie Chapitre 5 Terminale S ANALYSE SPECTRALE EN CHIMIE
Chimie Chapitre 5 Terminale S ANALYSE SPECTRALE EN CHIMIE
1) Faire un schéma de principe d’un spectrophotomètre UV-visible 2) Pourquoi a-t-on choisi de travailler à cette longueur d’onde ? 3) La loi de Beer-Lambert est-elle vérifiée ? 4) Déterminer le coefficient d’absorbance molaire dans ces conditions
 Corrigés exercices UV
Corrigés exercices UV
Thème 3 : Contrôle qualité Séquence III-3: UV-visible Exercice 35 : 1) A :C 2H 6N 2 B : C 7H 8N 2 C : C 12H 10N 2 2) Et 3) Couleur transmise Couleurs absorbées = Couleurs complémentaires de la couleur transmise Longueur d’onde correspondant au max d’absorbance molécules jaune bleu 450 nm A orangé Bleu roi 475 nm B rouge cyan 500 nm C
 spectrometrie absorption uv visible ir
spectrometrie absorption uv visible ir
Exercice 2 (Spectrophotométrie UV visible d’un complexe du cuivre) 1 Définir la transmittance d’un milieu absorbant et donner la relation liant l’absorbance A à la transmittance T 2 Le spectre d’absorption du complexe Cu(NiH 3)4 2+ est représenté ci-dessous Comment choisir la longueur d'onde de travail ? Justifier ce choix
 LPro Spectro 1011 - u-bourgognefr
LPro Spectro 1011 - u-bourgognefr
B En" spectroscopie" UVBvisible" pour" mesurer" l’absorbance" à 250 nm d’un" composé 3- Donner les qualités d’un solvant idéal en spetros opie UV
 Chimie Analytique 3ème Année -Département de Pharmacie
Chimie Analytique 3ème Année -Département de Pharmacie
Chimie Analytique- 3ème Année -Département de Pharmacie - Université Batna2 P r Maghchiche 1 TD N° 7: Spectroscopie UV -Visible EXERCICE 1 : Quelles sont toutes les transitions électroniques possibles pour les molécules suivantes : 1) Méthane ; 2) Ethanol ; 3) Phénol ; 4) Acétylène EXERCICE 2 : 1
 1- Qu'est-ce que la spectroscopie ? 2- Spectroscopie UV-Visible
1- Qu'est-ce que la spectroscopie ? 2- Spectroscopie UV-Visible
Le dosage par spectroscopie UV-visible suppose que les espèces mises en jeu sont colorées 1- A partir du spectre d'absorbtion définir graphiquement ? max 2- établir la courbe d'étalonnage à partir de solution colorées dont on connaît les concentrations
 Analyse spectrale Spectres IR - Labolycée
Analyse spectrale Spectres IR - Labolycée
Les spectroscopies IR (infrarouge) et de RMN (résonance magnétique nucléaire) en sont deux exemples 1 3 1 Donner l’origine des bandes d’absorption 1 et 2 du spectre infrarouge IR (document 1) en exploitant les données du document 2 Accès à la correction
 Spectroscopie Cours Et Exercices By J Michael Hollas
Spectroscopie Cours Et Exercices By J Michael Hollas
Exercices corrigs spectroscopie uv visible pdf Goulotte March 16th 2020 - I exercices SPECTROSCOPIE UV VISIBLE DENYSPierre Frédé rick Exercices spectroscopie et spectre UV visibleCorrigés Un spectre UV visible se décrit en indiquant les valeurs de la longueur Revoir le cours p 94 du livre fiche et faire les exercices corrigés 10 11
 Spectroscopie Cours Et Exercices - Paris Saint-Germain
Spectroscopie Cours Et Exercices - Paris Saint-Germain
Spectroscopie visible UV Chromatographie phase liquide et gazeus Corrigés des parcours en autonomie exercices n° 18 20 23 28 34 et 35''TS CHAPITRE 7 SPECTROSCOPIE UV VISIBLE IR RMN DU PROTON DECEMBER 18TH 2020 - TS INTERFéRENCES COURS PRéPARATION DU TP TS DIFFRACTION DES ONDES COURS PRéPARATION TP TS CHAPITRE 7 SPECTROSCOPIE UV VISIBLE IR
 Spectroscopie Cours Et Exercices By J Michael Hollas
Spectroscopie Cours Et Exercices By J Michael Hollas
Spectroscopie Cours Et Exercices By J Michael Hollas corrigs pdf chimie analytique LA SPECTROSCOPIE INFRAROUGE spectrometrie absorption uv visible ir Spectroscopie Cours et exercices Vegas PDF Free Td corrig Technique spectroscopie 5 EXERCICES CORRIGS SUR LA SPECTROSCOPIE INFRA ROUGE EN TERMINALE S EXERCICES Spectroscopie infra rouge
 Searches related to exercices corrigés spectroscopie uv visible pdf filetype:pdf
Searches related to exercices corrigés spectroscopie uv visible pdf filetype:pdf
Exercices corrigs spectroscopie uv visible pdf Goulotte Cet ouvrage présente les diverses techniques de spectroscopie disponibles aujourd'hui en fournissant les bases théoriques et en en exposant les applications notamment à la détermination des structures et à l'analyse chimique
Qu'est-ce que la spectroscopie UV visible?
- I – SPECTROSCOPIE U.V. VISIBLE. 1) Principe. ? En 1ère S, nous avons vu que les molécules organiques possédant au moins sept doubles liaisons conjuguées sont des espèces de la matière colorée, car elle absorbe des rayonnements dans le domaine du visible ( ? compris entre 400 et 800nm environ).
Qu'est-ce que la spectrophotométrie UV visible?
- La spectrophotométrie uv visible (spectroscopie d’absorption moleculaire) lorsqu’un faisceau lumineux monochromatique (une longueur d’onde fixe) de longueur l et intensité I0traverse une solution (exp bleu de méthylène + eau) les molécules dissoutes vont absorber une quantité de la lumière incidente
Comment fonctionne la spectroscopie d’absorption dans l’UV et le visible?
- • La spectroscopie d’absorption dans l’UV et le visible est une méthode très commune dans les laboratoires. • Elle est basée sur la propriété des molécules d’absorber des radiations lumineuses de longueur d’onde déterminée.
Quels sont les exercices de spectroscopie?
- Exercices spectroscopie Elucider un mécanisme réactionnel A l’obscurité et en présence d’inhibiteurs de radicaux, l’addition électrophile d’acide bromhydrique sur l’acroléine (prop-2-énal) conduit au composé A de formule brute C3H5BrO. Le spectre infra rouge de A présente une bande intense à 1740 cm-1 ; son spectre RMN est le suivant :
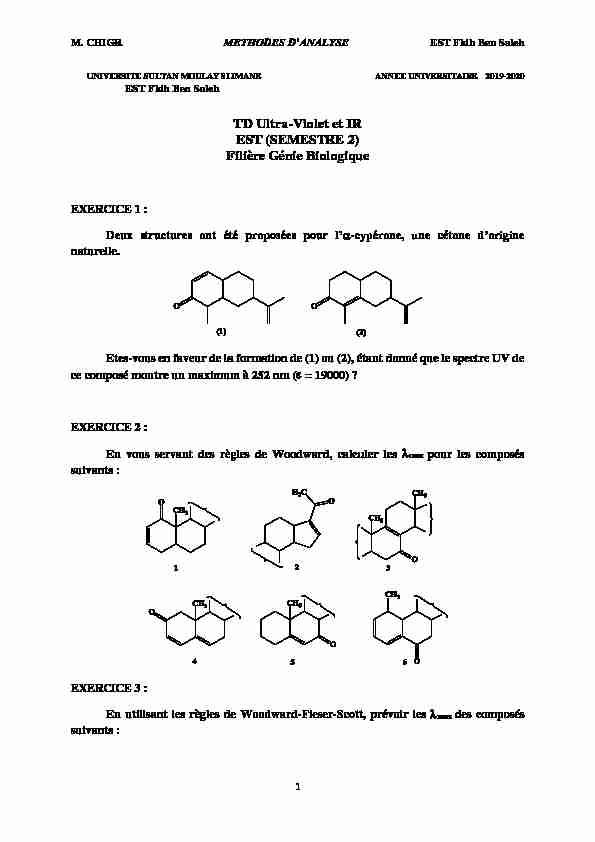 M. CHIGR EST Fkih Ben Saleh 1 UNIVERSITE SULTAN MOULAY SLIMANE ANNEE UNIVERSITAIRE 2019-2020
M. CHIGR EST Fkih Ben Saleh 1 UNIVERSITE SULTAN MOULAY SLIMANE ANNEE UNIVERSITAIRE 2019-2020 EST Fkih Ben Saleh
TD Ultra-Violet et IR
EST (SEMESTRE 2)
Filière Génie Biologique
EXERCICE 1 :
naturelle. Etes-vous en faveur de la formation de (1) ou (2), étant donné que le spectre UV de ce composé montre un maximum à 252 nm ( = 19000) ?EXERCICE 2 :
En vous servant des règles de Woodward, calculer les max pour les composés suivants :EXERCICE 3 :
En utilisant les règles de Woodward-Fieser-Scott, prévoir les max des composés suivants : M. CHIGR EST Fkih Ben Saleh 2EXERCICE 4 :
isomères : -ionone et -ionone. Les bandes observées sur les spectres UV-Visible de ces deux isomères correspondent à des transitions *.1) max
2) e. Justifier.
3) non polaire à un solvant polaire ? justifier.EXERCICE 5 :
On remplit une cuve de 2 mm avec une solution de benzène de concentration 10-5 mol. L-1 ; le spectre UV- de 256 nm. M. CHIGR EST Fkih Ben Saleh 3 1)2) tillon placé dans une cuve de 4
mm ?3) Quelle conclusion peut-on tirer de ces 2 expériences ?
EXERCICE 6 :
solaires pour ralentir leur dégradation (photolyse et réactions photochimiques). Quelle doit être la concentration en g.L-1 rayonnement soit absorbé sur une épaisseur de 0,3 mm ? Données : M = 500 g.mol-1 ; = 15 000 L.mol-1 .cm-1 pour max = 350 nm.EXERCICE 7 :
Une solution de permanganate de potassium (c = 1,28 . 10-4 mol.L-1) a une transmittance de 0,5 à 525 nm, si on utilise une cuve de 10 mm de parcours optique. a) b) Si on double la concentra nouvelle solution. Quelle conclusion peut-on tirer ?EXERCICE 8 :
90 %.EXERCICE 9 :
On veut doser un mélange de permanganate et de bichromate en exploitant en nm 266 288 320 350 360A permanaganate 0,042 0,082 0,168 0,125 0,056
A K2Cr2O7 0,410 0,283 0,158 0,318 0,181
A mélange 0,766 0,571 0,422 0,672 0,366
M. CHIGR EST Fkih Ben Saleh 4 La cuve utilisée a une épaisseur de 1 cm. C°1 = C°2 = 1.10-4 mol.L-1. a) Montrer que la relation ci-dessous est vérifiée ; C°1 et A°1 : Concentration et Absorbance de la solution de permanganate seule C°2 et A°2 : Concentration et Absorbance de la solution de bichromate de seule C1 et C2 : Concentration en permanganate et en bichromate du mélangeAm : Absorbance du mélange
b) Effectuer la régression linèaire ࢟ൌ ι en fonction de ࢞ൌι ι . En déduire les volumes de C1 et C2.EXERCICE 10 :
1) Une solution de concentration C = 1.10-5 mol. L-1 présente une absorbance de 0,02
de la molécule. est la concentration maximale que ? Commenter cette valeur.2) Le para-nitrophénol peut être dosé par la soude. Le spectre UV-Visible du para-
nitrophénol à différents pH est donné par la courbe suivante : ntifier les 2 formes du p-nitrophénol correspondantes.3) isobestique, les 2 éspèces ont le même coefficient
iso , on observe sur les différents spectres un point particulier appelé isobestique. Identifier ce point sur la figure. Justifier votre réponse. M. CHIGR EST Fkih Ben Saleh 5EXERCICE 11 :
= 580 nm la cuve a une épaisseur de 1,00 cm. On obtient les résultats suivants en fonction de la concentration massique des solutions. (g.l-1) 0,60.10-3 1,50.10-3 2,40.10-3 3,00.10-3 4,50.10-3 6,00.10-3A 0,075 0,250 0,420 0,515 0,775 1,040
Données : X : C25H30ClN3 M = 408,19 g.mol-1 1) mesures ? Pourquoi ?2) Montrer que la loi de beer-Lambert est vérifiée pour cette série de solutions.
3) ption molaire de X obtenue à partir de
cette série de mesures. 4) dans les mêmes conditions donne A = 0,531. Déterminer la concentration molaire C de cette solution. En déduire sa concentration massique.EXERCICE 12 :
Ci--Visible de la 1,2,4,5-tétrazine
dans 3 milieux différents. Identifier quel spectre est acquis dans quel milieu et expliquer pourquoi.EXERCICE 13 :
Le spectre UV--inflammatoire) de
concentration : 1.10-4 mol.L-1 a été éffectuée dans un tampon phosphate (tampon basique pH = 7,5). La cuve a une épaisseur de 11 mm. 1) ?2) max) pour une analyse quantitative ?
M. CHIGR EST Fkih Ben Saleh 63) max.
4) les concentrations limites utiles pour une analyse quantitative à max.5) Quels sont les facteurs qui peuvent affecter la linéarité de la relation de Beer-
Lambert ?
EXERCICE 14 :
On désire doser un principe actif Pa
par UV à 266 nm.La préparation de la solution mère Sm a été réalisée par extraction du principe actif sur 250 ml
de sirop. La totalité du principe actif recueilli est mise dans une fiole jaugée et ajustée avec le
solvant à 20 ml.Préparation de la solution fille : dans une fiole de 20 ml, on introduit 30 µl de la solution mère
fille est de 0,312.1) DETERMINATION DE LA CONCENTRATION DU Pa PAR ETALONNAGE :
Préparation de la gamme étalon : 1,25 g.mol-1, on prépare une gamme de cinq solutions diluées dans 5 fioles jaugées de 20 ml. Fiole Volume de solution du Pa de Référence en µl AbsorptionA 10 0,124
B 20 0,232
C 30 0,331
D 40 0,447
E 50 0,548
M. CHIGR EST Fkih Ben Saleh 7 Déterminer la concentration du Pa dans la solution mère puis dans le sirop.2) DETERMINATION DE LA CONCENTRATION DU Pa PAR MA METHODE DES
AJOUTS DOSES :
-1 et de la solution mère Sm à doser,5 solutions diluées sont préparées dans 5 fioles jaugées de 20 ml.
FioleVolume de solution du
Pa de Référence en µl
Volume de solution
mère Sm du Pa en µl Absorption0 50 0,508
5 50 0,562
10 50 0,618
15 50 0,670
20 50 0,728
Déterminer la concentration du Pa dans la solution mère puis dans le sirop. M. CHIGR EST Fkih Ben Saleh 8 UNIVERSITE SULTAN MOULAY SLIMANE ANNEE UNIVERSITAIRE 2019-2020EST Fkih Ben Saleh
TD Ultra-Violet et IR
EST (SEMESTRE 2)
Filière Génie Biologique
EXERCICE 1 :
Les spectres IR ci-
Attribuer à chaque spectre le type de composé correspondant.EXERCICE 2 :
Ci- Le solvant choisi est un solvant aprotique comme CCl4. M. CHIGR EST Fkih Ben Saleh 91) Commenter les spectres.
2) - ?
EXERCICE 3 :
M. CHIGR EST Fkih Ben Saleh 10EXERCICE 4 :
Un laboratin maldroit a mélangé les cinq étiquettes de cinq flacons de produits. Il effectue une analyse IR et il doit remettre les étiquettes en place.Solution 1 : hexane
Solution 2 : hexanal
Solution 3 : hexanol
Solution 4 : acide hexanoique
Solution 5
M. CHIGR EST Fkih Ben Saleh 11EXERCICE 5 :
reproduits ci-après.1) Donner jes formules des 3 composés.
2) Attribuer à chaque composé le spectre infrarouge corresponadant en repérant la
(les) bandes(s) caractéristiques. Préciser pour chaque bande repérée de quelle(s)quotesdbs_dbs2.pdfusesText_2[PDF] exercices corrigés stabilité des systèmes asservis
[PDF] exercices corrigés statique du solide
[PDF] exercices corrigés structure des molécules 1ere s
[PDF] exercices corrigés structures de données langage c
[PDF] exercices corrigés suites 1ere es
[PDF] exercices corrigés suites 1ere s
[PDF] exercices corrigés suites arithmético géométriques terminale es
[PDF] exercices corrigés suites arithmétiques géométriques pdf
[PDF] exercices corrigés suites numériques bac pro pdf
[PDF] exercices corrigés suites terminale s pdf
[PDF] exercices corrigés sur fichierprogrammation c
[PDF] exercices corrigés sur l état de rapprochement bancaire pdf
[PDF] exercices corrigés sur l ordonnancement des processus
[PDF] exercices corrigés sur l'échantillonnage des signaux
