 Une réaction chimique : la combustion du méthane
Une réaction chimique : la combustion du méthane
Pour que le gaz méthane brûle il faut que des molécules de dioxygène et des molécules de Etude d'un autre exemple : la combustion incomplète du méthane.
 Chp 2 - La combustion
Chp 2 - La combustion
méthane + dioxygène ? eau + dioxyde de carbone réactifs produits. 2. Combustion incomplète. Lorsque la combustion est incomplète la flamme observée est
 La combustion du butane _Doc. professeur
La combustion du butane _Doc. professeur
Réaliser décrire et schématiser la combustion du butane et/ou du méthane dans l'air. Certaines combustions incomplètes peuvent être dangereuses.
 La combustion du méthane
La combustion du méthane
Du test de reconnaissance du dioxyde de carbone (l'eau de chaux se trouble). Un comburant est un corps chimique qui a pour propriété de permettre la combustion.
 Combustion de Combustibles
Combustion de Combustibles
(CO2) du méthane (CH4) et de l'oxyde nitreux (N2O). la combustion incomplète des hydrocarbures présents dans les combustibles. Les émissions de méthane ...
 On veut équilibrer léquation de la combustion complète du méthane
On veut équilibrer léquation de la combustion complète du méthane
On veut équilibrer l'équation de la combustion complète du méthane : méthane (CH4) + dioxygène (O2) ? dioxyde de carbone (CO2) + eau (H2O).
 Cours n°8 : La combustion du méthane et du butane
Cours n°8 : La combustion du méthane et du butane
Expérience de combustion incomplète. Fumées noires issues de la combustion incomplète du gaz du briquet. Flamme éclairante et qui dégage de la fumée.
 ACTIVITE N°5 combustion du methane
ACTIVITE N°5 combustion du methane
Que se passe-t-il lors de la combustion complète du butane ? 1. Mise en œuvre expérimentale. Nous allons dans cette activité faire bruler du butane (gaz
 LES ALCANES
LES ALCANES
flamme est jaune et éclairante. Conclusion : en présence d'un défaut de dioxygène la combustion du méthane est incomplète et donne de l'eau et du carbone.
 Objectifs: Noter sur le cahier de texte pour la séance prochaine Ex
Objectifs: Noter sur le cahier de texte pour la séance prochaine Ex
II) Bilan et équation-bilan de la combustion du butane et du méthane. A) Combustion complète du butane. 1) ( B.R ): On écrit en toutes lettres les réactifs
 Une réaction chimique : la combustion du méthane
Une réaction chimique : la combustion du méthane
Dans la réaction de combustion du méthane il y a toujours deux fois plus de molécules de dioxygène que de molécules de méthane Etude d’un autre exemple : la combustion incomplète du méthane On parle de combustion incomplète quand l’un des produits de la réaction pourrait encore brûler : c’est le cas
 Leçon n°7 : La combustion du méthane et du butane
Leçon n°7 : La combustion du méthane et du butane
dioxygène la combustion incomplète du méthane et du butane produit de l’eaudu noir de carbone du dioxyde de carbone et un gaz mortel le monoxyde de carbone (de formule chimique CO) La poudre de carbone (le noir de carbone) n’apas brûlé par manque de dioxygène Ces particules de carbone portées à incandescence (au rouge)
 14 Natural Gas Combustion - US Environmental Protection Agency
14 Natural Gas Combustion - US Environmental Protection Agency
Methane emissions are highest during low-temperature combustion or incomplete combustion such as the start-up or shut-down cycle for boilers Typically conditions that favor formation of N2O also favor emissions of methane 1 4 4 Controls410 NOx Controls - Currently the two most prevalent combustion control techniques used to reduce NOx
 GROUPE CONSULTATIF D’EXPERTS SUR LES OMMUNICATIONS - UNFCCC
GROUPE CONSULTATIF D’EXPERTS SUR LES OMMUNICATIONS - UNFCCC
combustion de combustibles en vue de produire de l’énergie (p ex de l’électricité et de la chaleur) Le secteur de l’énergie comprend deux activités principales liées à la combustion: 1) la combustion stationnaire et 2) la combustion liée aux transports ou combustion mobile
 Cours n 8 : La combustion du méthane et du butane
Cours n 8 : La combustion du méthane et du butane
Combustion incomplète Si l'air (le dioxygène) est en défaut (il n'y en a pas assez) la combustion est incomplète Il se forme du carbone et du monoxyde de carbone (ce gaz est toxique) ainsi que de l'eau La flamme est alors jaune et éclairante
 Searches related to combustion incomplète du méthane PDF
Searches related to combustion incomplète du méthane PDF
2) Explication de la combustion du méthane avec le modèle moléculaire: Comme pour la combustion du carbone construit les modèles moléculaires des réactifs de la combustion du méthane À partir de ces deux modèles moléculaires reconstruit les produits obtenus lors de la combustion du méthane
Quels sont les effets de la combustion incomplète du méthane et du butane?
Conclusion : Quand il n’y a pas assez de dioxygène, la combustion incomplète du méthane et du butane produit de l’eau,du noir de carbone, du dioxyde de carbone et un gaz mortel, le monoxyde de carbone (de formule chimique CO). La poudre de carbone (le noir de carbone) n’apas brûlé, par manque de dioxygène.
Comment fonctionne la réaction de combustion?
•Conclusion : La réaction de combustion produit de la vapeur d’eau. Elle produit aussi du dioxyde de carbone. Résumons : Le méthane (ou le butane) réagit avec le dioxygène contenu dans l’air. Lorsqu’ily a assez de dioxygène, la combustion est complète (flamme bleue).
Quels sont les réactifs de la combustion du carbone dans le dioxygène ?
La combustion du carbone dans le dioxygène produit du dioxyde de carbone. Les réactifs de cette combustion sont le carbone et le dioxygène. Le produit est le dioxyde de carbone. Le bilan de cette combustion s’écrit : carbone + dioxygène ? dioxyde de carbone Il se traduit : le carbone réagit avec le dioxygène pour former du dioxyde de carbone
Quels sont les effets du dioxygène sur la combustion?
Si la quantité de dioxygène est insuffisante, la combustion devient incomplète et produit du monoxyde de carbone. ?Le monoxyde de carbone est un gaz incolore et inodore. Il se fixe sur les globules rouges et empêche le dioxygène que nous avons inspiré d’être délivré à nos cellules.
 Groupe Collège 2009 Ȃ 2010 Académie de Créteil Page 1
Groupe Collège 2009 Ȃ 2010 Académie de Créteil Page 1 La combustion du méthane
Je me souviens
Le réactif
Le produit
Les formules du dioxygène : O2 , dioxyde de carbone : CO2, eau : H2O et méthane : CH4. Une transformation chimique peut être traduite par une équation de réaction où apparaissent réactifs et produits.Du test de reconnaissance du dio
Un comburant est un corps chimique qui a pour propriété de permettre la combustion d'un combustible. Le principal comburant est le dioxygène.Je m'informe
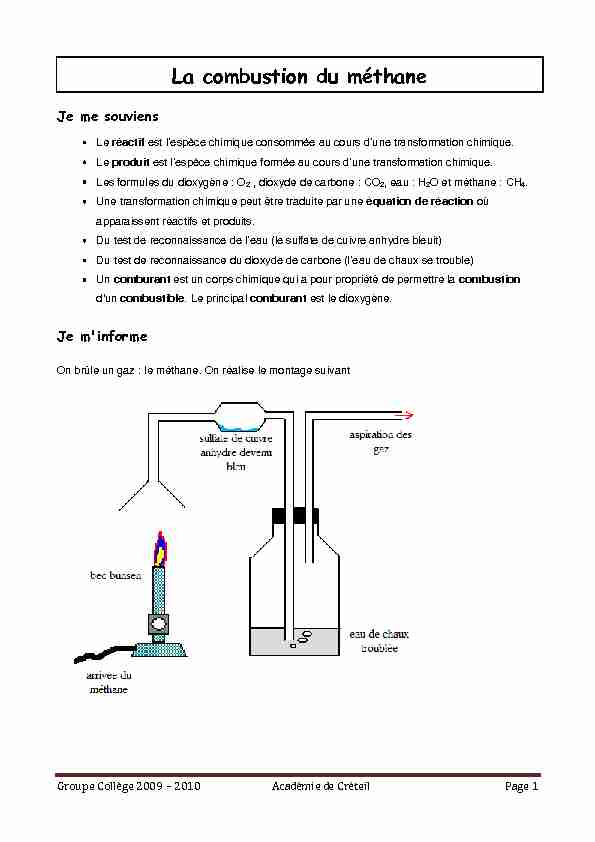
On brûle un gaz : le méthane. On réalise le montage suivant Groupe Collège 2009 Ȃ 2010 Académie de Créteil Page 2Je réponds aux questions
1. Dans cette combustion, quel est le combustible ?
2. Dans cette combustion, quel est le comburant ?
3. ? cette question utiliser les mots ou groupe de mots5. Compléter :
Les réactifs sont le _______________ et le ___________________Les produits sont
6. Compléter en toutes lettres:
________________ + ________________ AE ___________ __ _________ + _______7. Consulter votre livre ou le site http://rihetperez.free.fr/dmenu4.html puis compléter le
tableau ci-dessous en représentant les atomes de carbone C, H et O avec le modèle moléculaire (sphères colorées) correspondant:Atome Modèle Atome Modèle Atome Modèle
C H O Faire de même pour les molécules de dioxygène O2, de dioxyde de carbone CO2,H2O et de méthane CH4.
Molécule Modèle Molécule Modèle Molécule Modèle Molécule ModèleO2 CO2 H2O CH4
Groupe Collège 2009 Ȃ 2010 Académie de Créteil Page 3 Lavoisier a dit " Rien ne se perd, rien ne se crée, tout se transforme8. Ecrire le bilan avec les modèles moléculaires (question 8) en respectant la conservation
des atomes. + """"B AE """"B Ą """"B """"B9. Combien faut-il de molécules de dioxygène
méthane?10. Combien faut-il de moléc
méthane?11. Ajuster chimique de la combustion du méthane en complétant les pointillés par
le nombre correct.CH4 + "" O2 AE CO2 Ą ""H2O
Je vérifie
1. Le combustible est le méthane.
2. Le co
3. 4.5. Les réactifs sont le méthane et le dioxygène
Les6. méthane + dioxygène AE dioxyde de carbone + eau
7. Modèle moléculaire de quelques atomes :
Atome Modèle Atome Modèle Atome Modèle
C H O
Groupe Collège 2009 Ȃ 2010 Académie de Créteil Page 48. Modèle moléculaire de quelques molécules :
Molécule Modèle Molécule Modèle Molécule Modèle Molécule ModèleO2 CO2 H2O CH4
9. : + AE +Justification :
- Il y a un atome de carbone dans les réactifs, et un dans les produits. La conservation en atome de carbone est respectée. - le dioxyde de de dioxygène (2×2=4).10. Il faut donc 2 molécules de dioxygène
11.12. :
CH4 + 2 O2 AE CO2 + 2 H2O
Je retiens
Cette partie est à recopier / imprimer sur le cahier / classeurLorsque du méthane brûle, deux corps sont consommés : le méthane (combustible) et le
dioxygène (comburant). Deux corps nouveaux se forment : le dioxyde de carbone, mis en uivre anhydre. Les réactifs sont : le méthane et le dioxygène méthane + dioxygène AE dioxyde de carbone + eauCH4 + 2 O2 AE CO2 + 2 H2O
Groupe Collège 2009 Ȃ 2010 Académie de Créteil Page 5Je m'entraîne
Exercice 1 : Combustion du butane
1. utane.
2. Proposer une formule pour représenter la molécule de butane.
3. La combustion du butane donne les mêmes produits que la combustion du méthane. Quels
sont ces produits ? 4.5. Ecrire le bilan de la réaction en toute lettre.
6. chimique de cette réaction et
Exercice 2 : Combustion du butène
Soit la combustion du but-2-ène :
C4H8 + 6 O2 AE 4CO2 + 4 H2O
1. Quels sont les réactifs (noms) ?
2. Quels sont les produits (noms) ?
3. Combien y a-t-atomes de carbone dans les réactifs ydrogène ?
4. Combien y a-t-atomes de carbone dans les produits ? gène
5. Que constatez-vous ?
Groupe Collège 2009 Ȃ 2010 Académie de Créteil Page 6Correction
Exercice 1 : Combustion du butane
1. Le butane est composé de quatre atomes de carbone et de dix atomes d'hydrogène.
2. Formule: C4H10 .
3. Les produits sont l'eau et le dioxyde de carbone.
4. Test de reconnaissance de l'eau: le sulfate de cuivre anhydre bleuit.
Test de reconnaissance du dioxyde de carbone: L'eau de chaux se trouble.5. Butane + Dioxygène AE Eau + Dioxyde de carbone.
6. combustion du butane:
C5H10 + 8 O2 AE 5 CO2 + 6 H2O
Exercice 2 : Combustion du butène
1. Les réactifs sont le but-2-ène et le dioxygène.
2. Les produits sont l'eau et le dioxygène.
3. Il y a 4 atomes de carbone, 8 atomes d'hydrogène et 12 atomes d'oxygène dans
les réactifs.4. Il y a 4 atomes de carbone, 8 atomes d'hydrogène et 12 atomes d'oxygène dans
les produits.5. L'équation de réaction respecte la conservation des atomes.
quotesdbs_dbs29.pdfusesText_35[PDF] equation de combustion propane
[PDF] combustion complète de l'acétylène dans le dioxygène
[PDF] combustion ethane
[PDF] combustion de l'acétylène formule
[PDF] combustion incomplète des alcanes
[PDF] equation de combustion complete du glucose
[PDF] réaction exothermique
[PDF] réaction endothermique
[PDF] combustion du charbon dans l'air
[PDF] les combustions 4ème cours
[PDF] combustion du carbone définition
[PDF] identifier le dioxyde de carbone
[PDF] combustion de l'aluminium
[PDF] combustion du fer et du soufre
