 Chapitre sur « les combustions » (classe 4e)
Chapitre sur « les combustions » (classe 4e)
-Définition d'un produit : Corps formé au cours d'une transformation chimique b-Combustion combustible et comburant. -La combustion de la bougie nécessite
 CHP 4 : les combustions les combustions les combustions
CHP 4 : les combustions les combustions les combustions
Toutefois au cours de cette réaction chimique la masse n'a pas varié
 Chapitre 4 : Les combustions
Chapitre 4 : Les combustions
5- La combustion du carbone est une transformation chimique au cours de laquelle des réactifs disparaissent (le carbone et le dioxygène) et un produit apparaît
 Physique chimie 4eme Chapitre 2 Combustion
Physique chimie 4eme Chapitre 2 Combustion
11 mai 2005 Physique chimie 4eme. Chapitre 2 Combustion. Plan du cours: Introduction. Qu'est ce que brûler ? 1 – LA COMBUSTION DU CARBONE.
 Chapitre 4 - Atomes et transformations chimiques
Chapitre 4 - Atomes et transformations chimiques
microscopique au cours des combustions du carbone et du méthane. Fiche activité : interprétation de la combustion du carbone. On réalise la combustion du
 Plus de bonnes notes
Plus de bonnes notes
20 nov. 2019 Exercice 1 : questions de cours (4 pts). 1- Lors d'une réaction chimique comme une combustion qu'est-ce qu'un.
 Couverture Cours dété_sans devoirs_générique_18-séparées.indd
Couverture Cours dété_sans devoirs_générique_18-séparées.indd
4e. Physique. Chimie rédigé par des professeurs de l'Éducation Nationale. Reproduction interdite 6) Une combustion incomplète entraîne la production :.
 4ème Interrogation COMBUSTION 4ème Interrogation COMBUSTION
4ème Interrogation COMBUSTION 4ème Interrogation COMBUSTION
Exercice 1 Choisir le bon mot. Au cours de la combustion du carbone le carbone et le dioxygène sont les produits / réactifs et le dioxyde de carbone est le
 Chapitre 1 : Les combustions - LEtudiant
Chapitre 1 : Les combustions - LEtudiant
4) En résumé : ? Un combustible est une matière dont la combustion produit une quantité de chaleur utilisable. ? Le comburant est le deuxième « corps
 PHYSIQUE - CHIMIE 4e
PHYSIQUE - CHIMIE 4e
4e. Livret de cours. Rédaction. Muriel Couret. Anne Sontag. Julien Gomba. Relecture Exprime l'équation chimique de la combustion complète du méthane :.
 Chapitre sur « les combustions » (classe 4e - ac-guyanefr
Chapitre sur « les combustions » (classe 4e - ac-guyanefr
Chapitre sur « les combustions » (classe 4e) I- Une transformation chimique : la combustion a-Transformation chimique: Définition d’une transformation chimique : Au cours d’une transformation chimique des réactifs sont consommés et des produits nouveaux se forment REATIFS PRODUITS (la flèche signifie « donne »)
 CHP 4 les combustions - ac-versaillesfr
CHP 4 les combustions - ac-versaillesfr
Comme pour la combustion du carbone construit les modèles moléculaires des réactifs de la combustion du méthane À partir de ces deux modèles moléculaires reconstruit les produits obtenus lors de la combustion du méthane
 Leçon n°7 : La combustion du méthane et du butane
Leçon n°7 : La combustion du méthane et du butane
Le butane est le gaz contenu dans les briquets ou les camping-gaz L’unet l’autres’enflammentà la moindre étincelle : ce sont des gaz combustibles Leur combustion dégage beaucoup de chaleur Ne pas écrire mais bien lire : Comme la combustion du méthane est semblable à celle du butane les
Comment fonctionne la réaction de combustion?
•Conclusion : La réaction de combustion produit de la vapeur d’eau. Elle produit aussi du dioxyde de carbone. Résumons : Le méthane (ou le butane) réagit avec le dioxygène contenu dans l’air. Lorsqu’ily a assez de dioxygène, la combustion est complète (flamme bleue).
Qu'est-ce que la combustion ?
L’expérience dans laquelle une substance brûle est appelée combustion. • Le corps qui brûle est le combustible. • Le corps qui permet la combustion est le comburant. • les substances qui se forment sont les produits. Une combustion est une réaction chimique. On peut écrire le bilan de la réaction de combustion : II – La combustion du carbone.
Quels sont les produits de la combustion ?
Le butane et le dioxygène sont les réactifs. Le dioxyde de carbone et l’eau sont les produits. Remarque : On peut faire la combustion d’autres gaz tels que le méthane, le propane … etc. Les produits de tels combustions sont toujours les mêmes.
Comment fonctionne la combustion du carbone ?
La combustion du carbone produit de dioxyde de carbone. La combustion du méthane et/ou du butane produit de dioxyde de carbone et de l’eau. L’identification du dioxyde de carbone se fait à l’aide du test à l’eau de chaux et qu’il se forme un précipité blanc. Pour réaliser une combustion, il faut des réactifs : combustible et comburant
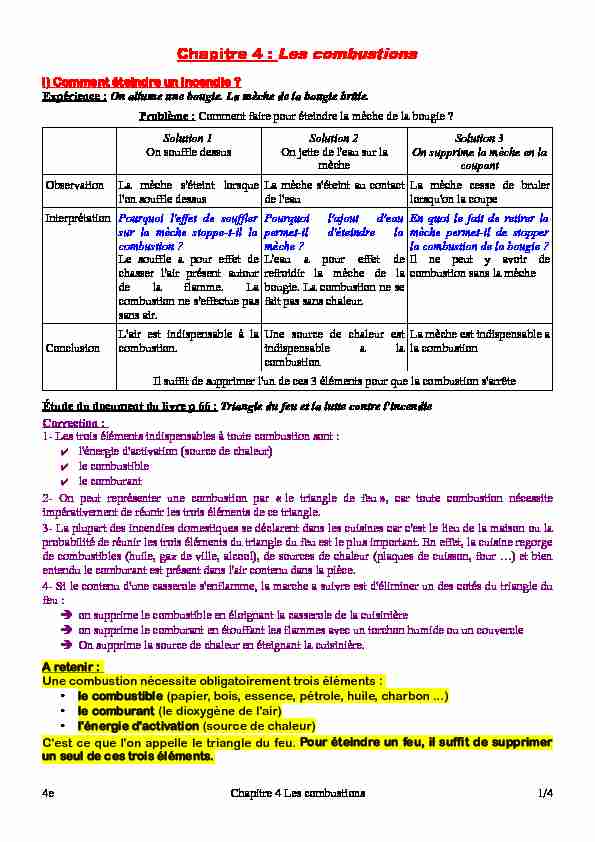 Chapitre 4 : Les combustionsI) Comment éteindre un incendie ? Expérience : On allume une bougie. La mèche de la bougie brûle. Problème : Comment faire pour éteindre la mèche de la bougie ?
Chapitre 4 : Les combustionsI) Comment éteindre un incendie ? Expérience : On allume une bougie. La mèche de la bougie brûle. Problème : Comment faire pour éteindre la mèche de la bougie ? Solution 1
On souffle dessusSolution 2
On jette de l'eau sur la
mècheSolution 3On supprime la mèche en la
coupantObservationLa mèche s'éteint lorsque
l'on souffle dessusLa mèche s'éteint au contact de l'eauLa mèche cesse de bruler lorsqu'on la coupeInterprétationPourquoi l'effet de souffler
sur la mèche stoppe-t-il la combustion ?Le souffle a pour effet de
chasser l'air présent autour de la flamme. La combustion ne s'effectue pas sans air.Pourquoi l'ajout d'eau permet-il d'éteindre la mèche ?L'eau a pour effet de
refroidir la mèche de la bougie. La combustion ne se fait pas sans chaleur.En quoi le fait de retirer la mèche permet-il de stopper la combustion de la bougie ?Il ne peut y avoir de
combustion sans la mècheConclusionL'air est indispensable à la
combustion.Une source de chaleur est indispensable a la combustionLa mèche est indispensable a la combustion Il suffit de supprimer l'un de ces 3 éléments pour que la combustion s'arrête Étude du document du livre p 66 : Triangle du feu et la lutte contre l'incendieCorrection :
1- Les trois éléments indispensables à toute combustion sont :
✔l'énergie d'activation (source de chaleur) ✔le combustible ✔le comburant2- On peut représenter une combustion par " le triangle de feu », car toute combustion nécessite
impérativement de réunir les trois éléments de ce triangle.3- La plupart des incendies domestiques se déclarent dans les cuisines car c'est le lieu de la maison ou la
probabilité de réunir les trois éléments du triangle du feu est le plus important. En effet, la cuisine regorge
de combustibles (huile, gaz de ville, alcool), de sources de chaleur (plaques de cuisson, four ...) et bien
entendu le comburant est présent dans l'air contenu dans la pièce.4- Si le contenu d'une casserole s'enflamme, la marche a suivre est d'éliminer un des cotés du triangle du
feu : ➔on supprime le combustible en éloignant la casserole de la cuisinière ➔on supprime le comburant en étouffant les flammes avec un torchon humide ou un couvercle ➔On supprime la source de chaleur en éteignant la cuisinière.A retenir :
Une combustion nécessite obligatoirement trois éléments : •le combustible (papier, bois, essence, pétrole, huile, charbon ...) •le comburant (le dioxygène de l'air) •l'énergie d'activation (source de chaleur) C'est ce que l'on appelle le triangle du feu. Pour éteindre un feu, il suffit de supprimer un seul de ces trois éléments.4eChapitre 4 Les combustions1/4
II) La combustion du carbone :
Voir la vidéo de l'expérience
Expérience : on réalise la combustion d'un morceau de fusain (carbone) dans le dioxygène.Exploitation de l'expérience : Activité 2 du livre p 59 Qu'est-ce qu'une transformation chimique ?
Correction :
1- Le volume du morceau de fusain diminue lors de la combustion. Le carbone disparaît donc au cours de
la combustion.2- La buchette incandescente plongée dans le flacon après la combustion s'éteint brutalement ce qui
prouve que le flacon ne contient plus de dioxygène après combustion.3- On appelle réactifs les corps qui disparaissent au cours de la combustion. Les réactifs de cette
combustion sont donc le carbone et le dioxygène.4- L'eau de chaux se trouble, ce qui indique la présence de dioxyde de carbone dans le flacon après la
combustion.5- La combustion du carbone est une transformation chimique au cours de laquelle des réactifs
disparaissent (le carbone et le dioxygène) et un produit apparaît (le dioxyde de carbone).A retenir :
Une combustion est une transformation chimique au cours de laquelle des réactifs disparaissent et des produits apparaissent. Ainsi la combustion du carbone est une transformation chimique dont le bilan s'écrit :RéactifsProduits
Carbone + dioxygèneDioxyde de carbone
Lorsqu'on lit ce bilan on comprend : " Le carbone réagit avec le dioxygène pour donner du dioxyde de
carbone »III) La combustion du butane :
Remarque : La combustion du butane (gaz contenu dans les briquets) est similaire a la combustion du méthane (gaz de ville) étudiée dans le livre activité 1 p 74.Voir la vidéo de l'expérience
Expérience :
4eChapitre 4 Les combustions2/4" Réagit avec »" Pour donner »
Tube à essais
Briquet ou réchaud à gaz
Observations :
Qu'observe-t-on sur les parois du tube à essai ? On observe l'apparition de buée, donc une formation d'eau sur les parois du tube à essais. Que se passe-t-il lorsque l'on ajoute de l'eau de chaux dans le tube à essais ? Lorsque l'on ajoute de l'eau de chaux dans le tube à essais, cette dernière se trouble. Interprétation : Quels sont les réactifs et les produits de la combustion du butane ?Les réactifs de la combustion du butane sont le butane (le combustible) et le dioxygène (le comburant).
Les produits de cette transformation sont le dioxyde de carbone et l'eau. Conclusion : écrire le bilan de cette transformation chimiqueLe bilan de la combustion du butane est :
Butane + dioxygèneeau + dioxyde de carbone
Remarque : de même pour la combustion du méthane on aMéthane + dioxygèneeau + dioxyde de carbone
IV) Le danger des combustions incomplètes :
Étude du document : article de Ouest France 5 intoxications au monoxyde de carboneCorrection :
1- Le malaise de la petite fille et de la voisine est dû à la présence dans l'air d'un gaz nocif : le monoxyde
de carbone.2- Ce taux élevé de monoxyde de carbone était dû à une combustion incomplète (à cause d'un manque de
dioxygène) de matière organique (ici vraisemblablement du méthane).3- L'hémoglobine est une protéine dont le rôle est de transporter le dioxygène dans le sang.
4- Le monoxyde de carbone se fixe sur l'hémoglobine du sang et prend la place du dioxygène. Le
dioxygène ne peut alors plus être transporté par le sang. C'est pour cette raison que même à très faible
concentration dans l'air, le monoxyde de carbone peut provoquer la mort. Quelques chiffres : 0,1% de monoxyde de carbone dans l'air tue en une heure.1% de monoxyde de carbone dans l'air tue en 15 minutes
10% de monoxyde de carbone dans l'air tue immédiatement.
De même, en cas d'intoxication au monoxyde de carbone, il est impératif de subir un traitement pour
l'éliminer du corps5- Le monoxyde de carbone est particulièrement dangereux, car étant incolore et inodore il est
indétectable par l'être humain. De plus lorsque les premiers symptômes apparaissent (maux de tête,
vomissement) il est bien souvent trop tard et une hospitalisation d'urgence est indispensable. Chaque année plus de 300 personnes décèdent d'un intoxication au monoxyde de carbone.6- Quelques précautions simples permettent de diminuer le risque d'intoxication au monoxyde de
carbone : •Ne jamais boucher les aérations et les ventilations à la maison•faire contrôler régulièrement (au moins une fois par an) et par un professionnel agréé les système
de chauffage (chaudière, cheminée ...)•Ne jamais utiliser de système de chauffage d'appoint à combustion (type poëlle ...) dans une pièce
mal ventilée ou trop petite. Et pour être vraiment à l'abri, faire installer un détecteur de monoxyde de carbone.7- Le seul traitement efficace contre les intoxications au monoxyde de carbone est l'hyperoxygénation.
Les victimes doivent être emmenées dans un caisson étanche hyperbare ou elles respirent du dioxygène
pur sous une pression de 3 bars, ce qui permet d'éliminer rapidement le monoxyde de carbone présent
dans le sang.4eChapitre 4 Les combustions3/4
A retenir :
Lorsque l'alimentation en dioxygène est insuffisante, une combustion est incomplète (elle produit un combustible : le carbone) et libère un gaz très toxique et indétectable par l'être humain : le monoxyde de carbone. Ce gaz tue plusieurs centaines de personnes par an en France.Le bilan d'une combustion incomplète est :
Combustible + dioxygènecarbone + monoxyde de carbone4eChapitre 4 Les combustions4/4
quotesdbs_dbs29.pdfusesText_35[PDF] identifier le dioxyde de carbone
[PDF] combustion de l'aluminium
[PDF] combustion du fer et du soufre
[PDF] oxyde magnétique de fer formule
[PDF] combustion du fer dans le dioxygène tableau d avancement
[PDF] combustion du fer wikipedia
[PDF] oxyde de fer fe2o3
[PDF] formule chimique de l'alumine
[PDF] combustion du zinc
[PDF] masse molaire co2
[PDF] combustion complète du butane
[PDF] combustion du soufre dans le dioxygène
[PDF] pouvoir comburivore d'un combustible pdf
[PDF] pouvoir comburivore definition
