 Les Sections du Module : Thermodynamique Chimique -SMC4 -
Les Sections du Module : Thermodynamique Chimique -SMC4 -
APOGEE. NOM. PRENOM. SEMESTRE. MODULE. SECTION. 18014638 AABAID. ABDELILAH. S4-SMC. Thermodynamique chimique. Section 1. 19010044 AACHAQ. AZIZA. S4-SMC.
 TD Thermodynamique Chimique (SMC S4)
TD Thermodynamique Chimique (SMC S4)
Chimie. TD Thermodynamique Chimique (SMC S4). Série N° 3. Exercice 1 : Un système homogène est formé de plusieurs constituants dont le nombre de moles du
 Solution - TD Série N°3
Solution - TD Série N°3
Filière SMC S4. Module : Thermodynamique Chimique. Solution - TD Série N°3. Pr Abdallaoui A. Exercice N° 1 -Diagramme de phase du benzène.
 Solution TD Série N°2 Exercice 1 : Cycle de Joule
Solution TD Série N°2 Exercice 1 : Cycle de Joule
Thermodynamique Chimique -Filière SMC S4. Pr Abdallaoui A. 1. Département de Chimie. Année universitaire 2020/2021. Filière SMC
 TD Série N°4
TD Série N°4
Département de Chimie. Année universitaire 2020/2021. Filière SMC S4. Module : Thermodynamique Chimique. TD Série N°4. Pr ABDALLAOUI A. Exercice N°1.
 dVPl dTC dU ) ( - + =
dVPl dTC dU ) ( - + =
Thermodynamique Chimique -Filière SMC S4. Pr Abdallaoui A. 1 çé. Département de Chimie. Année universitaire 2020/2021. Filière SMC
 Aucun titre de diapositive
Aucun titre de diapositive
FILIERE : SMC – Semestre 4. Module – M23. THERMODYNAMIQUE CHIMIQUE. Pr R. BCHITOU. DEPARTEMENT DE CHIMIE. FACULTE DES SCIENCES. UNIVERSITE MOHAMMED V RABAT
 CHAPITRE I : OBJET ET DEFINITION DE LA THERMODYNAMIQUE
CHAPITRE I : OBJET ET DEFINITION DE LA THERMODYNAMIQUE
I.9 Troisième loi de la thermodynamique - Entropie des corps purs à S4 SMC. II.1.7 Potentiel chimique d'un corps pur condensé ...
 Université Moulay Ismail
Université Moulay Ismail
Filière SMC S4 Rattrapage Thermodynamique Chimique ... Une machine thermique est un dispositif qui effectue des cycles thermodynamiques afin.
 ? ? ? ?
? ? ? ?
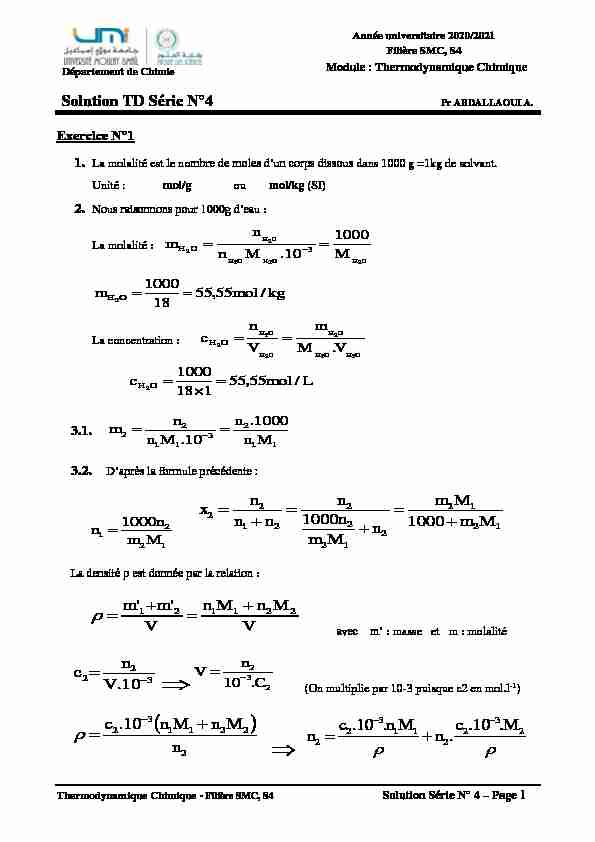
Filière SMC S4. Module : Thermodynamique Chimique. Solution TD Série N°4. Pr ABDALLAOUI A. Exercice N°1. 1. La molalité est le nombre de moles d'un corps
 Thermodynamique Chimique - Filière SMC, S4 Solution Série N° 4 Page 1
Thermodynamique Chimique - Filière SMC, S4 Solution Série N° 4 Page 1 Département de Chimie
Année universitaire 20/202
Filière SMC, S4
Module : Thermodynamique Chimique
Solution TD Série N°4 Pr ABDALLAOUI A.Exercice N°1
1. La molalité est le no dans 1000 g =1kg de solvant.
Unité : mol/g ou mol/kg (SI)
2. :La molalité :
OHOHOH
OH MMn nmOH 2222 2 1000
10.3 kgmolmOH/55,5518 1000
2
La concentration :
OHOH OH OH OH VM m V ncOH 222 2 2 2.
LmolcOH/55,55118
10002u 3.1. 11 2 3 11 2
21000.
10.Mn n Mn nm 3.2. : masse et m : molalité (On multiplie par 10-3 puisque c2 en mol.l-1) 12 2 11000Mm nn12 12 2 12 2 2 21
2
210001000Mm
Mm nMm n n nn nx V MnMn V mm221121'' U3 2 210.Vnc2 3 2 .10C nV 2 2211
3 210.
n MnMnc U 2 3 2 2 11 3 2
2.10...10.McnMncn
Thermodynamique Chimique - Filière SMC, S4 Solution Série N° 4 Page 2 2 3 2 11 3 2 2.10. .10. Mc Mncn U 223 112
2.10Mc
Mncn U22
3 12 1 2 .10Mc Mc n n U 12 223 2 1.10 Mc Mc n n U 1.101 12 22
3 2 1 Mc Mc n n 1.101 12 22
3 22
21
Mc Mc xn nn 1.10 1 12 22
32
Mc Mcx 1222
3 12
2.10McMc
Mcx U 21212
2.1000MMc
Mcx UExercice N°2
1) En utilisant la loi de Raoult, nous calculons les pressions partielles et la pression totale au-
dessus de la solution : mmHgPPPtoluènebenzènetotal4,2374,831542) En utilisant la loi de Henry
22KxP, et en supposant on en déduit : 2 2 2 2 22
2 2 CO OH OH CO COOH CO nM m n nn nx 2 2 2 2 2 CO OH OH CO nM m nKP u OH OH COM mn 2 2 2
Puisque
molM m OHOH55,5518
10002 2 U 11 3 22
3 2
2.10..10.1MncMcn
U2 3 2 11 3 22.10.1
.10. Mc Mncn Thermodynamique Chimique - Filière SMC, S4 Solution Série N° 4 Page 3 OH OH CO M m nKP 2 2 2 2 molKM Pmn OH OH CO 2 6210.38,310.25,118
7601000
2 2 2 u uLa solubilité du CO2
lmol/10.38,32Exercice 3
A) Calcul des nombres de moles :
molM mn OH OHOH72,918
1752 2 2 molM mn SONa SONa
SONa246,0142
3542
42
42
2SO4 solide, il y a
+ 42-, ainsi le nombre de moles de particules en solution est égal à trois fois le nombre de moles de soluté dissous : molnnSONasoluté738,0246,03342u u929,0738,072,9
72,92 2 2 solutéOH OH OHnn n On peut à présent utilisé la loi de Raoult pour caluler la pression de vapeur.
168,3929,022 qu OHOHsolutionPP
kPaPsolution94,2 Pbenzène = benzène Pobenzène Ptoluène = toluène Potoluène1 : Pbenzène = benzène Pobenzène = 0,500 x 12,7 kPa = 6,35 kPa
Ptoluène = toluène Potoluène = 0,500 x 3,79 kPa = 1,90 kPa Ptotale = Pbenzène + Ptoluène = 6,35 kPa + 1,90 kPa = 8,25 kPa2 : :
TAPP'A
T A AP P'F Donc,77,08,25
6,35' vapbenz F
et23,08,25
1,90'tolu vap F
- On remarque ici que la fraction molaire du liquide le plus volatil (benzène) est plus grande dans la phase vapeur (0,770) que dans la phase liquide (0,500). Thermodynamique Chimique - Filière SMC, S4 Solution Série N° 4 Page 4Exercice N°4
a. Voir courbe.2ème phase
3ème phase
c. se fait à température constante. d. e. Exercice N°5 - Diagramme binaire Eau Chlorure de Sodium1. cf. diagramme ci-dessous
10 3050
70
90
110
130
020406080100
Temps en min
Température en C
Température = f(temps)
P=1 barP=0,5 barP=0, bar
à P = 1 bar à P = 0,5 bar à P = 0,1 bar
100 °C 84 °C 56 °C
Thermodynamique Chimique - Filière SMC, S4 Solution Série N° 4 Page 5 2.3. Le point E correspond à la composition de leutectique. Le salage routier en le plus efficace
correspond à cette proportion : 23% en masse de NaCl dans le mélange eau-sel.En ce point, la saumure se transforme simultanément en 2 solides distincts : H2O(s) et
NaCl,2H2O(s).
Le calcul de la variance a pour but de déterminer le nombre de variables intensives, qui peuvent varier pour un système donné. v = (n-r) + 2 - ij Attention : P est Constante, donc : v = (n-r) + 1 - ijquotesdbs_dbs29.pdfusesText_35[PDF] La scintigraphie myocardique au Persantin ou Mibi Persantin
[PDF] Examens du Ministère 6e année - SOS étude
[PDF] Bilan Psychomoteur - Geopsy
[PDF] Annales de sujets d examen Volume 3 : Licence 2 - Ades Sorbonne
[PDF] Syllabus 2016 economie, vwo - Examenblad
[PDF] 1 Examen 2ième Session d 'Electronique Analogique ELE 004
[PDF] Travaux Dirigés, Électronique de puissance, Licence 3 - Chamilo
[PDF] dossier corrigé - Eduscol
[PDF] Electrostatique EXO Corriges
[PDF] Engels - vwo : vakspecifieke informatie centraal examen 2017
[PDF] Intrapreneuriat et entrepreneuriat organisationnel Examen de la
[PDF] DES EXAMENS ET CONCOURS INTERNES Filière permis de
[PDF] 1re secondaire - Collège Servite
[PDF] Technicien (ne) Supérieur (e) en Réseaux Informatiques et
