 TP Chimie n° 3
TP Chimie n° 3
TP Chimie n° 3. Dosage acido-basique en présence d'indicateurs colorés. (Dosage de l'acide acétique contenu dans le vinaigre). 1 Introduction. Le vinaigre de
 TRAVAUX PRATIQUES DE CHIMIE I
TRAVAUX PRATIQUES DE CHIMIE I
préparée par un dosage acido-basique. I. Objectifs ………………………………………………………………………………….. 15. II. Introduction ...…………………………………………………………………………….15. III. Principe du ...
 TP 3 Méthode de neutralisation (dosage acido-basique) Dosage de
TP 3 Méthode de neutralisation (dosage acido-basique) Dosage de
TP 3 Méthode de neutralisation (dosage acido-basique). Dosage de deux produits domestiques « le déboucheur et le vinaigre ». Introduction. Les acides et les
 1 TP Nº2 (Semestre 1) : Dosage dune base forte (NaOH) par un
1 TP Nº2 (Semestre 1) : Dosage dune base forte (NaOH) par un
Le but de ce TP est de vérifier la concentration molaire (inconnue) d'une solution d'hydroxyde de sodium NaOH préparée par dosage acido-basique. 4. Mode
 TP N°01 Le port de la blouse en coton blanche et assez longue est
TP N°01 Le port de la blouse en coton blanche et assez longue est
TP de Chimie 1. 11. TP N°03. Dosage Acido-basique. I. Introduction : ➢ Une des premières définitions d'un acide et d'une base a été proposée en 1887 par
 TP : Dosage acidobasique par pHmétrie
TP : Dosage acidobasique par pHmétrie
9 févr. 2018 TP : Dosage acidobasique par pHmétrie ... solution acide dans le bécher lors d'un dosage acido-basique et la solution basique dans la burette.
 TRAVAUX PRATIQUES DE CHIMIE DES SOLUTIONS
TRAVAUX PRATIQUES DE CHIMIE DES SOLUTIONS
TP N°3 : DOSAGE DES POLYACIDES A 25°C la neutralité acido-basique correspond à. pH=7
 Travaux Pratiques de Chimie 1 1 ère Année Licence (LMD) tronc
Travaux Pratiques de Chimie 1 1 ère Année Licence (LMD) tronc
TP N°03 : Titrage acido-basique. I. Introduction……………………………………………………………………………..20. II. Objectifs…………………………………………………………………..………….…..20. III. Généralités ...
 Dosages conductimétriques
Dosages conductimétriques
A - Introduction : Les dosages conductimétriques qui Nous n'étudierons ici
 Dosage dune solution aqueuse de peroxyde dhydrogène par
Dosage dune solution aqueuse de peroxyde dhydrogène par
TP dosage manganimetrie.DOC. Page 1 sur 4. Dosage d'une solution aqueuse de Introduction : Un antiseptique : l'eau oxygénée. Le peroxyde d'hydrogène de ...
 TP Chimie n° 3
TP Chimie n° 3
Dosage acido-basique en présence d'indicateurs colorés. (Dosage de l'acide acétique contenu dans le vinaigre). 1 Introduction. Le vinaigre de vin est un produit
 TRAVAUX PRATIQUES DE CHIMIE I
TRAVAUX PRATIQUES DE CHIMIE I
II. Introduction. Le dosage acidobasique est utilisé afin de déterminer la concentration inconnue d'une solution composée d'un acide ou d'une base
 TP CHIMIE-1 & TP CHIMIE-2
TP CHIMIE-1 & TP CHIMIE-2
I-Quelques recommandations en guise d'introduction . TP II : Le dosage acido-basique (cas d'un acide fort par une base forte) ....... 14.
 1 TP Nº2 (Semestre 1) : Dosage dune base forte (NaOH) par un
1 TP Nº2 (Semestre 1) : Dosage dune base forte (NaOH) par un
TP Nº2 (Semestre 1) : Dosage d'une base forte (NaOH) par un acide fort (HCl). 1. Introduction : Les réactions acido-basiques résultent du transfert d'un
 Travaux Pratiques de Chimie Générale (Génie Industriel)
Travaux Pratiques de Chimie Générale (Génie Industriel)
TP (03) : Dosage acido-basique…………………………………………………………… TP (04) : Titrage TP. ? Introduction à la démarche expérimentale : vous concevrez vous-mêmes vos.
 pH?7
pH?7
TP 3 Méthode de neutralisation (dosage acido-basique). Dosage de deux produits domestiques « le déboucheur et le vinaigre ». Introduction.
 Polycopie-TP-Chimie-1.pdf
Polycopie-TP-Chimie-1.pdf
DOSAGE ACIDO-BASIQUE. TPN°2. UHBChlef - S1 Licence LMD -ST- Polycopie TP Chimie 1 - Dr. Malika OUAGUED. Page 16. TP I – Dosage d'un acide fort par une base
 TP N 03 : Dosage dun acide fort par une base forte
TP N 03 : Dosage dun acide fort par une base forte
TP N. 0. 03 : Dosage d'un acide fort par une base forte. Objectifs : I- Introduction : L'acide sulfurique pur est un liq.
 Titrages acido-basiques
Titrages acido-basiques
Dosages acido-basiques conductimétriques. Spectrophotométrie (sera vu en TP). Dosage par ... dosage (-> introduction en faible quantité: une ou deux.
 Matière : Introduction aux techniques analytiques Responsable du
Matière : Introduction aux techniques analytiques Responsable du
Intitulé du TP : Dosage de l'acide citrique contenu dans un jus de citron On admet que l'équivalence acido-basique pour ce dosage se produit lorsque le ...
 [PDF] TP Chimie n° 3
[PDF] TP Chimie n° 3
Dosage acido-basique en présence d'indicateurs colorés (Dosage de l'acide acétique contenu dans le vinaigre) 1 Introduction Le vinaigre de vin est un produit
 [PDF] TRAVAUX PRATIQUES DE CHIMIE I
[PDF] TRAVAUX PRATIQUES DE CHIMIE I
II Introduction Le dosage acidobasique est utilisé afin de déterminer la concentration inconnue d'une solution composée d'un acide ou d'une base
 [PDF] TP : Dosage acidobasique par pHmétrie - cpge paradise
[PDF] TP : Dosage acidobasique par pHmétrie - cpge paradise
9 fév 2018 · TP : Dosage acidobasique par pHmétrie vendredi 9 février Objectifs : • Utiliser un pHmètre et un logiciel d'acquisition de données pour
 [PDF] Dosage dune base forte (NaOH) par un acide fort (HCl) 1 Introduction
[PDF] Dosage dune base forte (NaOH) par un acide fort (HCl) 1 Introduction
Le but de ce TP est de vérifier la concentration molaire (inconnue) d'une solution d'hydroxyde de sodium NaOH préparée par dosage acido-basique 4 Mode
 [PDF] DOSAGE ACIDO-BASIQUE Chaque groupe de TP rendra 1 seul
[PDF] DOSAGE ACIDO-BASIQUE Chaque groupe de TP rendra 1 seul
DOSAGE ACIDO-BASIQUE 1 BUT DU TP 1 1 On veut doser une solution d'acide chlorhydrique de concentration ca inconnue avec une
 [PDF] TP 3 Méthode de neutralisation (dosage acido-basique) Dosage de
[PDF] TP 3 Méthode de neutralisation (dosage acido-basique) Dosage de
Introduction Les acides et les bases sont des substances très utilisées dans notre vie quotidienne On les retrouve autour de soi pour nettoyer la maison
 [PDF] Polycopie-TP-Chimie-1pdf
[PDF] Polycopie-TP-Chimie-1pdf
Le dosage (ou titrage) acido-basique est utilisé afin de déterminer la concentration inconnue d'une solution composée d'un acide ou d'une base ou d'un mélange
 TP N°1 : DOSAGE DUNE SOLUTION DE SOUDE PAR - chimie
TP N°1 : DOSAGE DUNE SOLUTION DE SOUDE PAR - chimie
Le dosage acido-basique est utilisé afin de déterminer la concentration inconnue d'une solution composée d'un acide ou d'une base ou d'un mélange
 TP-cours : dosages acido-basiques - PDF Téléchargement Gratuit
TP-cours : dosages acido-basiques - PDF Téléchargement Gratuit
Définition : TP-cours : dosages acido-basiques Critères pour qu une Introduction : On va réaliser le dosage d une solution d acide éthanoïque (CH 3

UNIVERSITÉ MENTOURI 1 INSTITUT DES SCIENCES VÉTÉRINAIRES
DÉPARTEMENT PRÉCLINIC CHIMIE GÉNÉRALE 2019-2020
1TP Chimie n° 3
Dosage acido-NMVLTXH HQ SUpVHQŃH G LQGLŃMPHXUV ŃRORUpV GRVMJH GH O MŃLGH MŃpPLTXH ŃRQPHQX GMQV OH YLQMLJUHB1 Introduction
Le vinaigre de vin est un produit naturel. Son goût acide est dû à la présence d'acide acétique (ou acide éthanoïque : CH3-CO-OH) obtenu par l'oxydation de l'éthanol (CH3-CH2-OH) par le dioxygène de l'air.
2 Le principe du dosage
Chaque molécule d'acide acétique dissoute dans l'eau libère un proton H+, qui peut être neutralisé à l'aide d'un ion hydroxyde OH- provenant d'une base forte telle que NaOH, dont on connaît la concentration. Cette analyse s'appelle un titrage acide- base.͒Lorsque la quantité de base ajoutée est exactement équivalente à la quantité d'acide à titrer, le système est au point d'équivalence, point où la concentration en H+ est exactement égale à celle des OH-. Pour déterminer le point d'équivalence dans un titrage acide-base, deux méthodes sont employées principalement : l'emploi d'indicateurs colorés ou la mesure potentiométrique du pH lors du titrage. Pour ce TP, nous utiliserons la méthode de Les indicateurs sont des acides faibles organiques dont la forme protonée est d'une couleur différente de la forme non protonée.͒La relation suivante permet de calculer la concentration d'acide :CA .VA = CB .VB
CA = concentration de l'acide. VA = volume d'acide titré. CB = concentration de la base. VB = volume de base ajouté. Après avoir trouvé la concentration en mol/L d'acide dans l'eau, il faudra la convertir en concentration massique (g/L) pour pouvoir la comparer avec la valeur imprimée par le fabricant.UNIVERSITÉ MENTOURI 1 INSTITUT DES SCIENCES VÉTÉRINAIRES
DÉPARTEMENT PRÉCLINIC CHIMIE GÉNÉRALE 2019-2020
23 But de travail
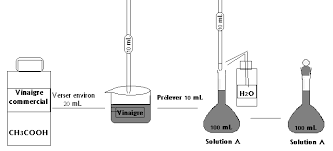
déterminé par dosage la concentration molaire en acide acétique de cette solution diluée de vinaigre.4 Matériels et produits
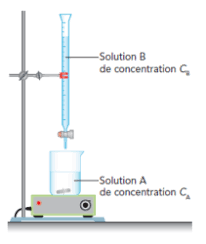
- Béchers,͒ - Fiole jaugée de 100 mL, - Pipette graduée, - Entonnoir, - Une burette graduée de 25ml, - Un agitateur magnétique avec barreau magnétique, - Erlenmeyer, - Statif, pince, noix, - Solution de soude de concentration 0,1 mol/L, - Solution diluée du vinaigre. - Un flacon de phénolphtaléine.Mode opératoire:
Fixez la burette sur son support et remplissez-la de NaOH de concentration 0,1 M, en prenant garde de faire la mise à zéro correctement.͒Choisissez un Erlenmeyer parfaitement propre et sec, puis, avec une pipette jaugée, prélevez exactement 10 mL de la solution A diluée de vinaigre (cette solution est 10 fois diluée).Versez-les dans l'Erlenmeyer.
Ajoutez 3 ou 4 gouttes de phénolphtaléine dans l'erlenmeyer. Mettez le barreau magnétique dans l'Erlenmeyer et réglez l'agitation de telle sorte qu'il n'y ait aucune éclaboussure.͒ A l'aide de la burette, ajoutez goutte à goutte la solution de NaOH jusqu'à ce qu'une coloration rose-violette apparaisse. Attention : le changement de couleur se fait à la goutte près ! Lisez le volume de NaOH ajouté et notez le résultat.Faites le titrage 2 fois de suite.
UNIVERSITÉ MENTOURI 1 INSTITUT DES SCIENCES VÉTÉRINAIRES
DÉPARTEMENT PRÉCLINIC CHIMIE GÉNÉRALE 2019-2020
35 Questions :
1. Donner le volume versé deq
3. Calculer la concentration molaire apportée CA en acide acétique dans la solution
diluée A.4. En déduire la concentration molaire apportée C0 en acide acétique dans le vinaigre
utilisé.quotesdbs_dbs2.pdfusesText_3[PDF] tp distillation simple pdf
[PDF] compte rendu de tp chimie preparation des solutions
[PDF] tp chaleur de dissolution enthalpie de dissolution
[PDF] preparation des solutions en chimie
[PDF] conclusion de tp chimie preparation des solutions
[PDF] tp extraction de l'adn d'oignon
[PDF] extraction d'adn de banane pdf
[PDF] tp extraction de l'adn d'oignon pdf
[PDF] tp extraction liquide liquide acide acétique
[PDF] tp extraction liquide liquide corrigé
[PDF] but de tp extraction liquide liquide
[PDF] correction tp distillation fractionnée
[PDF] tp extraction liquide liquide acide benzoique
[PDF] tp thermodynamique 2eme année chimie
